理想气体与真实气体
气体是物质存在的状态之一。它具有与固体和液体相矛盾的性质。气体没有顺序,它们占据任何给定的空间。它们的行为受温度、压力等变量的影响很大。
理想气体是什么?
理想气体是一个理论概念,我们用它来研究。为了使气体成为理想气体,它们应该具有以下特性。如果其中一个缺失,则该气体不被视为理想气体。
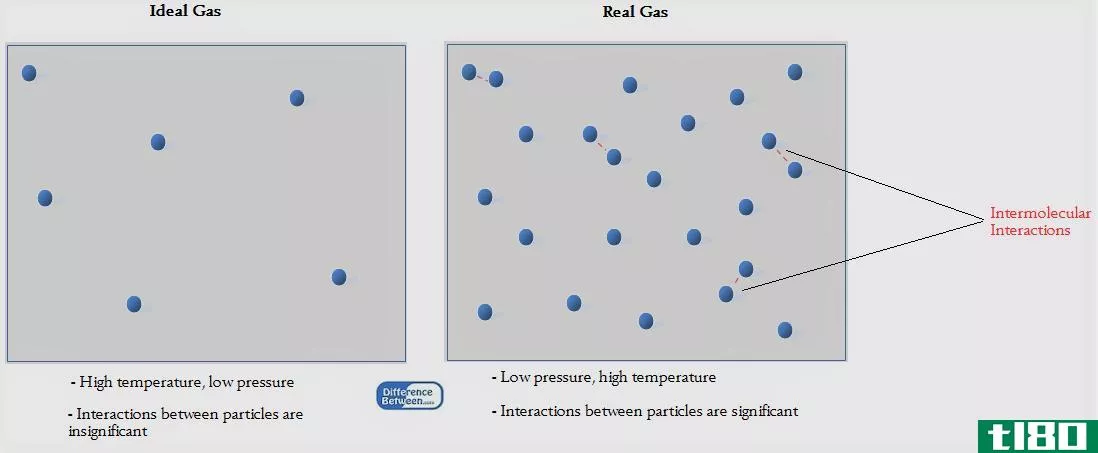
•气体分子之间的分子间作用力可以忽略不计。
•气体分子被视为点粒子。因此,与气体分子占据的空间相比,分子的体积微不足道。
通常气体分子填充任何给定的空间。因此,当一个大的空间被空气占据时,气体分子本身与空间相比是非常小的。因此,假设气体分子为点粒子在某种程度上是正确的。然而,有些气体分子的体积相当大。忽略卷会在这些实例中产生错误。根据第一个假设,我们必须考虑气体分子之间没有分子间的相互作用。然而,在现实中,它们之间至少存在着微弱的相互作用。但是,气体分子移动迅速且随机。因此,它们没有足够的时间与其他分子进行分子间的相互作用。因此,从这个角度来看,接受第一个假设也是有一定道理的。虽然我们说理想气体是理论上的,但我们不能说它是100%正确的。有些情况下,气体充当理想气体。理想气体有三个变量,压力、体积和温度。下面的方程式定义了理想气体。
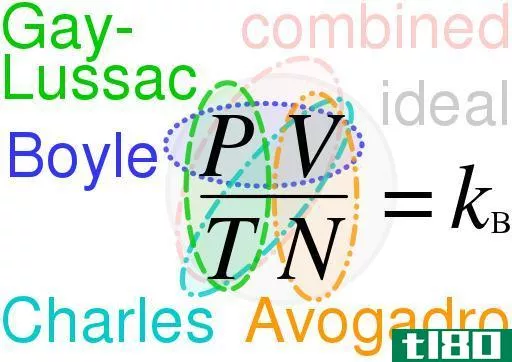
PV=nRT=NkT
P=绝对压力
V=体积
n=摩尔数
N=分子数
R=通用气体常数
T=绝对温度
K=玻尔兹曼常数
虽然有局限性,我们用上面的方程来确定气体的行为。
什么是真正的气体?
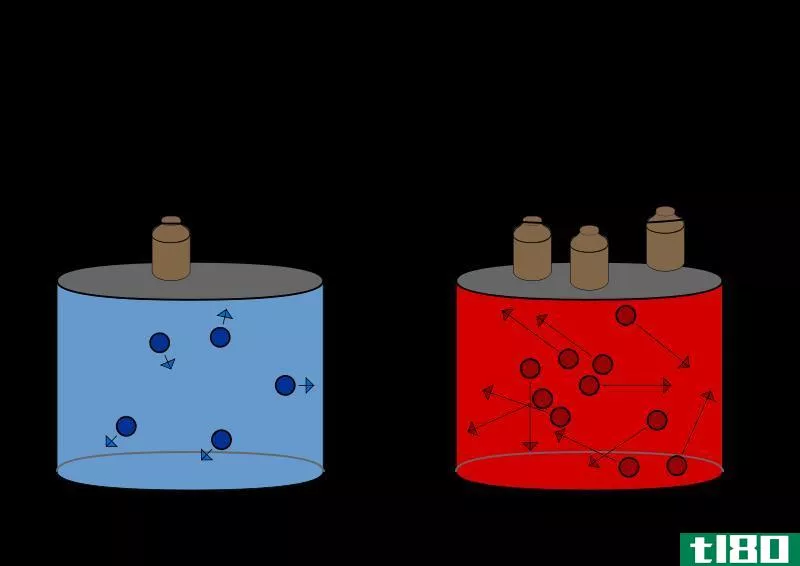
当上述两个或两个假设中的一个无效时,这种气体被称为真实气体。我们实际上在自然环境中遇到了真正的气体。真实气体在非常高的压力下与理想状态不同。这是因为,当施加非常高的压力时,填充气体的体积变得非常小。与空间相比,我们不能忽略分子的大小。此外,理想气体在很低的温度下达到真实状态。在低温下,气体分子的动能很低。因此,它们移动缓慢。正因为如此,气体分子之间会有分子间的相互作用,这是我们不能忽视的。对于实际气体,我们不能使用上述理想气体方程,因为它们的行为不同。对于实际气体的计算有更复杂的方程。
| 理想气体和真实气体的区别是什么?•理想气体没有分子间作用力,气体分子被视为点粒子。相反,真正的气体分子有一个大小和体积。此外,它们还具有分子间作用力。•在现实中找不到理想气体。但是气体在一定的温度和压力下会以这种方式表现。•气体在高压和低温下往往表现为真实的气体。真实气体在低压和高温下表现为理想气体。•理想气体可以与PV=nRT=NkT方程相关,而真实气体则不能。对于确定真实气体,有更复杂的方程。 |