理想气体定律和真实气体定律的关键区别在于,理想气体定律描述的是理论气体的行为,而真实气体定律描述的是宇宙中实际存在的气体的行为。
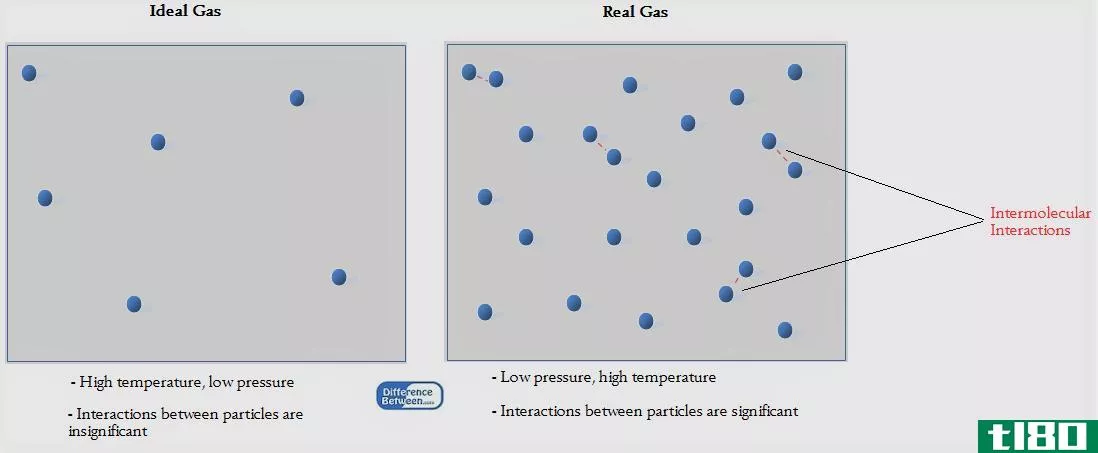
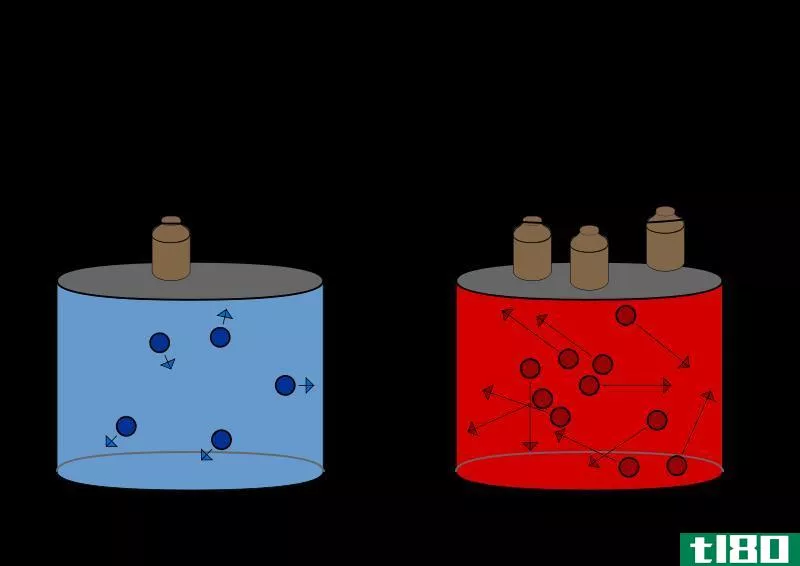
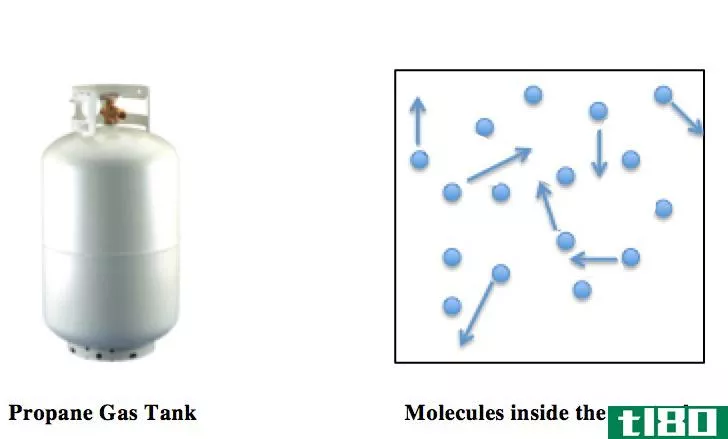
理想气体是一种理论气体,其随机运动的气体粒子之间没有其他相互作用,而是完全弹性碰撞。根据这个定义,我们可以理解这些理想气体在自然界中不可能出现,因为对于我们已知的任何气体来说,气体粒子之间基本上都存在相互作用。事实上,我们知道的气体是真正的气体。
目录
1. 概述和主要区别
2. 理想气体定律是什么
3. 什么是真正的气体定律
4. 并列比较-理想气体定律和实际气体定律的表格形式
5. 摘要
什么是理想气体定律(the ideal gas law)?
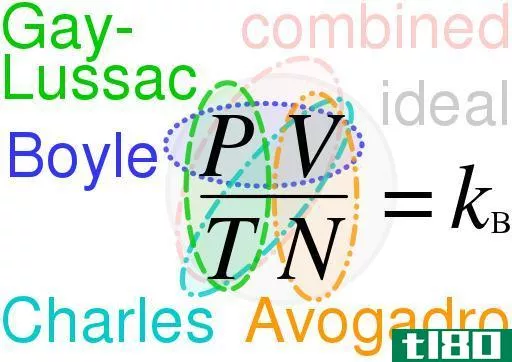
理想气体定律是描述理想气体行为的方程。理想气体是假想的,这些气体只在理论上出现。因此,利用理想气体定律,我们可以了解和估计我们所知道的许多实际气体的行为。然而,它有几个局限性。此外,这项法律是其他几项法律的结合:
- 波义耳定律
- 查尔斯定律
- 阿伏加德罗定律
- 盖卢萨克定律
计算
基本上,我们可以给出理想气体定律如下:;
PV=nRT
式中,P为压力,V为体积,T为理想气体的温度。这里,“n”是理想气体的摩尔数,“R”是一个常数,我们称之为理想气体常数。它有一个普适值,任何气体的R值都相同,为8.314j/(K·mol)。
此外,我们可以从这个定律得到不同的导数:摩尔形式,结合形式,等等。例如,因为“n”是摩尔数,我们可以用气体的分子量给出它。推导如下。
n=米/米
式中,n是气体的摩尔数,m是气体的质量,m是气体的分子量。通过使用上述方程式,
PV=nRT
PV=(m/m)室温
如果我们想得到气体的密度,我们可以使用上面的方程,如下所示:;
P=(m/VM)室温
P=ρRT/M
此外,如果我们想从理想气体定律得到组合气体定律,我们可以推导如下:对于“1”和“2”两种气体,压力、体积和温度分别为P1、V1、T1和P2、V2和T2。对于这两种气体,我们可以写出两个方程:;
P1V1=nRT1…………….(1)
(p22………..第2页)
通过将方程(1)与方程(2)分开,我们得到:,
(P1V1)/(P2V2)=T1/T2
我们可以把这个方程重新排列如下:;
P1V1/T1=P2V2/T2
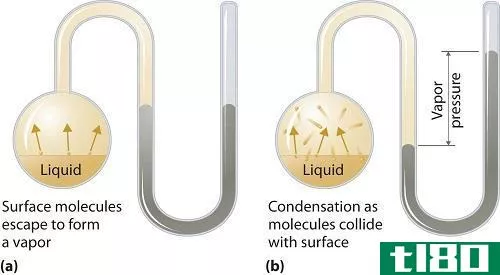
什么是真实气体定律(real gas law)?
真实气体定律,又称范德瓦尔斯定律,是从理想气体定律出发,用来描述真实气体的行为。由于真实气体不能理想地表现出来,所以真实气体定律改变了理想气体定律中的压力和体积成分。因此,我们可以得到如**积和压力:
实际气体体积=(Vm–b)
实际气体压力=(P+a{n2/V2})
然后,将这些修改后的组分应用到理想气体定律中,可以得到真实气体定律,如下所示:
(P+a{n2/V2})(Vm-b)=nRT
式中,Vm为气体摩尔体积,R为通用气体常数,T为实际气体温度,P为压力。
理想气体定律(ideal gas law)和真实气体定律(real gas law)的区别
理想气体定律是描述理想气体行为的方程。真实气体定律是从理想气体定律中推导出来的,以适应实际气体的行为。理想气体定律和真实气体定律的关键区别在于理想气体定律描述的是理论气体的行为,而真实气体定律描述的是宇宙中实际存在的气体的行为。
另外,我们可以从理想气体方程中推导出。
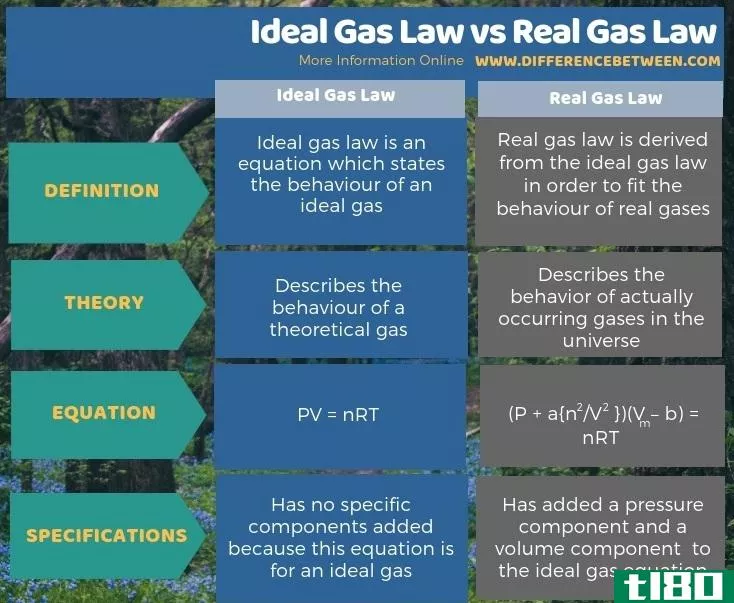
总结 - 理想气体定律(ideal gas law) vs. 真实气体定律(real gas law)
简言之,理想气体是一种假设的物质,它在气体粒子之间有完全的弹性碰撞,这是我们所知的大多数真实气体所没有表现出来的性质。理想气体定律和真实气体定律的关键区别在于,理想气体定律描述的是理论气体的行为,而真实气体定律描述的是宇宙中实际存在的气体的行为。
引用
1理想气体定律,超物理。乔治亚州立大学,这里有。