拉乌尔定律和道尔顿定律的主要区别在于,拉乌尔定律处理固体或液体的蒸气压,而道尔顿定律处理的是非反应气体的分压。
劳尔定律和道尔顿定律是化学中解释气态分压的重要定律。拉乌尔定律描述了改变溶质浓度时溶液蒸汽分压的行为。相反,道尔顿定律描述的是同一容器中非反应气体的行为。
目录
1. 概述和主要区别
2. 什么是拉乌尔定律
3. 什么是道尔顿定律
4. 并列比较——拉乌尔定律和道尔顿定律的表格形式
6. 摘要
什么是拉乌尔定律(raoult law)?
拉乌尔定律指出,溶剂在溶液上方的蒸汽压等于纯溶剂在相同温度下的蒸汽压,该温度由溶液中溶剂的摩尔分数标度。我们可以从数学上给出这种关系如下:
解=X溶剂.正溶剂
其中Psoltuion是溶液的蒸气压,Xsolvent是溶剂的摩尔分数,Posolvent是纯溶剂的蒸气压。这一定律是由法国化学家弗朗索瓦·玛丽·拉乌尔于1880年制定的。他发现,当向溶液中添加溶质时,溶液的蒸气压逐渐降低。然而,这种观察依赖于两个变量:溶解溶质的摩尔分数和纯溶剂的蒸气压。
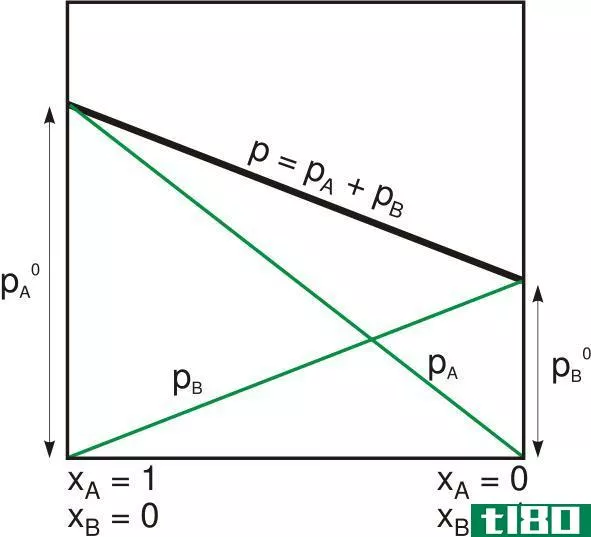
图01:遵循拉乌尔定律的二元溶液的蒸汽压
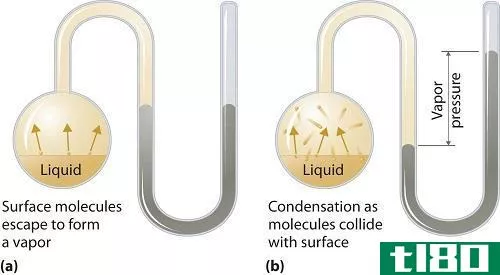
在特定固体或液体的给定压力下,存在一个压力,在该压力下,物质的蒸汽与固体或液体形式的物质达到平衡。在这个温度下,我们把物质上方的压力称为蒸汽压。此外,在这个平衡点上,固体或液体物质的蒸发速率等于凝结回固体或液体形式的蒸汽。因此,这是拉乌尔定律背后的基本理论。然而,拉乌尔定律适用于理想解。但它也能很好地与溶剂在非常稀的状态。对于真实物质(非理想物质),蒸气压的下降实际上大于我们根据拉乌尔定律计算的值。
什么是道尔顿定律(dalton law)?
道尔顿定律指出,非反应气体混合物的总压力等于每种气体的分压之和。这项法律是约翰·道尔顿于1802年制定的。我们可以从数学上给出这个定律如下:
Ptotal=π
式中,Ptotal是气体混合物的总压力,而Pi是每种气体的分压。
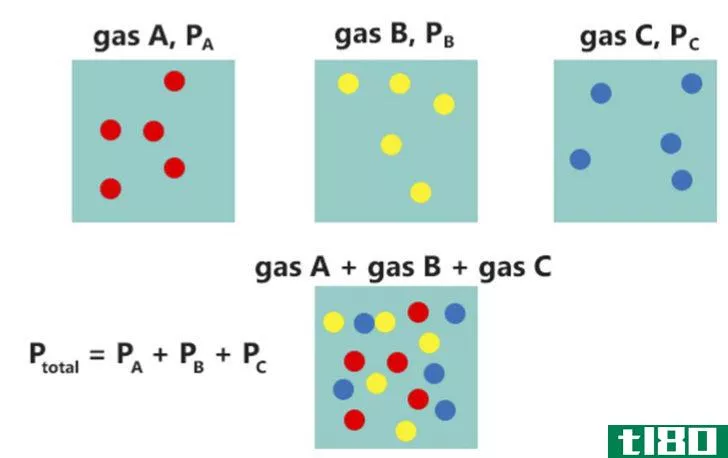
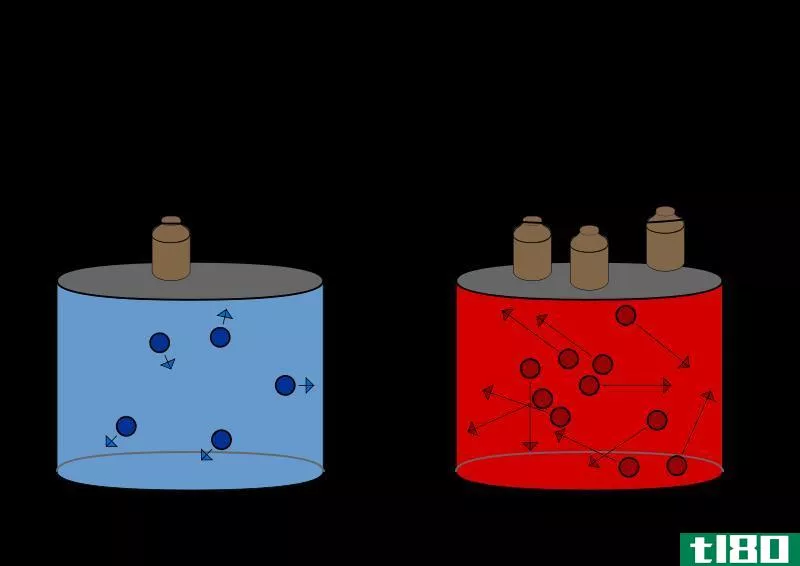
图02:道尔顿定律
例如,如果我们有一种含有三种成分的非反应性气体混合物,我们可以将关系式写如下:
Ptotal=P1+P2+P3
拉乌尔定律(raoult law)和道尔顿定律(dalton law)的区别
劳尔定律和道尔顿定律是化学中解释气态分压的重要定律。拉乌尔定律和道尔顿定律的主要区别在于,拉乌尔定律处理固体或液体的蒸气压,而道尔顿定律处理的是非反应气体的分压。也就是说,拉乌尔定律指出,溶液上方溶剂的蒸汽压等于纯溶剂在相同温度下的蒸汽压,该温度由溶液中溶剂的摩尔分数标度。同时,道尔顿定律指出,非反应气体混合物的总压力等于每种气体分压之和。拉乌尔定律的数学表达式是Psolution=X溶剂.正溶剂道尔顿定律的数学表达式是Ptotal=Pi。

总结 - 拉乌尔定律(raoult law) vs. 道尔顿定律(dalton law)
劳尔定律和道尔顿定律是化学中解释气态分压的重要定律。然而,拉乌尔定律和道尔顿定律的关键区别在于,拉乌尔定律处理的是固体或液体的蒸气压,而道尔顿定律处理的是非反应气体的分压。
引用
1赫尔曼斯汀,安妮·玛丽。“拉乌尔化学定律定义”,ThoughtCo,2019年1月9日,可在这里查阅。