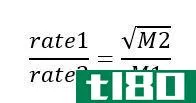定比例定律和多重比例定律的关键区别在于,定比例定律规定化合物的样品中的元素质量比例始终相同。相反,多重比例定律(有时称为道尔顿定律)指出,如果两个元素结合形成一个以上的化合物,那么第二个元素的质量与第一个元素的固定质量的比率将是小整数的比率。
定比定律和倍率定律是用来解释化学计量比的理论。化学计量学是对化学反应中反应物和产物的相对数量的量度。
目录
1. 概述和主要区别
2. 什么是定比例定律
3. 什么是多重比例定律
4. 并列比较-确定比例定律与表格形式的多重比例法则
5. 摘要
什么是定比例律(law of definite proporti***)?
定比例定律指出,化合物的样品总是含有相同质量比例的元素。换句话说,一个给定的化合物总是以相同的质量比例包含相同的元素。
例如,无论是自来水还是海水,水分子总是以以下比例含有氢和氧元素。
水分子的化学式为H2O
水分子摩尔质量=18 g/mol
因此,一摩尔水含有18克水,水分子中H和O的比例是2:1。因此,水中氢的质量分数=(2g/18g)x100%=11.11%,氧的质量分数=(16g/18g)x100%=88.89%。当水源和分离方法不同时,这些组分是确定的,不会改变。

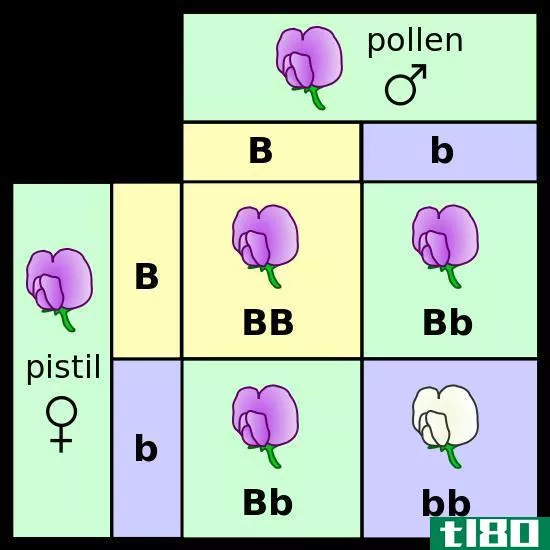
图01:定比例定律表明,在一种给定的化学物质中,元素总是以相同的质量比例结合在一起。
这个定律的基础是同一元素的任何原子(原子序数相同的原子)彼此相似。对于上面的例子,我们认为任何氢原子都与另一个氢原子相似,反之亦然。但也有一些例外。例如,一种元素的同位素组成可能因来源而异。因此,化学计量学显示了基于元素来源的变化。
什么是多比例定律(law of multiple proporti***)?
多比例定律指出,当两个元素相互结合形成一个以上的化合物时,一个元素的权重与另一个元素的固定权重成小整数比。
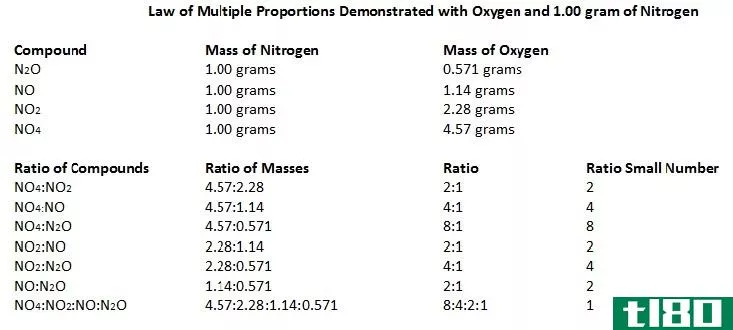
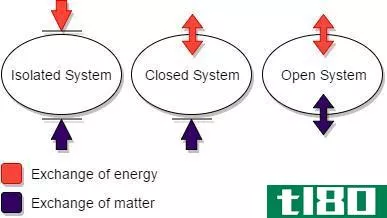
图02:多重比例定律的解释
这有时被称为道尔顿定律。那是在1803年约翰道尔顿发现这条定律之后。让我们用一些例子来理解这个定律。
- 氮氧化物由氮原子和氧原子组成。存在五种不同的氮氧化物:N2O、NO、N2O3、NO2和N2O5。当考虑这些化合物中氮和氧的质量比时,14克氮原子与8克、16克、24克、32克和40克氧按质量比结合。当取小整数时,比率为1:1、1:2、1:3、1:4和1:5。
定比律与倍数律的区别?
定比例定律指出,化合物的样品总是含有相同质量比例的元素。另一方面,多重比例定律强调,当两个元素相互结合形成一个以上的化合物时,一个元素的权重与另一个元素的固定权重是小整数的比率。这就是定比律与倍比律的主要区别。

总结 - 定比例律(law of definite proporti***) vs. 多比例定律(law of multiple proporti***)
化学反应中化合物的化学计量学可以用定比定律和多重比定律来解释。定比例定律指出,化合物的样品总是含有相同比例的元素。相反,多重比例定律指出,如果两种元素结合形成一种以上的化合物,那么第二种元素的质量与第一种元素的固定质量之比将是小整数之比。因此,这就是定比律与倍比律的区别。
引用
1Helmenstine,Anne Marie,博士,“确定比例法的定义”,ThoughtCo,2017年11月14日。可在此处获取2。大英百科全书的编辑。“固定比例法”,《大英百科全书》,大英百科全书公司,2017年2月3日。这里有3个。“化学计量学”,维基百科,维基媒体基金会,2018年2月25日。此处提供
2大英百科全书的编辑。“固定比例法”,《大英百科全书》,大英百科全书公司,2017年2月3日。
三。“化学计量学”,维基百科,维基媒体基金会,2018年2月25日。