关键区别-组合气体定律与理想气体定律
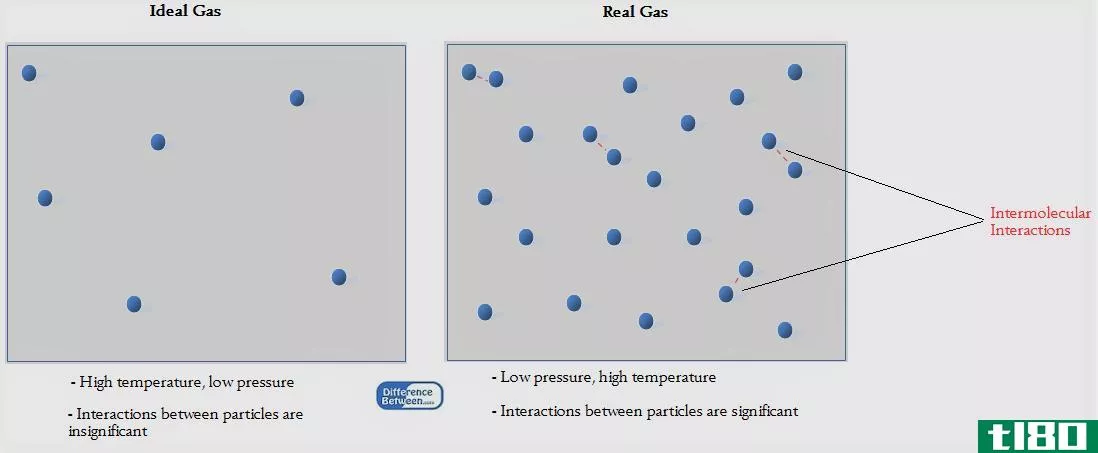
在研究不同气体时,气体的体积、压力、温度和气体存在量之间的关系非常重要。这些关系由理想气体定律和组合气体定律给出。在解释这些定律时,通常使用“理想气体”一词。理想气体在现实中并不存在,而是一种假设的气体化合物。气体分子之间没有分子间的作用力。然而,当提供适当的条件(温度和压力)时,一些气体可以作为理想气体。气体定律是为理想气体而产生的。当把这些气体定律用于实际气体时,需要考虑一些修正。组合气体定律是三种气体定律的组合:博伊尔定律、查尔斯定律和盖伊·卢萨克定律。组合气体定律与理想气体定律的主要区别在于,组合气体定律是三种气体定律的集合,而理想气体定律是单个气体定律的集合。
目录
1. 概述和关键区别
2. 什么是组合气体定律
3. 理想气体定律是什么
4.组合气体定律与理想气体定律的关系
5. 并排比较——组合气体定律与理想气体定律的表格形式
6. 摘要
什么是混合气体定律(combined gas law)?
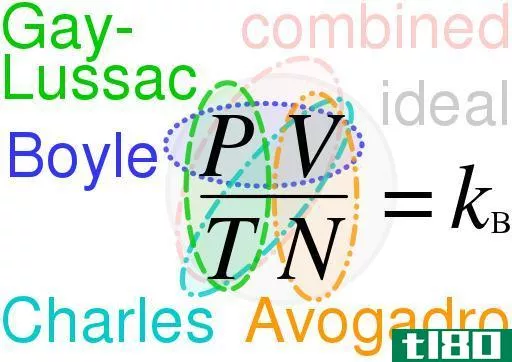
组合气体定律是由三种气体定律组合而成的:波义耳定律、查尔斯定律和盖卢萨克定律。组合气体定律表明,气体的压力与体积乘积与绝对温度之比等于常数。
PV/T=k
式中P为压力,V为体积,T为温度,k为常数。当组合气体定律与阿伏伽德罗定律一起使用时,它会产生理想气体定律。综合气体法没有所有者或发现者。上述关系也可以给出如下。
P1V1/T1=P2V2/T2
这给出了理想气体在两种状态下的体积、温度和压力之间的关系。因此,该方程可用于解释和预测初始状态或最终状态下的这些参数。
波义耳定律
在恒定温度下,理想气体的体积与该气体的压力成反比。这意味着初始压力(P1)和初始体积(V1)的乘积等于相同气体的最终压力(P2)和最终体积(V2)的乘积。
P1V1=P2V2
查尔斯定律
在恒定压力下,理想气体的体积与该气体的温度成正比。这条法律可以给出如下。
V1/T1=V2/T2
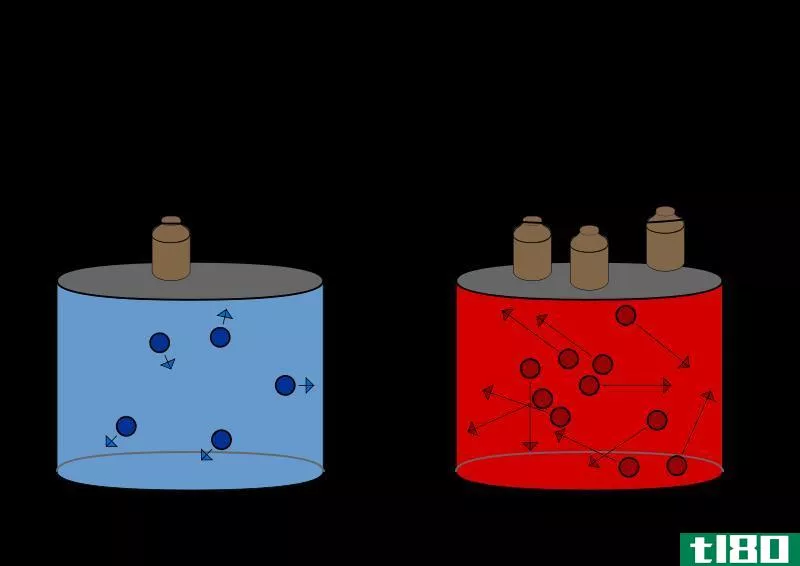
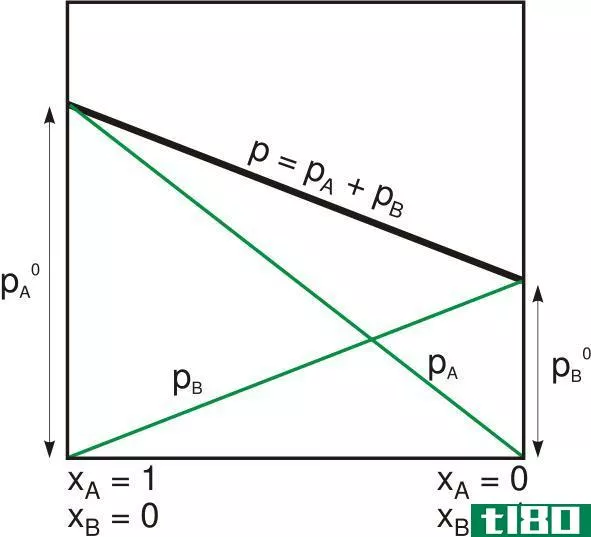
图01:压力-体积定律图解
盖卢萨克定律
在恒定体积下,理想气体的压力与同一气体的温度成正比。可以给出如下公式:,
P1/T1=P2/T2
什么是理想气体定律(ideal gas law)?
理想气体定律是化学中的一个基本定律,它表明理想气体的压力(P)和体积(V)的乘积与温度(T)和气体的若干粒子数(n)的乘积成正比。
PV=kNT
这里,k是一个比例常数。它被称为玻尔兹曼常数。该常数的值为1.38 x 10-23 J/K。然而,理想气体的简单表达式如下。
PV=nRT
式中,n是气体的摩尔数,R是8.314 Jmol-1K-1给出的通用气体常数。这个方程只适用于理想气体。如果它需要用于实际气体,则需要进行一些修正,因为真实气体与理想气体有许多不同之处。
这个新方程被称为范德瓦尔斯方程。如下所示。
(P+a{n/V}2)({V/n}-b)=RT
在这个方程中,“a”是一个常数,它取决于气体的类型,b也是一个常数,它给出了每摩尔气体的体积(被气体分子占据)。
什么是组合气体定律与理想气体定律的关系(the relati***hip between combined gas law and ideal gas law)?
- 当组合气体定律与阿伏伽德罗定律一起使用时,它会产生理想气体定律。
混合气体定律(combined gas law)和理想气体定律(ideal gas law)的区别
| 组合气体定律与理想气体定律 | |
| 组合气体定律是由三种气体定律组合而成的:博伊尔定律、查尔斯定律和盖卢萨克定律。 | 理想气体定律是化学中的一个基本定律,它表明理想气体的压力(P)和体积(V)的乘积与温度(T)和气体中若干粒子(n)的乘积成正比。 |
| 形成 | |
| 盖尔定律和盖尔定律结合而成。 | 理想气体定律是一个独立的定律。 |
| 方程式 | |
| 组合气体定律由PV/T=k给出 | 理想气体定律由PV=nRT给出 |
总结 - 混合气体定律(combined gas law) vs. 理想气体定律(ideal gas law)
气体定律用于理解和预测气体的行为和性质。组合气体定律与理想气体定律的区别在于,组合气体定律是三种气体定律的集合,而理想气体定律是单个气体定律。组合气体定律是由波义耳定律、查尔斯定律和盖卢萨克定律组成的。
引用
1.赫尔曼斯汀,安妮·玛丽。“理解化学中的混合气体定律。”ThoughtCo。这里有2.Helmenstine,Anne Marie。“理想气体定律是什么?复习一下你的化学概念。“ThoughtCo。在这里3。”理想气体定律和组合气体定律有什么不同?|苏格拉底“,组织。此处提供
2.赫尔曼斯汀,安妮·玛丽。“理想气体定律是什么?复习你的化学概念。
3.“理想气体定律与组合气体定律有何不同?|苏格拉底“,组织。