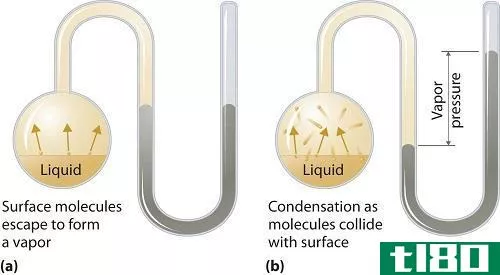
理想气体(ideal gas)和非理想气体示例问题(non-ideal gas example problem)的区别
这个示例问题演示了如何使用理想气体定律和范德华方程计算气体系统的压力。它还说明了理想气体和非理想气体之间的区别。


范德华方程问题
在-25°C温度下,使用a计算0.2000 L容器中0.3000 mol氦施加的压力。理想气体定律。范德华方程非理想气体和理想气体之间的区别是什么?给定值:aHe=0.0341 atm·L2/mol2He=0.0237 L·mol
如何解决这个问题
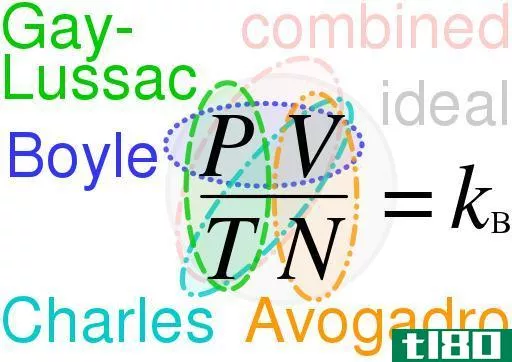
第1部分:理想气体定律理想气体定律用以下公式表示:PV=nRTW其中P=压力EV=体积=气体摩尔数R=理想气体常数=0.08206 L·atm/mol·KT=绝对温度和绝对温度et=°C+273.15T=-25+273.15T=248.15 KFind压力PV=nRTP=nRT/VP=(0.3000 mol)(0.08206 L·atm/mol·K)(248.15)/0.2000 LPideal=30.55 atmPart 2:Van der Waals方程Van der Waals方程由公式P+a(n/V)2=nRT/(V-nb)表示式中,P=压力EV=体积=气体摩尔数a=单个气体颗粒之间的吸引力B=单个气体颗粒的平均体积R=理想气体常数=0.08206 L·atm/mol·KT=绝对温度压力溶解度EP=nRT/(V-nb)-a(n/V)2为了使数学更容易理解,方程将分为两部分,其中P=X-Y其中X=nRT/(V-nb)Y=a(n/V)2X=P=nRT/(V-nb)X=(0.3000 mol)(0.08206 L·atm/mol·K)(248.15)/[0.2000 L-(0.3000 mol)(0.0237 L/mol)]X=6.109 L·atm/(0.2000 L-.007 L)X=6.109 L·atm/0.19 LX=32.152 atmY=a(n/V)2Y=0.0341·atm/mol/0.2000 L]2Y=0.0341 atm·L2/mol2 x(1.5 mol/L)2Y=0.0341 atm·L2/mol2 x 2.25 mol2/L2Y=0.077 atmRecombine,求出压力ep=x-YP=32.152 atm-0.077 atm非理想=32.075 atmPart 3-求出理想和非理想条件之间的差异非理想-Pideal=32.152 atm-30.55 atm非理想-Pideal=1.602 atmAnswer:理想气体的压力为30.55 atm,非理想气体的压力为30.55 atm非理想气体的范德华方程为32.152atm。非理想气体的压力大1.602 atm。
完美的(ideal) vs. 非理想气体(nonideal gases)
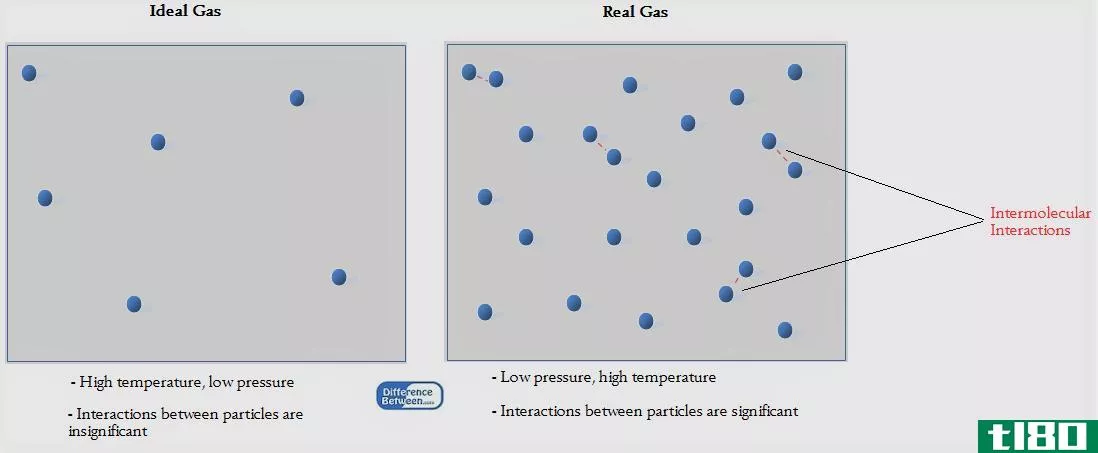
理想气体是分子之间不相互作用,也不占据任何空间的气体。在理想世界中,气体分子之间的碰撞是完全弹性的。现实世界中的所有气体都有直径相同的分子,它们相互作用,所以使用任何形式的理想气体定律和范德华方程都会有一些误差。
然而,惰性气体的作用很像理想气体,因为它们不参与与其他气体的化学反应。特别是氦,它的作用就像一种理想气体,因为每个原子都很小。
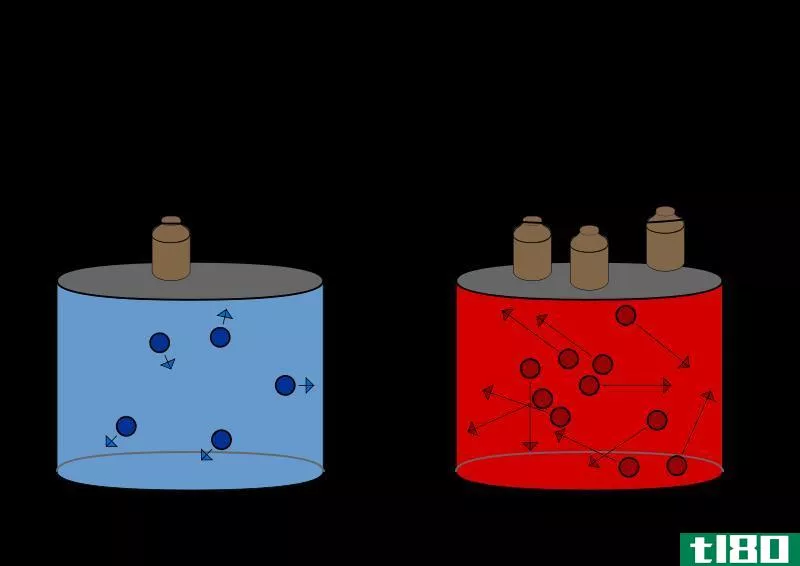
其他气体在低压和低温下的行为与理想气体非常相似。低压意味着气体分子之间很少发生相互作用。低温意味着气体分子的动能较低,因此它们不会四处移动,彼此或容器之间不会发生相互作用。
- 发表于 2021-10-14 06:36
- 阅读 ( 312 )
- 分类:数学
你可能感兴趣的文章
通用气体常数(universal gas constant)和特征气体常数(characteristic gas constant)的区别
...,其他元素中只有11种元素以气体的形式存在。然而,“理想气体定律”给了我们一个可以用来解释正常气体行为的方程。它有一个比例常数,称为通用气体常数,当它应用于实际气体时,这个常数是经过修改后使用的。然后它...
- 发布于 2020-09-22 22:50
- 阅读 ( 573 )
水煤气(water gas)和发生炉煤气(producer gas)的区别
... 水煤气和发生炉煤气的主要区别在于,水煤气含有易燃气体,而发生炉煤气同时含有易燃和不可燃气体。 水煤气和发生炉煤气都是几种气体的混合物。水煤气含有一氧化碳和氢气。发生炉煤气中含有一氧化碳和氢气以及一些...
- 发布于 2020-10-17 15:50
- 阅读 ( 659 )
理想气体定律(ideal gas law)和范德瓦尔斯方程(van der waals equation)的区别
关键区别——理想气体定律与范德瓦尔斯方程 理想气体定律是一个基本定律,而范德瓦尔斯方程是理想气体定律的修正版本。理想气体定律与范德瓦尔斯方程的主要区别在于,理想气体定律方程适用于理想气体,而范德瓦尔...
- 发布于 2020-10-19 04:40
- 阅读 ( 764 )
混合气体定律(combined gas law)和理想气体定律(ideal gas law)的区别
关键区别-组合气体定律与理想气体定律 在研究不同气体时,气体的体积、压力、温度和气体存在量之间的关系非常重要。这些关系由理想气体定律和组合气体定律给出。在解释这些定律时,通常使用“理想气体”一词。理想...
- 发布于 2020-10-19 04:51
- 阅读 ( 622 )
理想气体定律(ideal gas law)和真实气体定律(real gas law)的区别
理想气体定律和真实气体定律的关键区别在于,理想气体定律描述的是理论气体的行为,而真实气体定律描述的是宇宙中实际存在的气体的行为。 理想气体是一种理论气体,其随机运动的气体粒子之间没有其他相互作用,而...
- 发布于 2020-10-20 21:30
- 阅读 ( 865 )
气体(gas)和汽油(petrol)的区别
...。它含有轻质碳氢化合物和一些添加剂的混合物,以提高理想的性能。我们可以用原油生产汽油;一般来说,42加仑的原油可以产生19加仑的汽油。 图02:加油站 通常,这种燃料中的碳氢化合物混合物含有从C4到C12的分子。因此...
- 发布于 2020-10-29 19:45
- 阅读 ( 439 )
氩气(argon)和窗户用氪气填充物(krypton gas fillers for windows)的区别
...效率更高。它是由组件组成,使它成为不同形式的窗户的理想选择,它的性能比氩气更好。 氪气对于宽度约四分之一英寸的窄窗和三窗玻璃是理想的选择。在窄窗玻璃中,氪气的性能最佳,因为这种宽度在提供能源的同时,提...
- 发布于 2021-06-22 15:06
- 阅读 ( 378 )
油(oil)和气体(gas)的区别
...燃料的使用。 残余燃料含有相对较高的硫,并且具有不理想的特性,这使得它不太有用,而且也是最便宜的。它也不能用于汽车或车辆,因为使用前需要加热。在工业部门,天然气已经取代了石油,天然气战胜了石油,因为它...
- 发布于 2021-06-23 02:47
- 阅读 ( 361 )
分压(partial pressure)和蒸汽压(vapor pressure)的区别
...用力较强的溶液中,蒸气压较小。 蒸汽压也可以发生在理想的混合物中,这可以用拉乌尔定律来解释。它指出,液体或固体混合物**定组分的部分蒸汽压等于该组分的蒸汽压乘以给定温度下该混合物中该组分的摩尔分数。下面的...
- 发布于 2021-06-25 01:21
- 阅读 ( 521 )
理想溶液(ideal solution)和非理想溶液(non ideal solution)的区别
主差理想解(main difference ideal solution) vs. 非理想溶液(non ideal solution) 理想溶液是具有与理想气体混合物相似性质的溶液。然而,理想气体中气体分子之间没有相互作用。但是我们不能在溶液中考虑同样的情况,因为溶液中...
- 发布于 2021-06-29 11:30
- 阅读 ( 694 )