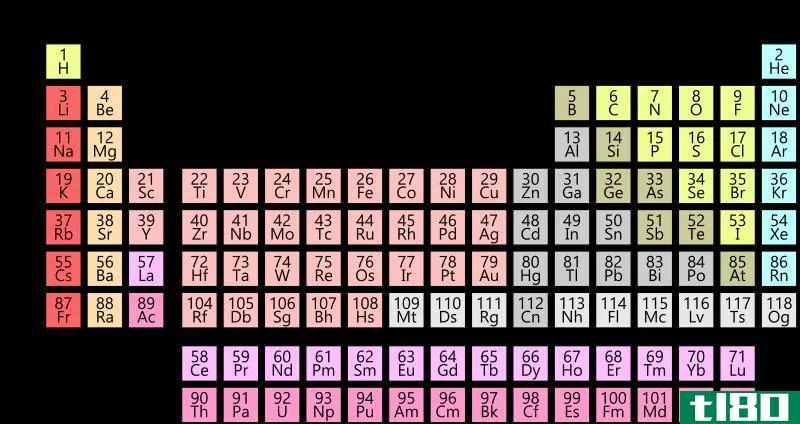
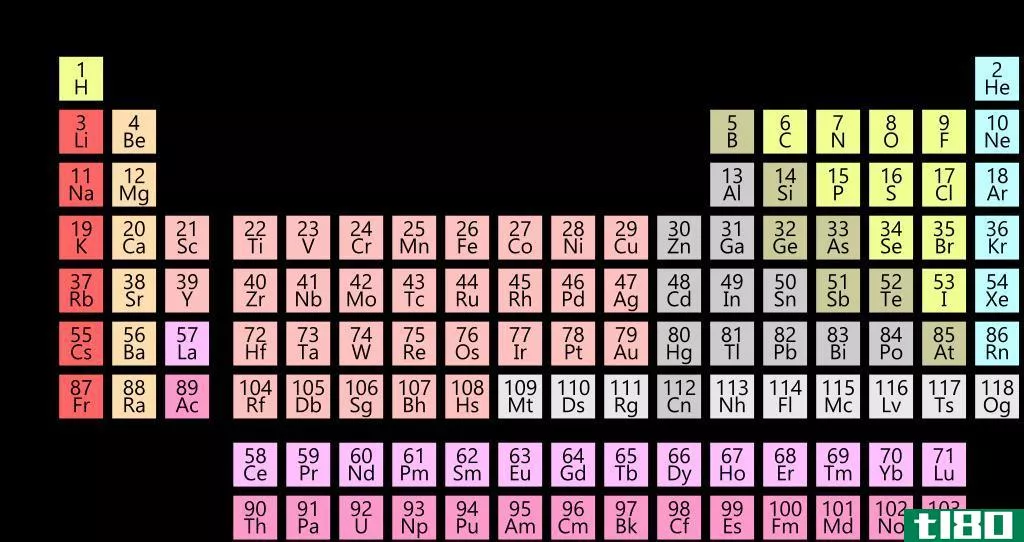
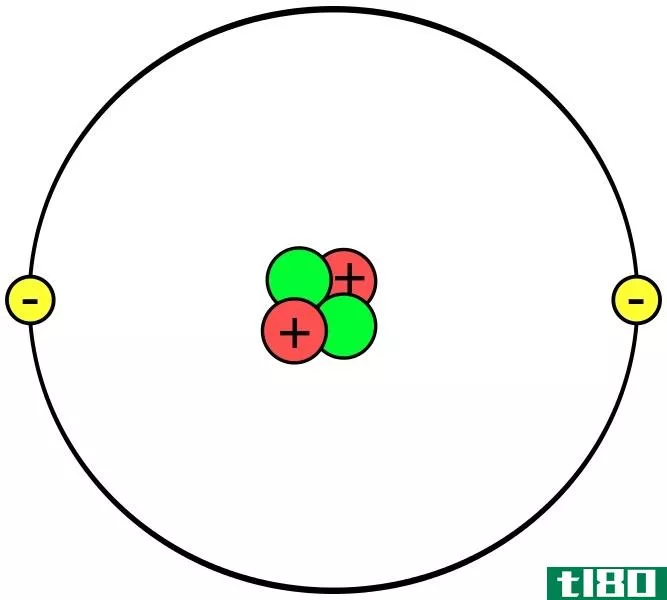
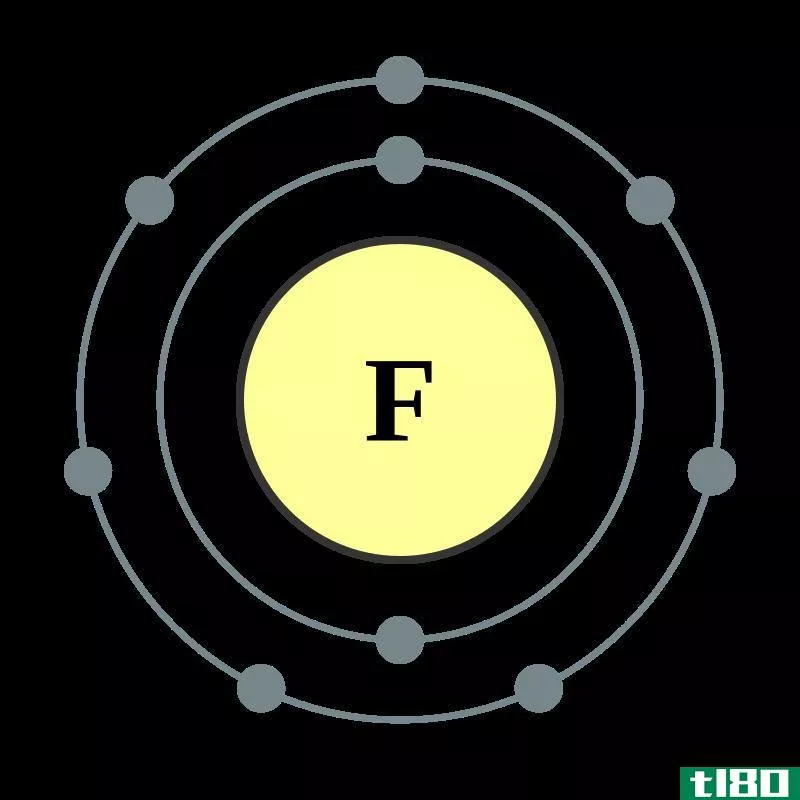
周期表的前20个元素
01
二十
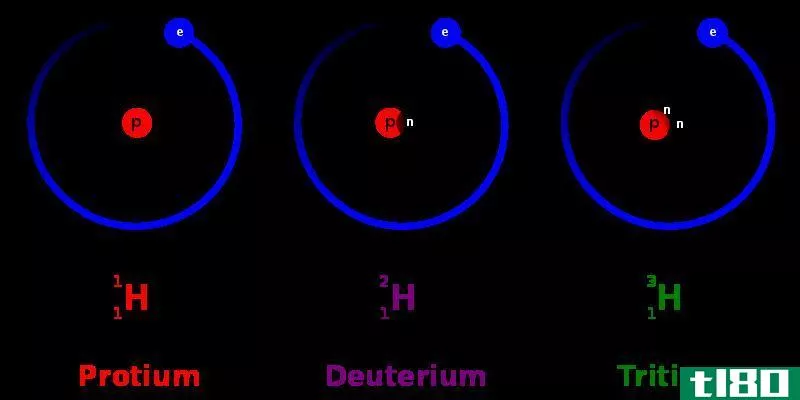
氢

在正常条件下,氢是一种非金属无色气体。它在极端压力下变成碱金属。
原子序数:1
符号:H
原子质量:1.008
电子构型:1s1
组:第1组,s型块,非金属
02
二十
氦

氦是一种轻的无色气体,形成无色液体。
原子序数:2
符号:他
原子质量:4.002602(2)
电子构型:1s2
组:18组,s区块,惰性气体
03
二十
锂

锂是一种活性银金属。
原子序数:3
文号:李
原子质量:6.94(6.938-6.997)
电子构型:[He]2s1
组:第1组,s-块,碱金属
04
二十
铍

铍是一种闪亮的灰白色金属。
原子序数:4
符号:Be
原子质量:9.0121831(5)
电子构型:[He]2s2
组:第2组,s-块,碱土金属
05
二十
硼

硼是一种具有金属光泽的灰色固体。
原子序数:5
符号:B
原子质量:10.81(10.806–10.821)
电子构型:[He]2s2 2p1
组:13组,p-块,类金属
06
二十
碳

碳有几种形式。它通常是灰色或黑色固体,尽管钻石可能是无色的。
原子序数:6
符号:C
原子质量:12.011(12.0096-12.0116)
电子构型:[He]2s2 2p2
组:组14,p-块,通常为非金属,但有时被视为类金属
07
二十
氮

氮气在普通条件下是无色气体。冷却后形成无色液体和固体。
原子序数:7
符号:N
原子质量:14.007
电子构型:[He]2s2 2p3
组:第15组(pnictogens),p-块,非金属
08
二十
氧气

氧是无色气体。它的液体是蓝色的。固态氧可以是几种颜色中的任何一种,包括红色、黑色和金属色。
原子序数:8
符号:O
原子质量:15.999或16.00
电子构型:[He]2s2 2p4
组:第16组(硫属),p-块,非金属
09
二十
氟

氟是淡黄色的气体和液体以及亮黄色的固体。固体可以是不透明的,也可以是半透明的。
原子序数:9
符号:F
原子质量:18.998403163(6)
电子构型:[He]2s2 2p5
组:第17组,p-块,卤素
10
二十
霓虹的

氖是一种无色气体,在电场中被激发时会发出特有的橙红色辉光。
原子序数:10
符号:东北
原子质量:20.1797(6)
电子构型:[He]2s2 2p6
组:第18组,p区块,惰性气体
11
二十
钠

钠是一种柔软的银白色金属。
原子序数:11
符号:Na
原子质量:22.98976928(2)
电子构型:[Ne]3s1
组:第1组,s-块,碱金属
12
二十
镁

镁是一种闪亮的灰色金属。
原子序数:12
符号:Mg
原子质量:24.305
电子构型:[Ne]3s2
组:第2组,s-块,碱土金属
13
二十
铝

铝是一种柔软的银色非磁性金属。
原子序数:13
符号:Al
原子质量:26.9815385(7)
电子构型:[Ne]3s2 3p1
组:组13,p-块,被认为是后过渡金属或有时是类金属
14
二十
硅

硅是一种坚硬的蓝灰色晶体固体,具有金属光泽。
原子序数:14
符号:Si
原子质量:28.085
电子构型:[Ne]3s2 3p2
组:第14组(碳基),p-块,非金属
15
二十
磷

磷在普通条件下是固体,但有几种形式。最常见的是白磷和红磷。
原子序数:15
符号:P
原子质量:30.973761998(5)
电子构型:[Ne]3s2 3p3
组:第15组(pnictogens),p-块,通常被认为是非金属,但有时是类金属
16
二十
硫黄

硫是黄色固体。
原子序数:16
符号:S
原子质量:32.06
电子构型:[Ne]3s2 3p4
组:第16组(硫属),p-块,非金属
17
二十
氯

在正常条件下,氯是一种浅黄绿色气体。它的液体形态是亮黄色。
原子序数:17
符号:Cl
原子质量:35.45
电子构型:[Ne]3s2 3p5
组:第17组,p-块,卤素
18
二十
氩

氩是无色的气体、液体和固体。当在电场中被激发时,它会发出明亮的紫丁香色光芒。
原子序数:18
符号:Ar
原子质量:39.948(1)
电子构型:[Ne]3s2 3p6
组:第18组,p区块,惰性气体
19
二十
钾

钾是一种活泼的银色金属。
原子序数:19
符号:K
原子质量:39.0983(1)
电子组态:[Ar]4s1
组:第1组,s-块,碱金属
20
二十
钙

钙是一种暗银色金属,有一种淡黄色的铸件。
原子序数:20
符号:Ca
原子质量:40.078(4)
电子构型:[Ar]4s2
组:第2组,s-块,碱土金属
- 发表于 2021-09-22 00:37
- 阅读 ( 249 )
- 分类:化学
你可能感兴趣的文章
钠(natrium)和钠(sodium)的区别
...号是钠,它来自于它的拉丁名钠。这个化学元素位于元素周期表的第1组和第3周期。因此,它是一个s块元素。我们可以把钠归为碱金属,因为它是第一类金属。钠的电子构型为[Ne]3s1。因此,我们可以确定钠的价态是1。这意味着...
- 发布于 2020-09-18 03:08
- 阅读 ( 818 )
第一秒(first second)和第三过渡系列(third transition series)的区别
...d。 过渡金属是一种具有部分填充d轨道的化学元素。元素周期表中有三个过渡元素系列,我们称之为第一、第二和第三个跃迁系列。这些是元素周期表中三个不同时期的化学元素。因此,它们包含不同的最外层轨道。 目录 1. 概...
- 发布于 2020-10-15 14:56
- 阅读 ( 268 )
时期(periods)和组(groups)的区别
化学元素周期表中周期和组的关键区别在于周期是水平行,而组是垂直列。元素周期表中有7个主要周期和18个组。 元素周期表是一个大表,其中每一个已知的化学元素都放在一个考虑到原子结构的特定位置。因此,与任何网...
- 发布于 2020-10-22 03:56
- 阅读 ( 335 )
钙(calcium)和镁(magnesium)的区别
...钙的原子序数是20,而镁的原子序数是12。 钙和镁是元素周期表第2组中的两种化学元素。虽然它们在同一组中,但它们处于周期表的不同时期,因为钙比镁多了一个电子壳层。因此,它们具有不同的化学和物理性质。 目录 1. 概...
- 发布于 2020-10-22 08:34
- 阅读 ( 670 )
碱金属(alkali metals)和碱土金属(alkaline earth metals)的区别
...属都有两个外层电子。 由于碱金属和碱土金属都是元素周期表中的前两类,碱金属和碱土金属之间的区别是任何化学学生都感兴趣的课题。碱金属和碱土金属是“S-块”元素,因为这两类元素的最外层电子都在S-亚壳层中。 碱金...
- 发布于 2020-10-24 18:18
- 阅读 ( 862 )
溴(bromine)和溴化物(bromide)的区别
溴和溴的主要区别在于溴是溴的还原形式。 元素周期表中的化学元素除了惰性气体外都是不稳定的。因此,元素试图与其他元素反应以获得稀有气体电子构型以达到稳定性。同样,溴也必须得到一个电子,才能得到惰性气体...
- 发布于 2020-10-25 08:45
- 阅读 ( 434 )
原子(atoms)和元素(elements)的区别
...元素氧的所有原子的原子核中都有8个质子。 图02:元素周期表 此外,所有化学元素都列在元素周期表中。它有118种已知的化学元素。其中94种是自然发生的元素。另外24个是合成的。此外,还有80种元素至少有一种稳定同位素。...
- 发布于 2020-10-29 03:07
- 阅读 ( 240 )
氟(fluorine)和氟化物(fluoride)的区别
...物的关键区别在于氟是中性的,而氟是带负电的。 元素周期表中除惰性气体外的元素都是不稳定的。因此,元素试图与其他元素反应以获得稀有气体的电子构型并获得稳定性。氟是一种元素,它也必须得到一个电子,才能实现...
- 发布于 2020-11-03 01:57
- 阅读 ( 574 )
门捷列夫(mendeleev)和现代元素周期表(modern periodic table)的区别
门捷列夫周期表与现代周期表的关键区别在于,现代周期表的基础主要是元素的电子构型,我们称之为原子序数,而在门捷列夫周期表中,它是元素的原子质量。 让我们看看什么是门捷列夫周期表和什么是现代周期表,然后...
- 发布于 2020-11-03 03:51
- 阅读 ( 233 )
氢(hydrogen)和氦(helium)的区别
...于氢是双原子气体,而氦是单原子气体。 氢和氦是元素周期表中的前两个元素。它们都是气体,在宇宙中都有很高的丰度。它们是非常简单的元素,电子只填充到1s轨道。氢只有一个电子,它可以通过获得另一个电子来实现氦的...
- 发布于 2020-11-04 10:49
- 阅读 ( 682 )