溴和溴的主要区别在于溴是溴的还原形式。
元素周期表中的化学元素除了惰性气体外都是不稳定的。因此,元素试图与其他元素反应以获得稀有气体电子构型以达到稳定性。同样,溴也必须得到一个电子,才能得到惰性气体氪的电子构型。所有金属都与溴反应生成溴化物。由于一个电子的变化,溴和溴具有不同的物理化学性质。
目录
1. 概述和主要区别
2. 什么是溴
3. 什么是溴化物
4. 并列比较-溴与溴化物的表格形式
5. 摘要
什么是溴(bromine)?
溴是元素周期表中的一种化学元素,用Br表示。它是元素周期表第四周期的卤素(第17族)。溴的原子序数是35,因此它有35个质子和35个电子。其电子构型为[Ar]4s2 3d10 4p5。由于p子层应该有6个电子才能获得氪稀有气体的电子组态,溴具有吸引电子的能力。它具有很高的电负性,根据Pauling标度,约为2.96。
溴的原子量为79.904amu。在室温下,它以双原子分子(Br2)的形式存在。而且,这种双原子分子是一种红棕色的液体。溴的熔点为265.8K,沸点为332.0K。
溴的进一步性质
在所有的溴同位素中,Br-79和Br-81是最稳定的同位素。此外,这种化学元素微溶于水,但很容易溶于有机溶剂,如氯仿。此外,它有7,5,4,3,1,-1氧化态。
溴的化学反应性介于氯和碘之间。溴的活性不如氯,但比碘更活泼。溴通过吸收一个电子产生溴离子。因此,溴很容易参与离子化合物的形成。实际上,在自然界中,溴是以溴盐的形式存在的,而不是Br2。

图01:溴
溴可以氧化元素周期表中位于溴之下的元素的阴离子。然而,它不能氧化氯化物产生氯。此外,用氯气处理富溴卤水可以生产溴化丁苯。或者用硫酸处理HBr形成溴气。溴在工业和化学实验室中非常有用。溴化物是重要的汽油添加剂,杀虫剂和消毒剂在水净化。
什么是溴化物(bromide)?
溴是溴从另一个正电荷元素中吸收电子时形成的阴离子。我们可以用符号Br-。它是带-1电荷的一价离子。因此,它有36个电子和35个质子。

溴化物的电子构型为[Ar]4s2 3d10 4p6。它存在于溴化钠、溴化钙和HBr等离子化合物中。它也自然存在于水源中。
溴(bromine)和溴化物(bromide)的区别
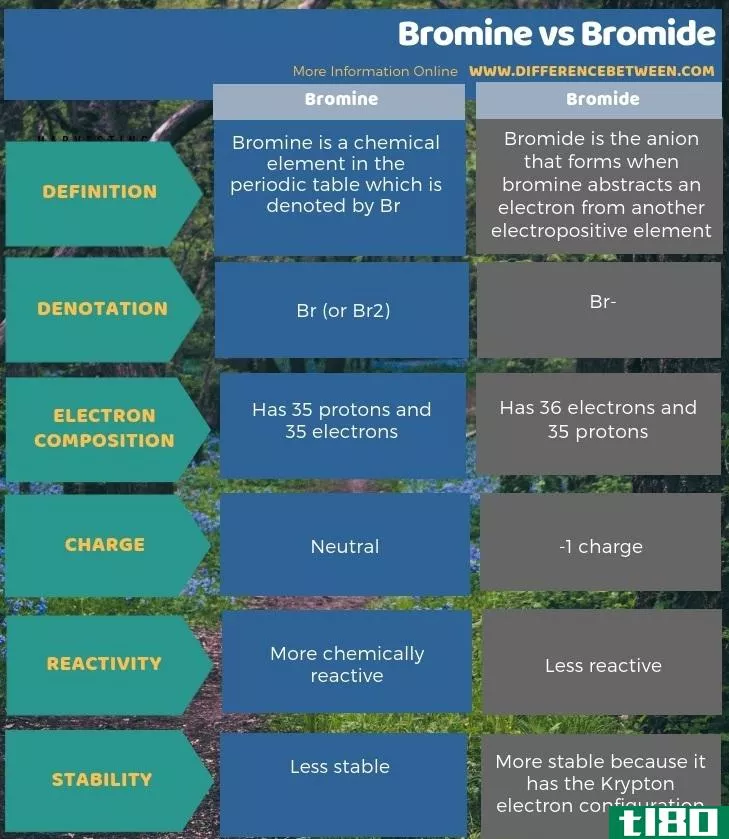
溴是周期表中的一种化学元素,用Br表示,而溴是溴从另一种正电荷元素中吸收电子时形成的阴离子。此外,溴和溴的关键区别在于溴是溴的还原形式。此外,溴有36个电子,而溴只有35个电子,但两者都有35个质子。因此,溴的电荷是-1,而溴是中性的。
此外,溴比溴更具化学反应性。另外,溴和溴化物之间的另一个区别是,溴化物已经实现了氪电子构型,因此比溴原子更稳定。
总结 - 溴(bromine) vs. 溴化物(bromide)
溴是元素周期表中的一种化学元素,用Br表示。同时,溴是溴从另一个正电荷元素中吸收电子时形成的阴离子。此外,溴和溴之间的关键区别在于溴是溴的还原形式。