原子和元素之间的关键区别在于,原子是构成所有物质的最小单位,而元素是包含具有相同化学和物理性质的原子的一种原子。
我们所看到和感受到的一切都叫做物质。这种物质,包括人和动物,还有植物和非生物,如水和岩石,是由非常小的微粒组成的,我们认为这些微粒是构成物质的基石。化学元素描述一种原子。
目录
1. 主要区别和主要概述
2. 什么是原子
3. 什么是元素
4. 并列比较——原子与元素的表格形式
5. 摘要
什么是原子(atoms)?
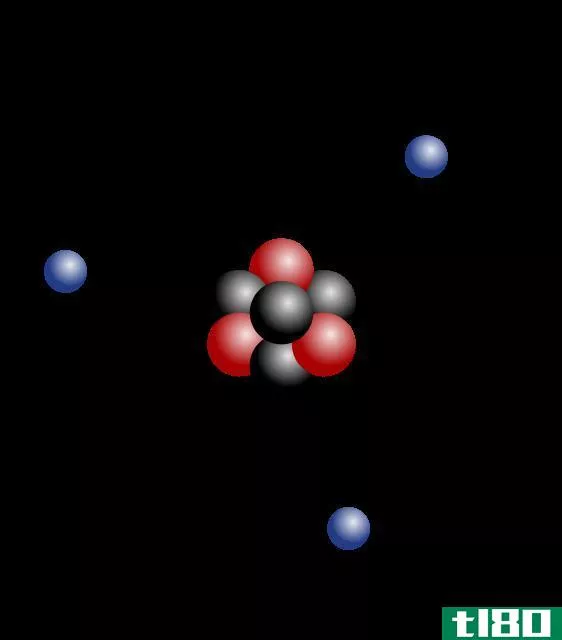
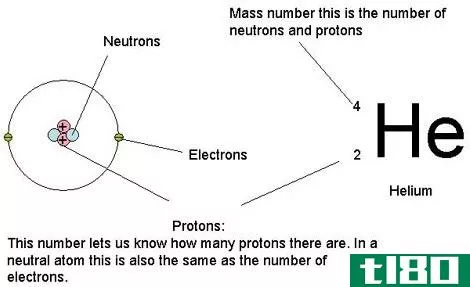
原子是构成所有物质的最小重复单位。一个原子非常小,它的大小大约是100μm。原子的质量以含有质子和中子的原子核为中心。另外,在这个原子核周围有一个电子云。因此,质子、中子和电子都是原子的亚原子粒子。
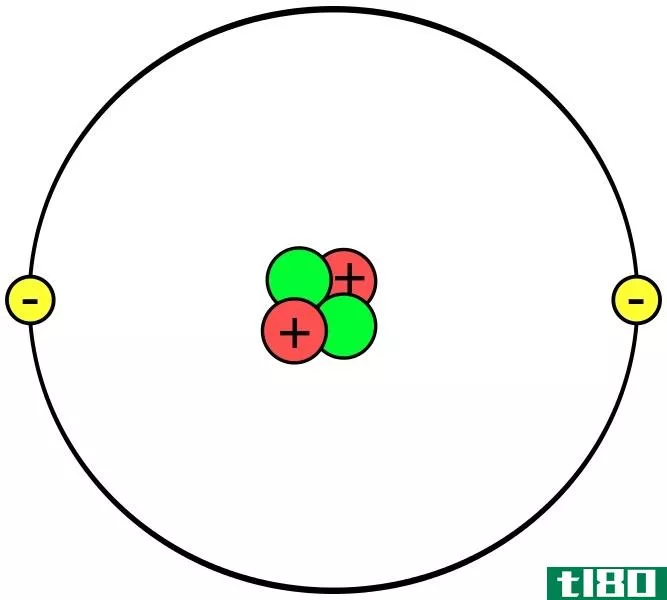
图01:氦原子
通常,原子核中的质子数等于电子数和中子数。然而,有些原子的质子数相同,但中子数不同。我们把它们命名为一种化学元素的同位素(因为如果这些原子拥有相同数量的质子,则表明这些原子属于同一化学元素)。此外,质子和中子的质量之和决定了原子的质量(与质子和中子相比,电子的质量可以忽略不计)。
什么是元素(elements)?
化学元素是一种原子。因此,原子具有其特定化学元素的化学和物理性质。因此,同一化学元素的原子具有相同的化学和物理性质。特别是,这些原子的原子核中有相同数量的质子。但是,中子的数量可以是相等的,也可以是不同的。如果一个原子与另一个原子的中子数不同,我们把它们命名为化学元素的同位素。
例如原子核里有8个质子。因此,一个原子应该有8个质子,如果我们把它命名为氧。然后,化学元素氧的所有原子的原子核中都有8个质子。
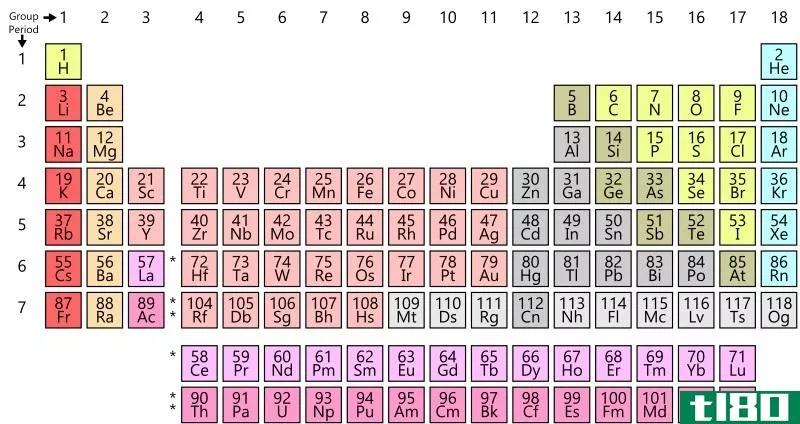
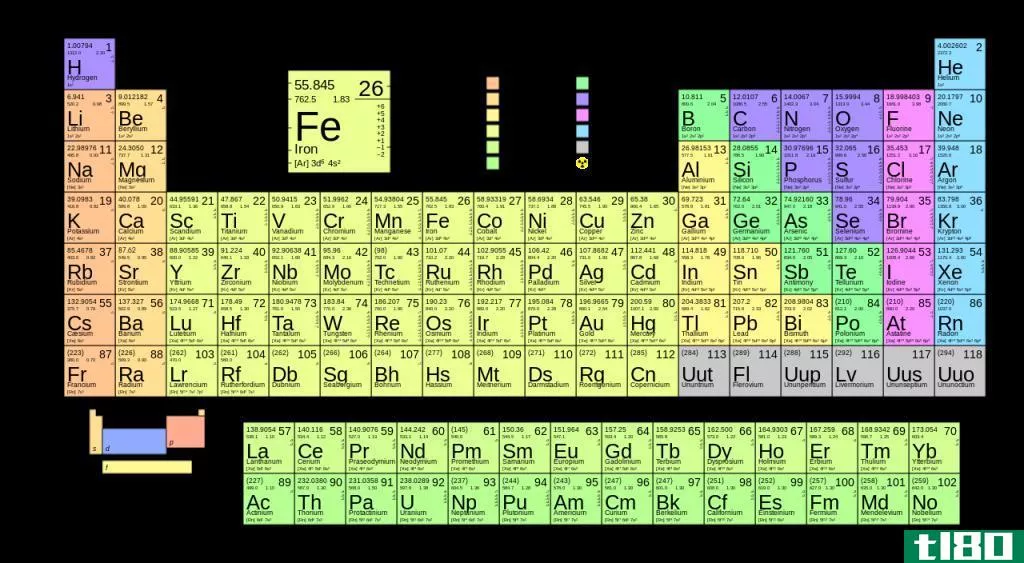
图02:元素周期表
此外,所有化学元素都列在元素周期表中。它有118种已知的化学元素。其中94种是自然发生的元素。另外24个是合成的。此外,还有80种元素至少有一种稳定同位素。同样,元素周期表按原子序数(原子核中的质子数)的升序排列化学元素。这些元素的化学和物理性质有周期性的变化趋势。
原子(atoms)和元素(elements)的区别
所有物质都含有原子。此外,原子核中质子数相同的原子属于同一化学种类;化学元素。因此,原子和元素之间的关键区别在于,原子是构成所有物质的最小单位,而元素是包含具有相同化学和物理性质的原子的一种原子。此外,单个原子的原子核中的质子和中子数量可以相等或不同。但同一化学元素的原子有相等数量的质子和中子。但是,如果数字不同,我们就把它们命名为该化学元素的同位素。
下面的信息图以表格形式总结了原子和元素之间的区别。

总结 - 原子(atoms) vs. 元素(elements)
所有的物质都是由叫做原子的微粒组成的。元素是由单一原子组成的化学物质。因此,一个元素的每一个原子都保留了该元素的属性,并且是该元素具有相同属性的最小单元。因此,原子和元素之间的关键区别在于原子是构成所有物质的最小单位,而元素是包含具有相同化学和物理性质的原子的一种原子。
引用
1“化学元素”,维基百科,维基媒体基金会,2018年10月11日。可在这里查阅2。“原子”,维基百科,维基媒体基金会,2018年10月10日。此处提供
2“原子”,维基百科,维基媒体基金会,2018年10月10日。