原子量和原子质量之间的关键区别在于,原子量是元素相对于所有同位素及其相对丰度的平均重量,但是原子质量是单个原子的质量。
大多数人交替使用原子质量和原子量这两个术语。然而,它们的含义不同,如果将这两个术语视为一个术语,则会导致散料计算中的重大错误。
目录
1. 概述和主要区别
2. 原子量是多少
3. 原子质量是多少
4. 并列比较-以表格形式显示原子量与原子质量
5. 摘要
什么是原子量(atomic weight)?
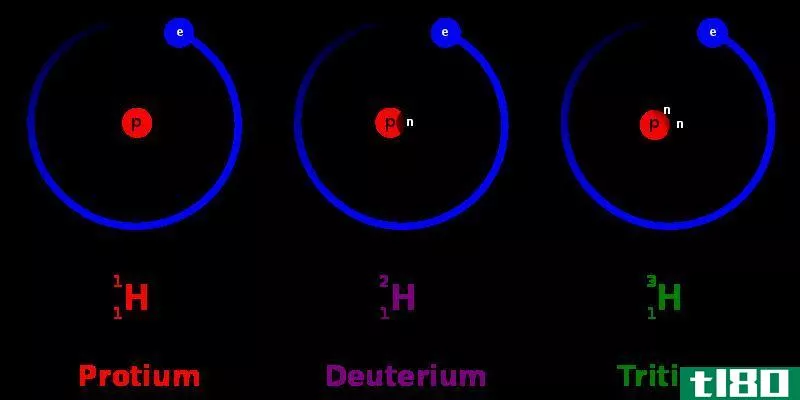
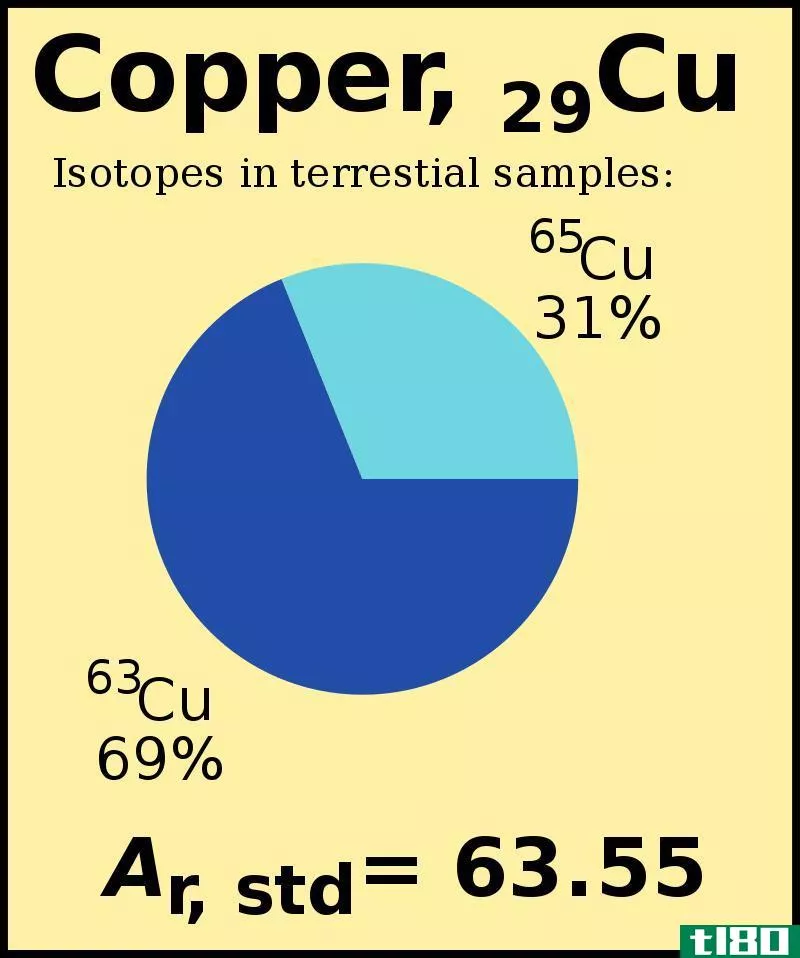
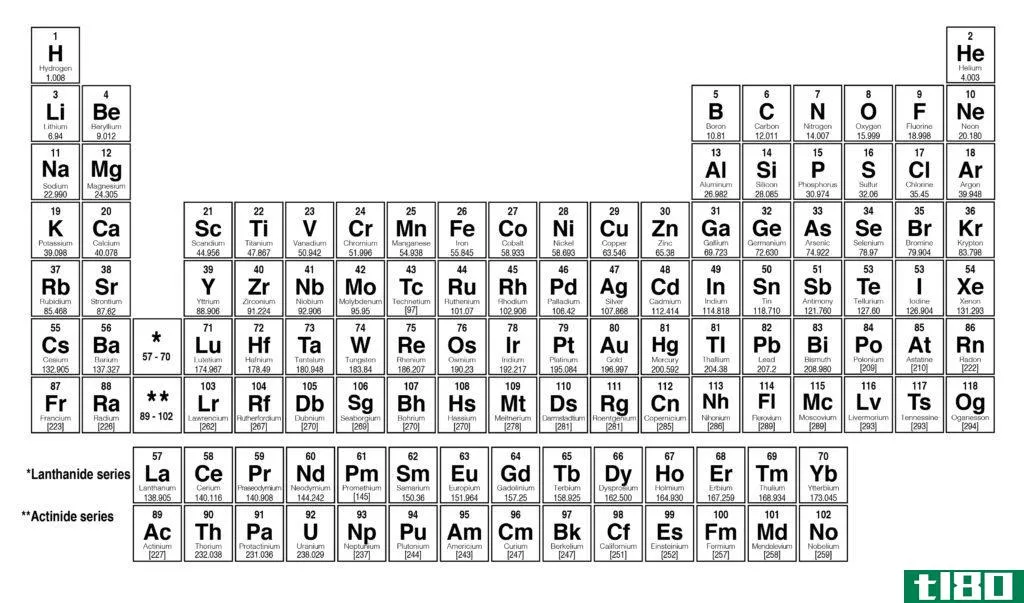
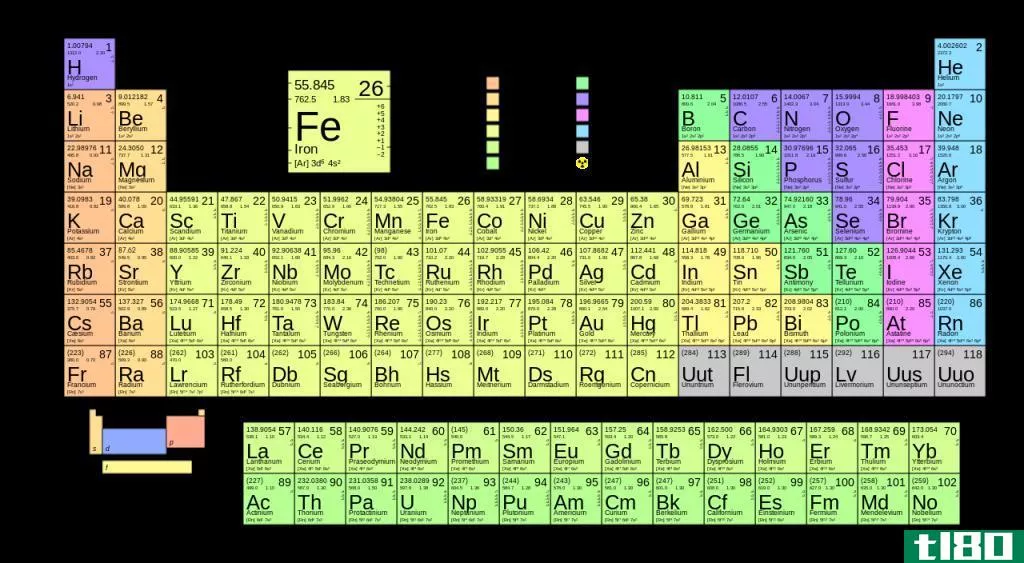
原子量是一种元素相对于其所有同位素及其相对丰度的平均重量。大多数时候,化学元素有同位素;同位素是同一化学元素的不同形式。同位素在原子核中有相同数量的质子(这使得它们属于同一化学元素)和不同数量的中子。自然界中有不同比例的不同同位素。当我们得到一个化学元素的原子量时,我们需要考虑所有同位素的原子质量及其百分比。在那里,我们可以用每个同位素的原子质量来计算平均质量,从而得到原子量。我们在周期表中看到的原子量就是根据这种现象计算出来的。
我们可以使用以下两个步骤进行计算;
- 首先,将百分数除以100,将其转换为十进制值。
- 接下来,从这些十进制值中相应地乘以每个同位素的原子质量。
- 最后,将答案相加得到最终答案。
视频1:计算原子量
例如:假设我们有98%的C-12同位素和2%的C-13同位素。让我们用这些同位素的原子质量来计算碳的原子量。
- 转换为十进制值:
- C-12百分比的十进制值为0.98(用98除以100得到)。
- 12 x 0.98=11.76
最终,我们可以得到化学元素碳的原子量为12.02amu(原子质量单位)。此外,我们可以将这个术语命名为“相对原子质量”,因为它是同位素实际原子质量的平均值。
什么是原子质量(atomic mass)?
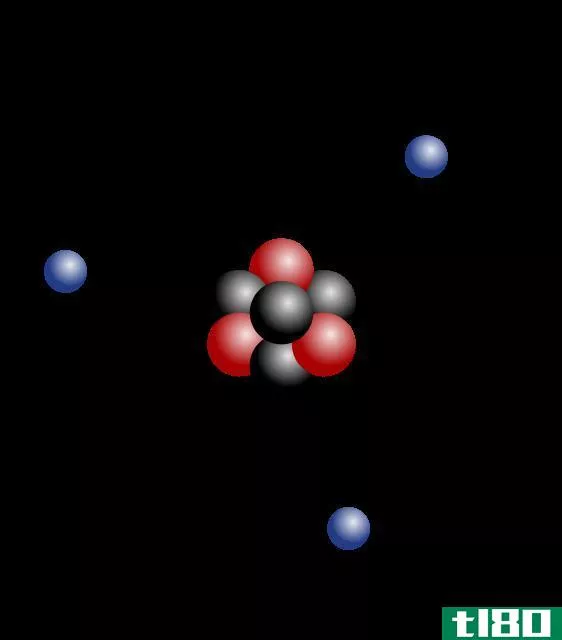
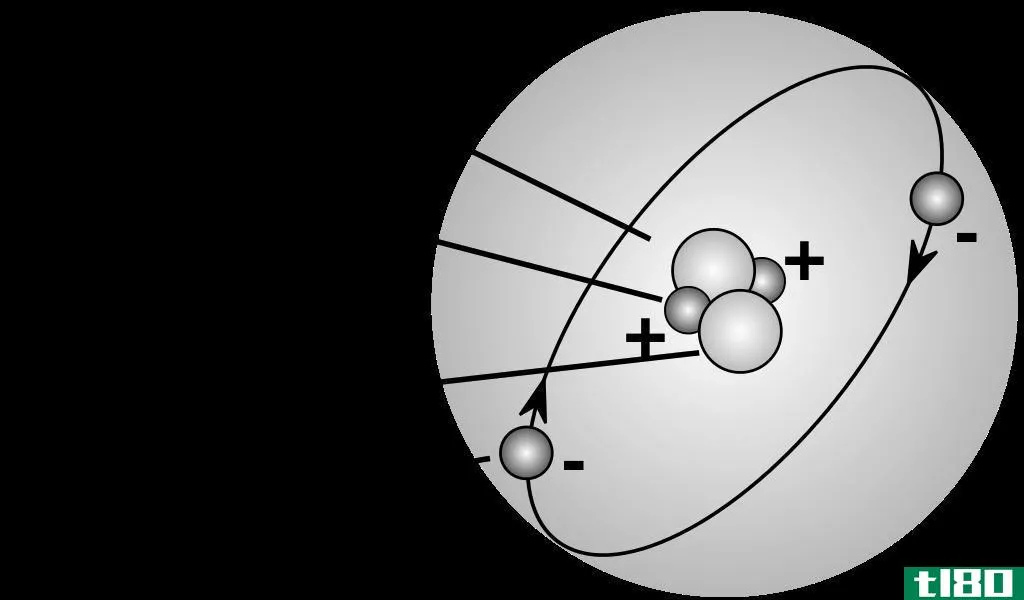
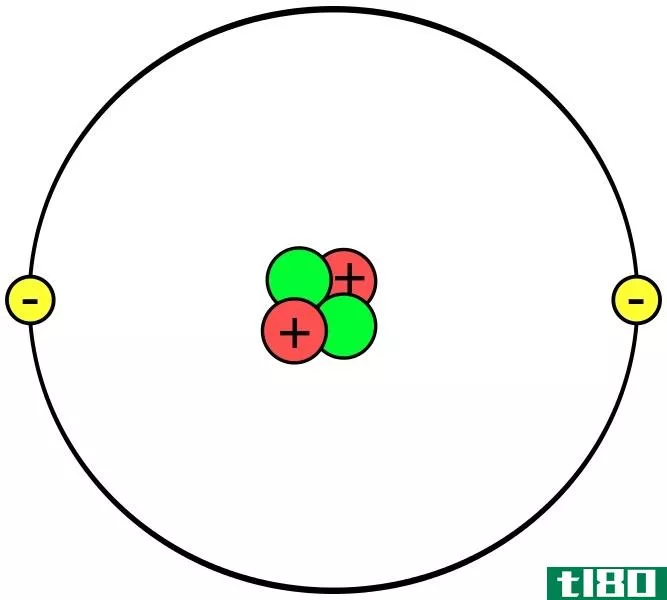
原子主要含有质子、中子和电子。原子质量就是原子的质量。换句话说,它是单个原子中所有中子、质子和电子的质量的集合,特别是当原子不运动时(静止质量)。我们只取剩余质量,因为根据物理学的基本原理,当原子以非常高的速度运动时,质量会增加。然而,与质子和中子的质量相比,电子的质量相当小。因此,我们可以说电子对原子质量的贡献较小。因此,在计算原子质量时,我们可以忽略电子的质量。最重要的是,不同的同位素有不同的原子质量,尽管它们属于同一化学元素,因为它们有不同数量的中子。
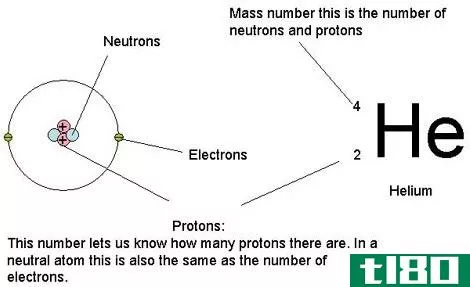
图01:我们可以利用原子的质子、中子和电子的质量来计算原子质量
此外,原子的质量非常小,所以我们不能用克或公斤这样的正常质量单位来表示它们。为了我们的目的,我们使用另一种叫做原子质量单位(amu)的单位来测量原子质量。同样,1个原子质量单位是C-12同位素质量的十二分之一。当我们把一个原子的质量从碳-12同位素质量的十二分之一的质量中除掉,我们就可以得到它的相对质量。然而,在一般情况下,当我们说一个元素的相对原子质量时,我们指的是它们的原子量(因为我们计算时考虑了所有的同位素)。
原子量(atomic weight)和原子质量(atomic mass)的区别
大多数时候,我们用原子量和原子质量这两个词是一样的。然而,这两个术语之间的区别主要取决于定义。因此,根据定义,原子量和原子质量之间的关键区别在于,原子量是元素相对于所有同位素及其相对丰度的平均重量,而原子质量是单个原子的质量。
此外,我们还可以通过考虑每一个值的计算方式来确定原子量和原子质量之间的另一个重要区别;我们应该用自然界中一个化学元素的所有同位素的丰度百分比来计算原子量,而我们可以简单地加上质子的质量来计算原子质量,原子的中子和电子。

总结 - 原子量(atomic weight) vs. 原子质量(atomic mass)
原子量和原子质量是我们在化学计算中经常使用的两个重要术语。原子量和原子质量之间的关键区别在于,原子量是元素相对于所有同位素及其相对丰度的平均重量,而原子质量是单个原子的质量。
引用
1威奇斯、爱德华和H.斯特芬·佩瑟。“原子量”,不列颠百科全书,不列颠百科全书,2017年12月15日。这里有2个。Helmenstine,Anne Marie博士,“如何计算原子质量”,《ThoughtCo》,2018年4月1日。可在此处查阅
2Helmenstine,Anne Marie博士,“如何计算原子质量”,ThoughtCo,2018年4月1日