原子质量和平均原子质量的关键区别在于,原子质量是一个原子的质量,而平均原子质量是通过考虑某一特定化学元素的同位素计算出的原子质量。
我们经常交替使用原子质量和平均原子质量这两个术语,但它们是两个不同的术语。
目录
1. 概述和主要区别
2. 原子质量是多少
3. 平均原子质量是多少
4. 并列比较-原子质量与平均原子质量的表格形式
5. 摘要
什么是原子质量(atomic mass)?
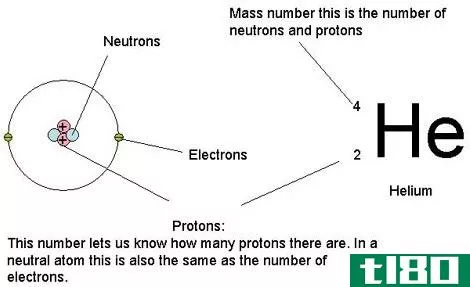
原子质量是原子核中存在的核子的总质量。核子不是p7p就是中子。因此,原子质量是原子核中质子和中子的总质量。虽然电子也存在于原子中,但电子的质量并没有用于计算,因为电子非常小,与质子和中子相比质量可以忽略不计。
与相对原子质量不同,这里我们计算每个原子的质量而不计算任何平均值。因此,我们得到不同同位素的原子质量值。这是因为同一元素的同位素中存在的核子数目是不同的。
我们来举个例子:
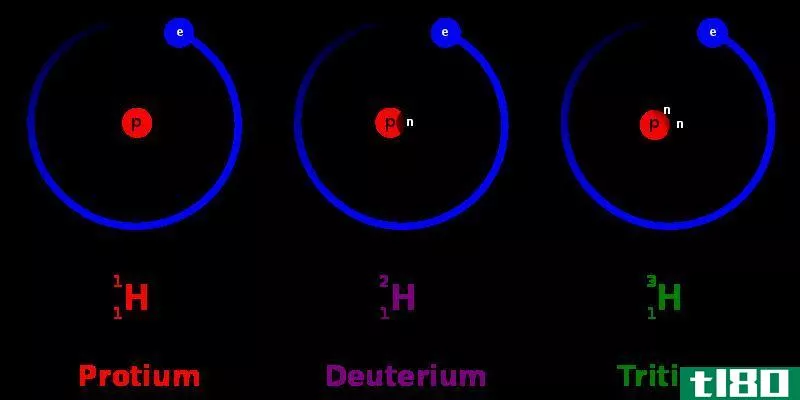
氢的原子质量=2
因此,氢-2(氘)同位素的原子质量计算如下。
原子核中的质子数=1原子核中的中子数=1因此,氢的原子质量=(1 amu+1 amu)=2 amu
这里,t原子质量由单位amu(原子质量单位)给出。一个质子或中子的质量为1 amu。
什么是平均原子质量(average atomic mass)?
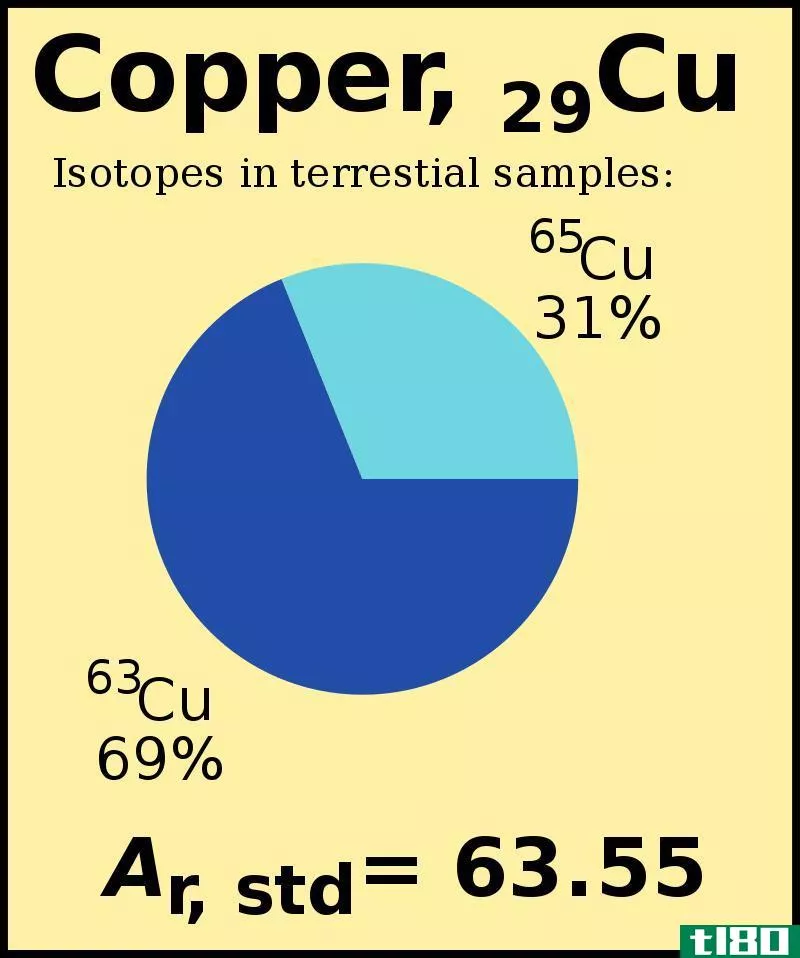
平均原子质量是通过考虑某一化学元素的同位素计算出的某一化学元素的原子质量。在这种情况下,质量值取决于一种化学元素的自然丰度。
计算平均原子质量有两个步骤。
- 从自然丰度(以丰度为百分比)中分别乘以每种同位素的原子质量。
- 把得到的值相加,得到平均原子质量。
我们来举个例子:
碳有两种同位素,即碳-12和碳-13。其丰度分别为98%和2。然后我们可以通过计算来确定碳的平均原子质量。这里,我们要用丰度值乘以每个同位素的原子质量。那么,我们需要把丰度作为两位小数,而不是百分比。接下来,我们可以将获得的值相加。
碳-12:0.98*12=11.76
碳-13:0.02*13=0.26
则碳的平均原子质量为=11.76+0.26=12.02g/mol。
原子质量(atomic mass)和平均原子质量(average atomic mass)的区别
虽然“原子质量”和“平均原子质量”听起来很相似,但它们是两个不同的术语。原子质量和平均原子质量的关键区别在于,原子质量是一个原子的质量,而平均原子质量是通过考虑某一特定化学元素的同位素计算出的原子质量。原子质量是指单个原子的质量,而平均原子质量是指化学元素的质量。
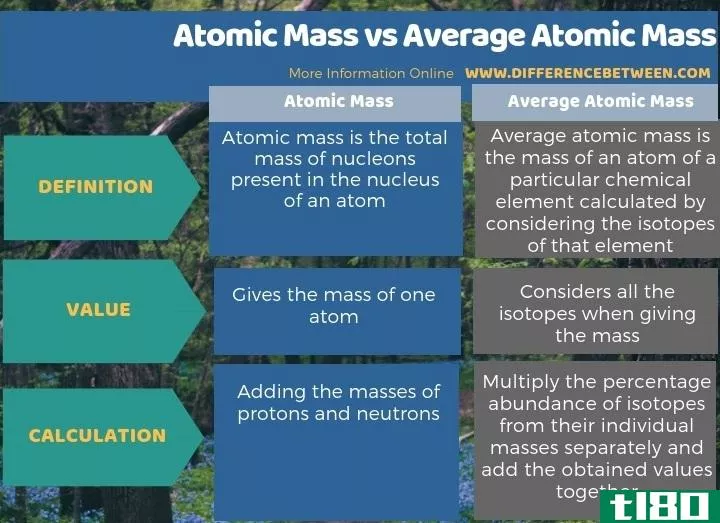
总结 - 原子质量(atomic mass) vs. 平均原子质量(average atomic mass)
原子质量是指单个原子的质量,而平均原子质量是指某一特定化学元素原子的平均质量。因此,原子质量和平均原子质量的关键区别在于,原子质量是原子的质量,而平均原子质量是通过考虑某一化学元素的同位素计算出的某一化学元素的原子质量。
引用
赫尔曼斯汀,安妮·玛丽。“如何计算原子质量”,ThoughtCo,2019年8月21日,可查阅给你。赫尔曼斯汀,安妮·玛丽。“如何计算原子质量”,ThoughtCo,2019年8月21日,可在这里查阅。
赫尔曼斯汀,安妮·玛丽。“如何计算原子质量”,ThoughtCo,2019年8月21日,