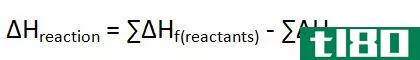为什么o2的标准生成焓等于零?
要理解O2的标准生成焓等于零,您需要理解标准生成焓的定义。这是在1大气压和298K温度的标准状态条件下,当一摩尔标准状态的物质由其元素形成时的焓变。氧气的组成元素已经处于标准状态,所以这里没有任何变化。标准状态下的氧(元素)为O2。


其他气体元素,如氢和氮,以及固体元素,如石墨形式的碳,也是如此。处于标准状态的元素的标准生成焓为零。
- 发表于 2021-10-14 06:43
- 阅读 ( 694 )
- 分类:数学
你可能感兴趣的文章
生成热(heat of formation)和反应热(heat of reaction)的区别
生成热和反应热的关键区别在于,生成热是在标准条件下形成一摩尔物质过程中的焓变化,而反应热是在恒压下发生的化学反应过程中焓的变化。 生成热和反应热是化学反应的重要焓值。我们将这些术语定义为标准条件,即...
- 发布于 2020-10-18 06:22
- 阅读 ( 535 )
溶剂化能(solvation energy)和晶格能(lattice energy)的区别
...iF)形成的Born-Haber循环 Born-Haber循环可由以下方程给出。 生成热=原子化热+离解能+电离能之和+电子亲和力之和+晶格能 然后通过重新排列这个方程,可以得到化合物的晶格能,如下所示。 晶格能=生成热–{原子化热+离解能+电离...
- 发布于 2020-10-20 03:46
- 阅读 ( 800 )
焓(enthalpy)和熵(entropy)的区别
...,焓的变化取决于反应物的相。例如,当氧气和氢气反应生成水蒸气时,焓变为-483.7kj。当相同反应物反应生成液态水时,焓变为-571.5kj。 2H2(g)+O2(g)→2H2O(g);∆H=-483.7千焦 2H2(g)+O2(g)→2H2O(l);∆H=-571.7 kJ 什么是...
- 发布于 2020-11-04 20:59
- 阅读 ( 1884 )
焓(enthalpy)和热(heat)的区别
...,焓的变化取决于反应物的相。例如,当氧气和氢气反应生成水蒸气时,焓变为-483.7kj。但是,当相同反应物反应生成液态水时,焓变为-571.5kj。 什么是热(heat)? 一个系统做功的能力就是这个系统的能量。我们可以在系统上做功...
- 发布于 2020-11-05 19:40
- 阅读 ( 897 )
原子化焓(enthalpy of atomisation)和键裂解(bond dissociation)的区别
...何化学键。因此,原子化焓总是一个正值。这种焓变化的标准焓值是“标准原子化焓”。本文中考虑的标准条件为268.15 K温度和1 bar压力。 例如,水分子的原子化焓是指分离水分子中两个氢原子和氧原子所需的能量。换句话说,...
- 发布于 2021-03-04 20:07
- 阅读 ( 961 )
键能(bond energy)和键离解能焓(bond dissociation energy enthalpy)的区别
...对共享)被均裂(分解为相等的碎片)裂解产生碎片时的标准焓变;通常是激进的物种。因此,键能和键离解能之间的主要区别是键能是平均值,而键离解能是特定键的特定值。 什么是键能和键离解能(焓)(bond energy and bond d...
- 发布于 2021-06-26 10:13
- 阅读 ( 482 )
熵(entropy)和焓(enthalpy)的区别
...化是产物焓和反应物焓之差。焓的单位是Jmol-1。 只有在标准条件下发生反应时,反应的热变化才称为焓。即压力为1巴,指定温度通常为25℃°C.存在许多类型的反应焓。i、 反应焓、生成焓、燃烧焓、中和焓、溶解焓等。 Josiah Wil...
- 发布于 2021-06-27 08:16
- 阅读 ( 1278 )
焓(enthalpy)和内能(internal energy)的区别
...示,内能的变化用符号U表示∆美国。 恒压下的内能变化等于系统的焓变化。内能的变化有两种方式。一个是由于热传递-系统可以吸收外部热量或释放热量到周围。这两种方式都会导致系统的内能发生变化。另一种方法是工作。...
- 发布于 2021-06-29 08:17
- 阅读 ( 944 )
简历(cv)和内容提供商(cp)的区别
...体积的乘积之和。这是因为一个系统吸收或释放的总能量等于系统已经拥有的能量(内能)和系统中发生的变化(PV)。温度的变化将引起系统焓的变化。因此,可以如下给出。 哪里, CP是恒压下的比热 dH是焓变 dT是温度的变...
- 发布于 2021-06-29 08:29
- 阅读 ( 850 )
吸热的(endothermic)和放热反应(exothermic reactions)的区别
...环境中的体积和压力所需的能量之和。一开始,系统的焓等于反应物的焓之和。在吸热反应结束时,由于能量的吸收,产物的焓或能量较高。这可以解释如下。 A+B组合→ C+D公司 ΔH={HC+HD}–{HA+HB} ΔH=(H产品)–(H反应物)=正值 ...
- 发布于 2021-06-29 08:53
- 阅读 ( 1320 )