为什么水被认为是极性分子?
为什么水被认为是极性分子?
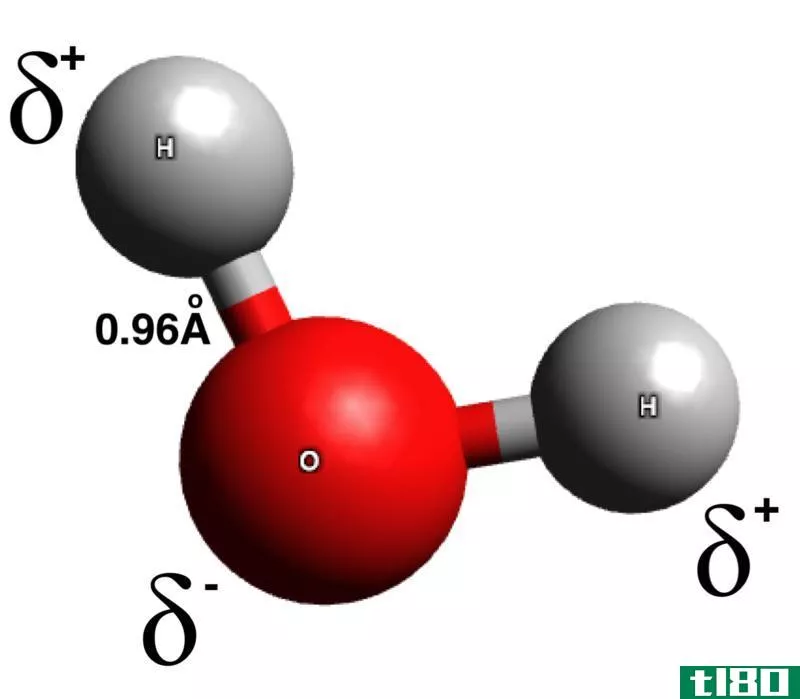
水分子由于其形状而具有极性。水有两个带正电荷的氢原子和一个带负电荷的氧原子共价键合在一个水分子中。氢原子中每个原子有一个电子,氧原子有4个电子对。氧的两个电子对与氢的两个电子形成共价键。剩下的两对孤电子实际上是氧电负性的原因。由于氧原子上有两对孤对电子,水分子的形状呈角状,键角为104.5度。水的键角将略小于四面体角。因此,水的分子结构呈棱角状。
当氧倾向于将共价键中的共享电子拉向其一侧时,水的极性就得到了。虽然在共价键中,电子在原子之间平均分配,但在水分子的情况下,电子被强烈吸引到氧上。氧对电子的这种引力使电荷分布不对称。分子结构的不对称性提供了部分负电荷和部分正电荷。水的这种极性使其他物质很容易溶解到水中。
水的极性通过一种称为内聚力的力帮助其分子保持彼此接近。极性有助于水分子以另一种称为粘附力的力附着到其他分子上。由于这种粘附力,利用毛细管作用,水往往会在管中上升。水分子所具有的内聚和粘附特性有助于它在木质部导管中从根移动到叶。水的极性对动物来说也很重要,因为它们在许多方面依赖植物。
水的极性有助于它充当通用溶剂,而由于一个分子的氢和另一个分子的氧的极性性质,水分子之间存在氢键。
- 发表于 2021-11-18 08:55
- 阅读 ( 435 )
- 分类:科学
你可能感兴趣的文章
极地的(polar)和偶极分子(dipolar molecules)的区别
极性分子和偶极分子的关键区别在于,极性分子有两个相反的两端,带着相反的电荷,而极性分子有两个极性。 一般来说,我们可以交替使用极性和偶极两个术语,因为这两个术语都描述了具有两个相反末端的单个分子。这...
- 发布于 2020-09-24 05:10
- 阅读 ( 538 )
四面体(tetrahedral)和三角金字塔(trigonal pyramid)的区别
...四面体的角上时,才能形成四面体。也有四面体分子也被认为是手性的情况。手征面用来描述一个没有内对称面的物体。 在分子几何学中,成键原子和非成键原子可以极大地决定分子的形状。成键原子对分子的形状没有任何普...
- 发布于 2021-06-23 16:01
- 阅读 ( 318 )
极地的(polar)和非极性分子(nonpolar molecules)的区别
主要差异极性(main difference polar) vs. 非极性分子(nonpolar molecules) 不同或相同元素的原子聚在一起形成分子。由两个原子共用一对电子形成的键称为“共价键”。不同的原子对电子有不同程度的吸引力。它们把电子拉向它们...
- 发布于 2021-06-28 12:20
- 阅读 ( 1812 )
如何极性分子和非极性分子相互作用(polar and nonpolar molecules interact with each other)
...,从而产生了一个零的净偶极子。因此,二氧化碳分子被认为是非极性分子。 非极性化合物的实例主要是双原子气体分子,例如N2、Cl2和O2。烃类液体在大多数情况下也是非极性的。甲苯、汽油、戊烷和己烷就是一些例子。 极性...
- 发布于 2021-06-28 12:27
- 阅读 ( 895 )
如何分子形状影响极性(molecular shape affect polarity)
...loride-3D-balls” (Public Domain) via Comm*** Wikimedia 参考文献: 为什么四氯化碳分子是非极性的,而其中的键却是极性的。N.p.,N.d.网站。2017年2月13日。 “氨是极性的吗?”Reference.com。N.p.,N.d.网站。2017年2月13日。 奥法德,查尔斯E...
- 发布于 2021-06-28 12:34
- 阅读 ( 290 )
疏水的(hydrophobic)和亲水分子(hydrophilic molecules)的区别
...能与水混合的物质称为疏水物质。这主要是由于水分子的极性。非极性化合物不能溶解在极性溶剂中。在这里,我们应该考虑“似溶似”的事实。极性化合物能溶于极性溶剂。非极性化合物溶于非极性溶剂。因此,亲水性物质应...
- 发布于 2021-06-29 14:28
- 阅读 ( 297 )
共价分子(covalent molecular)和共价网络(covalent network)的区别
...。共价网络化合物中没有单独的分子。因此,整个物质被认为是一个大分子。 由于共价网络结构高度稳定,这些化合物具有较高的熔点和沸点。它们不溶于水。由于整个网络结构中原子间存在强共价键,硬度非常高。与共价分...
- 发布于 2021-06-29 16:21
- 阅读 ( 575 )
键的极性(bond polarity)和分子极性(molecular polarity)的区别
主差键极性(main difference bond polarity) vs. 分子极性(molecular polarity) 在化学中,极性是指导致分子产生偶极矩的电荷分离。在这里,部分正电荷和部分负电荷在键或分子中分开。这主要是因为原子电负性值的不同。原子的电负性是...
- 发布于 2021-06-29 20:34
- 阅读 ( 466 )
极地的(polar)和非极性电介质(nonpolar dielectrics)的区别
主要差异极性(main difference polar) vs. 非极性电介质(nonpolar dielectrics) 电介质是电绝缘体。它们不是导电材料,因为它们没有自由电子导电。电介质可以通过施加电场而极化。电介质有两种类型:极性电介质和非极性电介质。极性...
- 发布于 2021-06-29 22:02
- 阅读 ( 467 )
极地的(polar)和非极性(non-polar)的区别
...例如O2(氧)、H2(二氢)和O3(臭氧)结合时。这些键被认为是非常强的键,需要大量的能量才能切断。然而,情况并非总是如此。碳(X=2.55)和氢(X=2.2)可以在大量的有机化合物中结合在一起,由于电负性的微小差异(0.35)...
- 发布于 2021-07-07 08:12
- 阅读 ( 387 )