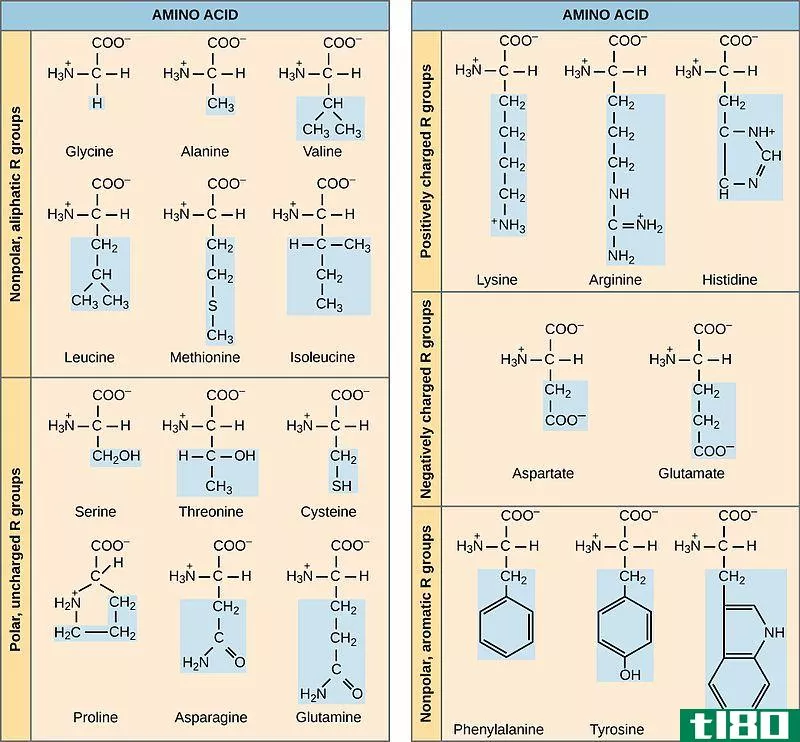
极性和非极性分子示例
两类主要的分子是极性分子和非极性分子。有些分子显然是极性或非极性的,而另一些分子则介于两类分子之间。下面我们来看一下极性和非极性的含义,如何预测一个分子是一个还是另一个,以及代表性化合物的例子。

关键要点:极性和非极性
- 在化学中,极性是指原子、化学基团或分子周围电荷的分布。
- 当键合原子之间存在电负性差异时,就会产生极性分子。
- 非极性分子发生在双原子分子的原子之间相等地共享电子,或者大分子中的极性键相互抵消时。
极性分子
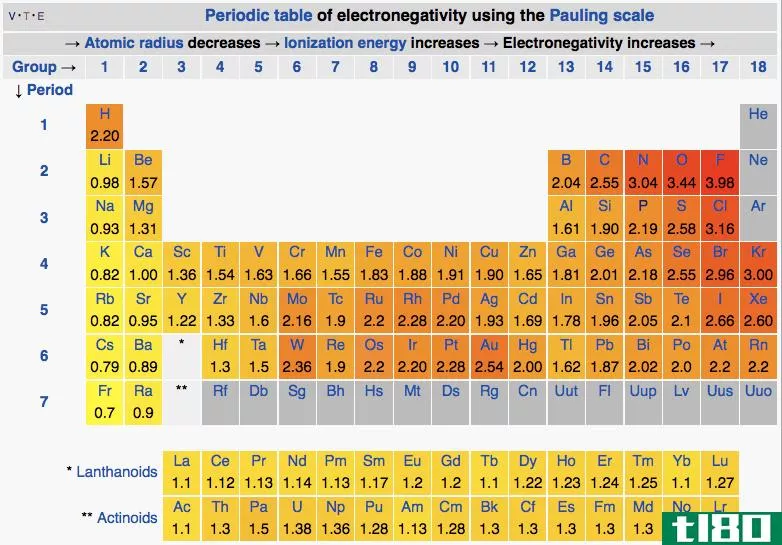
当两个原子在共价键中不相等地共享电子时,就会产生极性分子。形成偶极子,分子的一部分带有轻微的正电荷,另一部分带有轻微的负电荷。当每个原子的电负性值存在差异时,就会发生这种情况。极端差异形成离子键,而较小差异形成极性共价键。幸运的是,你们可以在一张表上查到电负性来预测原子是否有可能形成极性共价键。如果两个原子之间的电负性差在0.5和2.0之间,则两个原子形成极性共价键。如果原子间的电负性差大于2.0,则键是离子键。离子化合物是极性极强的分子。
极性分子的例子包括:
- 水-H2O
- 氨氮
- 二氧化硫-二氧化硫
- 硫化氢-硫化氢
- 乙醇-C2H6O
注:离子化合物,如氯化钠(NaCl),是极性的。然而,大多数时候,当人们谈论“极性分子”时,他们指的是“极性共价分子”,而不是所有类型的具有极性的化合物!当提到化合物的极性时,最好避免混淆,称之为非极性、极性共价和离子。
非极性分子
当分子在共价键中平均共享电子时,分子上没有净电荷。在非极性共价键中,电子均匀分布。你可以预测当原子具有相同或相似的电负性时,会形成非极性分子。一般来说,如果两个原子之间的电负性差小于0.5,则该键被认为是非极性的,即使唯一真正非极性的分子是由相同原子形成的分子。
当共享极性键的原子排列成电荷相互抵消时,也会形成非极性分子。
非极性分子的例子包括:
- 任何一种稀有气体:氦、氖、氩、氪、氙(这些是原子,从技术上讲不是分子。)
- 任何一种同核双原子元素:H2、N2、O2、Cl2(它们是真正的非极性分子)
- 二氧化碳-二氧化碳
- 苯-C6H6
- 四氯化碳-四氯化碳
- 甲烷-CH4
- 乙烯-C2H4
- 碳氢化合物液体,如汽油和甲苯
- 大多数有机分子
极性和混合溶液
如果你知道分子的极性,你就可以预测它们是否会混合在一起形成化学溶液。一般的规则是“like溶解like”,这意味着极性分子将溶解到其他极性液体中,而非极性分子将溶解到非极性液体中。这就是油和水不混合的原因:油是非极性的,而水是极性的。
知道哪些化合物介于极性和非极性之间是很有帮助的,因为你可以用它们作为一种中间体,将一种化学物质溶解成一种它不会与之混合的物质。例如,如果你想在有机溶剂中混合离子化合物或极性化合物,你可以将其溶解在乙醇中(极性,但不能大量溶解)。然后,你可以将乙醇溶液溶解成有机溶剂,如二甲苯。
来源
- 英戈尔德,C.K。;Ingold,E.H.(1926年)。“碳链交替效应的性质。第五部分:芳香取代的讨论,特别是极性和非极性离解的各自作用;以及氧和氮的相对定向效率的进一步研究”。J.化学。Soc:1310–1328。内政部:10.1039/jr9262901310
- 鲍林,L.(1960年)。化学键的性质(第3版)。牛津大学出版社。第98-100页。ISBN 080140332。
- 齐埃·莫亚耶德、玛亚姆;爱德华·古德曼;威廉姆斯,彼得(2000年11月)。“极性液体流的电偏转:一个被误解的演示”。化学教育杂志。77 (11): 1520. 内政部:10.1021/ed077p1520
- 发表于 2021-09-20 11:44
- 阅读 ( 223 )
- 分类:化学
你可能感兴趣的文章
极地的(polar)和非极性氨基酸(nonpolar amino acids)的区别
关键区别-极性氨基酸与非极性氨基酸 氨基酸按极性可分为极性氨基酸和非极性氨基酸两大类。极性氨基酸与非极性氨基酸的主要区别在于极性氨基酸具有极性,而非极性氨基酸则没有极性。 氨基酸是有机化合物。氨基酸由...
- 发布于 2020-10-19 04:50
- 阅读 ( 1177 )
电负性(electronegativity)和极性(polarity)的区别
...才是极性的。一个带有永久性偶极子的分子可以在另一个非极性分子中诱导一个偶极子,然后这个非极性分子也会变成暂时性的极性分子。即使在一个分子内,某些变化也可能引起暂时的偶极矩。 电负性(electronegativity)和极性(pol...
- 发布于 2020-10-22 10:07
- 阅读 ( 900 )
胶体(colloid)和解决方案(solution)的区别
...的一个例子。也有许多有机溶剂。溶质颗粒的溶解取决于极性。极性溶质粒子只溶于极性溶剂,而非极性溶质则溶于非极性溶剂。下面给出一些例子。 水(极性溶剂)+盐(极性溶质) 液溴(非极性溶剂)+固体碘(非极性溶剂...
- 发布于 2021-06-28 12:15
- 阅读 ( 663 )
解决方案(solution)和暂停(suspension)的区别
...有粒子沉降。 溶液的形成取决于溶质对溶剂的亲和力。极性溶质只溶于极性溶剂,非极性溶质只溶于非极性溶剂。水是最著名的极性溶剂。极性溶质如盐、糖、KCl等易溶解。大多数有机溶剂如苯、己烷和石油醚是非极性的。碘...
- 发布于 2021-06-28 12:17
- 阅读 ( 456 )
极地的(polar)和非极性分子(nonpolar molecules)的区别
主要差异极性(main difference polar) vs. 非极性分子(nonpolar molecules) 不同或相同元素的原子聚在一起形成分子。由两个原子共用一对电子形成的键称为“共价键”。不同的原子对电子有不同程度的吸引力。它们把电子拉向它们...
- 发布于 2021-06-28 12:20
- 阅读 ( 1818 )
如何极性分子和非极性分子相互作用(polar and nonpolar molecules interact with each other)
共价物质中既有极性分子也有非极性分子。有些共价分子有极化的能力,有些则没有。极性分子和非极性分子以不同的方式相互作用。极性分子通过偶极-偶极相互作用等力相互作用,而非极性分子通过伦敦色散力相互作...
- 发布于 2021-06-28 12:27
- 阅读 ( 915 )
简单扩散(simple diffusion)和促进扩散(facilitated diffusion)的区别
...就达到平衡,没有观察到分子的净运动。一般来说,小的非极性分子如氧气、二氧化碳和乙醇可以自由地扩散到细胞膜上。扩散速率取决于温度、分子大小和浓度梯度的陡度。温度影响溶液中粒子的动能。与较小的粒子相比,较...
- 发布于 2021-06-28 18:30
- 阅读 ( 636 )
坚强的(strong)和弱酸(weak acids)的区别
...要区别的比较 关键词:酸,酸离解常数,脱质子,pH值,极性,质子,强酸,弱酸 什么是强酸(a strong acid)? 强酸是在水中完全分解成离子的分子。换句话说,酸通过完全电离将H+离子释放到溶液中。酸的强度由其酸离解常数(K...
- 发布于 2021-06-28 19:21
- 阅读 ( 1047 )
共价的(covalent)和配位键(coordinate bond)的区别
...了形成一个双键,每个原子有两个电子。 共价键可以是极性键也可以是非极性键,这取决于每个原子的电负性。如果两个原子的电负性之差很小(小于0.4)或为零,则形成非极性共价键。如果两个原子的电负性之差更大(0.4-1.7...
- 发布于 2021-06-29 10:35
- 阅读 ( 842 )
共价的(covalent)和氢键(hydrogen bonds)的区别
...氟原子最外层轨道中的电子。 共价键主要有两种类型:极性共价键和非极性共价键。这两个键是根据共价键的极性命名的。键的极性取决于形成共价键的两个原子的电负性值。如果这些电负性值之间的差值小于0.4,则为非极性...
- 发布于 2021-06-29 11:01
- 阅读 ( 629 )