胶体(colloid)和解决方案(solution)的区别
主要区别胶体(main difference colloid) vs. 解决方案(solution)
胶体和溶液的主要区别在于它们的颗粒大小。溶液中的微粒比胶体中的微粒小。在光学显微镜下看不到溶质颗粒;然而,在相同的条件下可以看到胶体颗粒。
这篇文章解释道,
1.什么是胶体?–定义、特性、示例
2.什么是解决方案?–定义、特性、示例
3.如何从溶液中分离胶体离心、超滤、透析
4. What is the difference between Colloid and Solution?
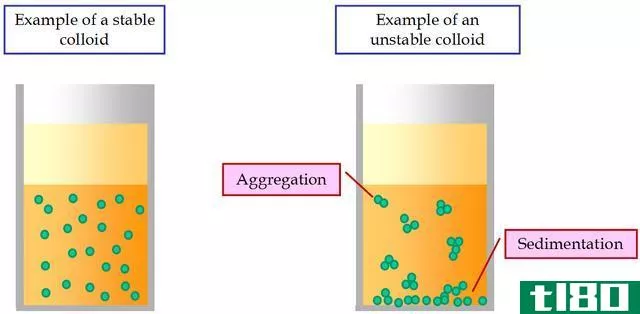
什么是胶体(a colloid)?
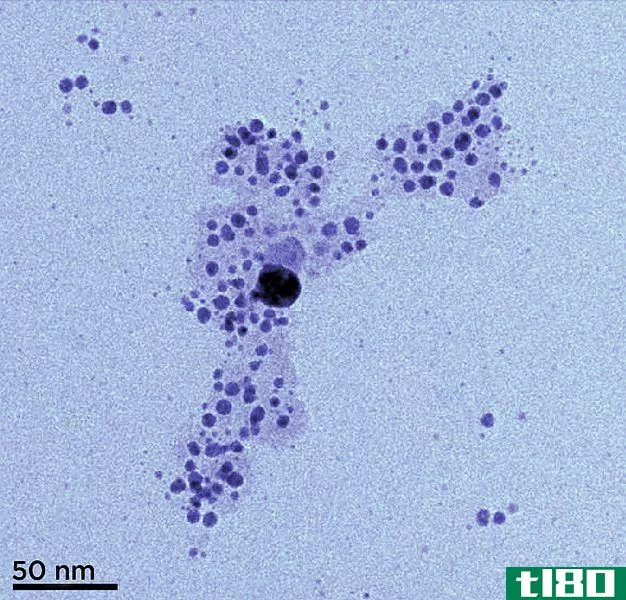
胶体是一种特殊物质的状态,其粒径在1-200纳米之间。这些都不足以成为一个暂停,也不会脱离解决方案。胶体系统由分散在分散介质中的胶粒组成。由于光被较大的粒子散射,胶体溶液常常显得不透明。这种现象被称为廷德尔效应。
不同类型胶体系统的例子
| 分散相 | 分散介质 | 胶体体系 | 示例 |
| 固体 | 固体 | 固体溶胶 | 矿物、宝石、玻璃 |
| 固体 | 液体 | 溶胶 | 浑水,水中淀粉,细胞液 |
| 固体 | 煤气 | 固体气溶胶 | 沙尘暴、烟雾 |
| 液体 | 液体 | 乳化液 | 药物、牛奶、洗发水 |
| 液体 | 固体 | 凝胶 | 黄油、果冻 |
| 液体 | 煤气 | 液体气溶胶 | 雾,雾 |
| 煤气 | 固体 | 固体泡沫 | 石材、泡沫橡胶 |
| 煤气 | 液体 | 泡沫,泡沫 | 苏打水、鲜奶油 |
In the above systems, the dispersed phase always contains particles with sizes ranging from 1-200 nm; hence, these particles are colloids. The dispersion medium is where these particles are dispersed.
什么是解决方案(a solution)?
溶液是溶剂和溶质粒子的组合。溶质颗粒溶解在溶剂中,大小<1 nm。这些溶质颗粒肉眼看不见,不能通过滤纸过滤。它们可以是离子、单分子或晶体,均匀地分布在溶剂中。糖溶液和盐溶液可以作为例子。溶液总是同质的,站着不沉淀。光通过溶液时没有任何散射。
溶剂主要是液体。水是溶剂的一个例子。也有许多有机溶剂。溶质颗粒的溶解取决于极性。极性溶质粒子只溶于极性溶剂,而非极性溶质则溶于非极性溶剂。下面给出一些例子。
水(极性溶剂)+盐(极性溶质)
液溴(非极性溶剂)+固体碘(非极性溶剂)

如何从溶液中分离胶体
胶体不容易从溶液中分离出来。因此,必须采用离心、超滤和透析等方法来分离它们。
离心
含有胶体和其他杂质的溶液会受到离心力的作用,从而导致胶体沉淀。离心后,密度较小的颗粒倾向于留在溶液中。然后可以除去溶液并回收胶体颗粒。
超滤
这种方法是基于这样一个事实:由于胶体的大小,它们无法通过某些膜。该方法可采用孔径小于1nm的特制过滤器。超滤器保留胶体颗粒,让溶液中的小颗粒通过。它们是通过用明胶或火棉胶处理普通滤纸来制备的,明胶或火棉胶可以缩小孔径。
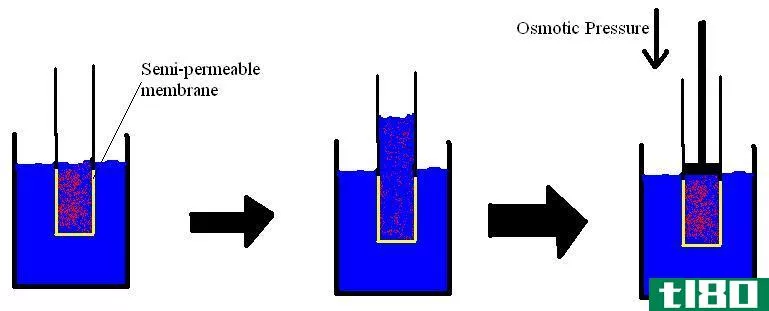
透析
透析是将胶体从尺寸较小的溶质颗粒中分离出来的过程。这个过程是由化学家托马斯·格雷厄姆在1861年发现的。透析过程是由于胶体和溶质颗粒(离子、分子或晶体)通过半透膜的渗透性不同而发生的。这种方法常用于治疗肾脏疾病等医学治疗。
胶体(colloid)和解决方案(solution)的区别
粒度
胶体的粒径为1-200nm。
溶液的粒径为<;1牛米。
自然
胶体是不均匀的。
解决方案是同质的。
渗透
胶体只能通过超滤纸渗透。
溶液可透过大多数膜。
廷德尔效应
光被胶体中较大的粒子散射。
光通过溶液。
系统外观
胶体是半透明的。
解决方案是透明的。
溶质分子和胶体都不与溶剂发生化学键合;因此,它们可以在物理上恢复。
参考列表:
“胶体溶液、真溶液和悬浮液|化学学习。”胶体溶液、真溶液和悬浮液|化学学习。N.p.,N.d.网站。2017年1月26日。
G、 Ellis Sidney、Stevenson Peter C和Rca Corp.“专利US2648636–胶体溶液中胶体分离的方法和装置”,谷歌图书。N.p.,N.d.网站。2017年1月26日。
Gimbert, Laura J., et al. “Comparison of centrifugation and filtration techniques for the size fractionation of colloidal material in soil suspensi*** using sedimentation field-flow fractionation.” Environmental science & technology39.6 (2005): 1731-1735.
Law , Jimmy. “Colloids.” Chemistry LibreTexts. libretexts,2017年1月9日,网络。2017年1月26日。
Raymond, Kenneth W. General Organic and Biological Chemistry. john wiley&s***,2009年。
“Study Material, Chemistry, Surface Chemistry, Purification of Colloidal Solution.” Purification Of Colloids, Dialysis, ElectroDialysis, Ultra filtration, Chemistry Study Material @eMedicalprep.Com. n、 p.,n.d.网站。2017年1月26日。
沃尔特,沃兰。”溶液和混合物在线化学入门。http://www.800mainstreet.com/,2005年3月29日。2017年1月26日。
Image Courtesy:
“Spoon Sugar Solution with Glass” By APN MJM – Own work (CC BY-SA 3.0)通过Comm*** Wikimedia
“Milk – olly claxton” By Pingpongwill at English Wikipedia (CC BY-SA 3.0) 通过Comm*** Wikimedia
- 发表于 2021-06-28 12:15
- 阅读 ( 651 )
- 分类:科学
你可能感兴趣的文章
纳米银(nano silver)和胶体银(colloidal silver)的区别
...化为胶体银粒子时,就会发生这种形核。 什么是胶体银(colloidal silver)? 胶体银是一种悬浮在液体中的银颗粒。这些银粒子的尺寸大于100nm。通常,胶体银被市场作为口服膳食补充剂。然而,胶体银是以注射的形式出现的,或者...
- 发布于 2020-09-20 11:34
- 阅读 ( 674 )
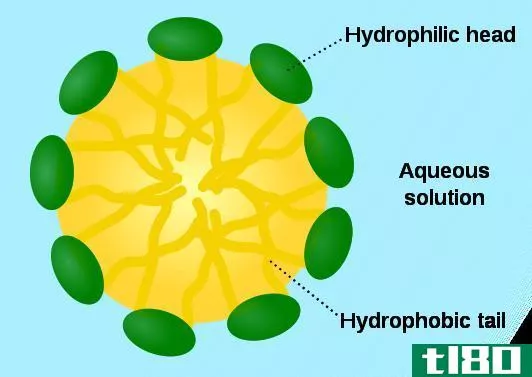
微胶粒(micelles)和胶粒(colloidal particles)的区别
...物的熵和焓之间的平衡,胶束会自发形成。 什么是胶粒(colloidal particles)? 胶粒是分散在悬浮液中的粒子。这种悬浮液称为胶体悬浮液。悬浮颗粒可以是可溶或不溶的颗粒。胶体有两种不同的物质相:液相溶剂和固相颗粒。液相...
- 发布于 2020-10-01 01:11
- 阅读 ( 593 )
离子型(ionic)和胶体银(colloidal silver)的区别
...有形成团簇(这是胶体银的常见问题)。 什么是胶体银(colloidal silver)? 胶态银是一种补充形式,由离子化和结合形式的银组成。这种溶液的形成是由于一个电磁过程,它将亚微观的银粒子(在微米范围内)从一块较大的纯银中...
- 发布于 2020-10-17 16:12
- 阅读 ( 534 )
胶体(colloid)和乳状液(emulsion)的区别
.... 并列比较-胶体与乳状液的表格形式 5. 摘要 什么是胶体(colloid)? 胶体是一种均匀的非晶态物质,由一种物质的大分子或超微颗粒组成,分散在另一种物质中。分散的粒子不会自发沉降,因为胶体非常稳定。 根据不同的参数,...
- 发布于 2020-10-18 14:47
- 阅读 ( 425 )
冻干性(lyophilic)和憎液胶体(lyophobic colloids)的区别
...较-表格形式的嗜干胶体和憎干胶体 6. 摘要 什么是胶体(colloids)? 胶体是直径在1-1000nm范围内的任何物质的微粒。胶体系统由两个相组成:(A)连续相,即细颗粒分布的介质;(b)不连续或分散相,即胶体范围内的细颗粒相。分...
- 发布于 2020-10-20 18:29
- 阅读 ( 209 )
真解(true solution)和胶体溶液(colloidal solution)的区别
...分离,然后用特殊的过滤器过滤。 廷德尔效应: 真正的解决方案:真正的解决方案不显示廷德尔效应。(不要散射光) 胶体溶液:胶体溶液表现出廷德尔效应。(也被称为“廷德尔散射”,是指胶体中的粒子或极细悬浮液中的...
- 发布于 2020-10-24 11:38
- 阅读 ( 633 )
解决方案(solution)和胶体(colloid)的区别
...质以不同的比例混合。 目录 1. 概述和主要区别 2. 什么是解决方案 3. 什么是胶体 4. 并列比较-溶液与胶体的表格形式 5. 摘要 什么是解决方案(the solution)? 溶液是两种或两种以上物质的均匀混合物。我们称之为均相混合物,因为...
- 发布于 2020-10-24 22:17
- 阅读 ( 207 )
胶体二氧化硅(colloidal silica)和活性二氧化硅(reactive silica)的区别
...活性二氧化硅的表格形式 5. 摘要 什么是胶体二氧化硅(colloidal silica)? 胶体二氧化硅是二氧化硅颗粒在液相中的悬浮液。这种悬浮液中的二氧化硅结构可以描述为无定形、无孔、典型的球形二氧化硅颗粒。当二氧化硅颗粒在水...
- 发布于 2020-11-02 16:25
- 阅读 ( 541 )
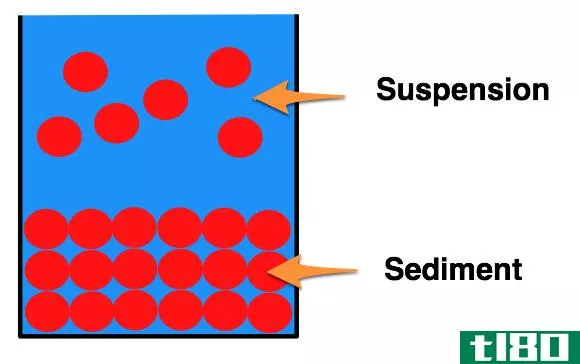
暂停(suspension)和胶体(colloid)的区别
...分离。悬浮液不透明,因为悬浮液不透光。 什么是胶体(colloid)? 胶体溶液是一种均匀的混合物,但也可以是不均匀的混合物(如牛奶、雾)。如果我们把胶体溶液中的颗粒与溶液和悬浮液中的颗粒相比较,它们是中等大小的(...
- 发布于 2020-11-02 21:50
- 阅读 ( 464 )
类晶体(crystalloids)和胶体(colloids)的区别
...过度使用晶体液治疗可导致周围和肺水肿。 什么是胶体(colloids)? 胶体溶液是一种均匀的混合物,但也可以是非均质的(例如牛奶、雾)。与溶液、悬浮液或晶体中的颗粒相比,胶体溶液中的颗粒尺寸中等(大于分子)。但是就...
- 发布于 2020-11-04 21:03
- 阅读 ( 502 )