极性键的定义和示例
化学键可分为极性键和非极性键。区别在于键中电子的排列方式。

什么是化学中的极性键(a polar bond in chemistry)?
- 极性键是一种共价键,其中形成键的电子分布不均匀。换句话说,电子在键的一侧比在键的另一侧花费更多的时间。
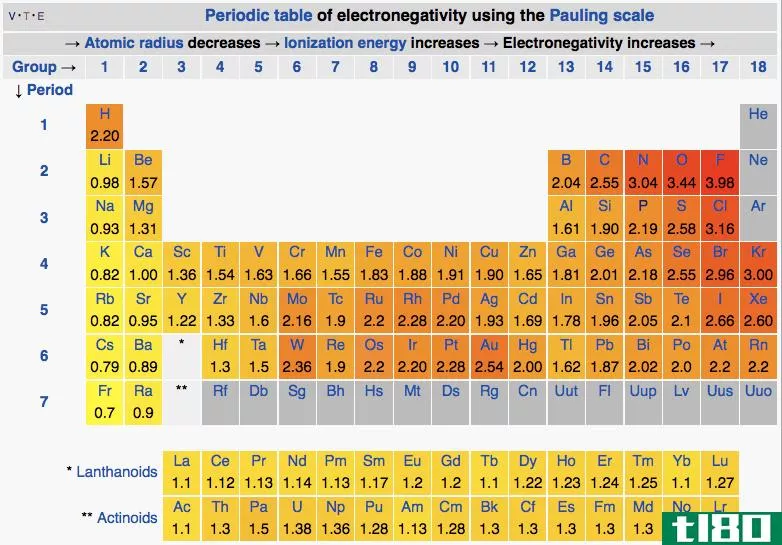
- 极性键介于纯共价键和离子键之间。当阴阳离子之间的电负性差在0.4和1.7之间时形成。
- 具有极性键的分子包括水、氟化氢、二氧化硫和氨。
极性键定义
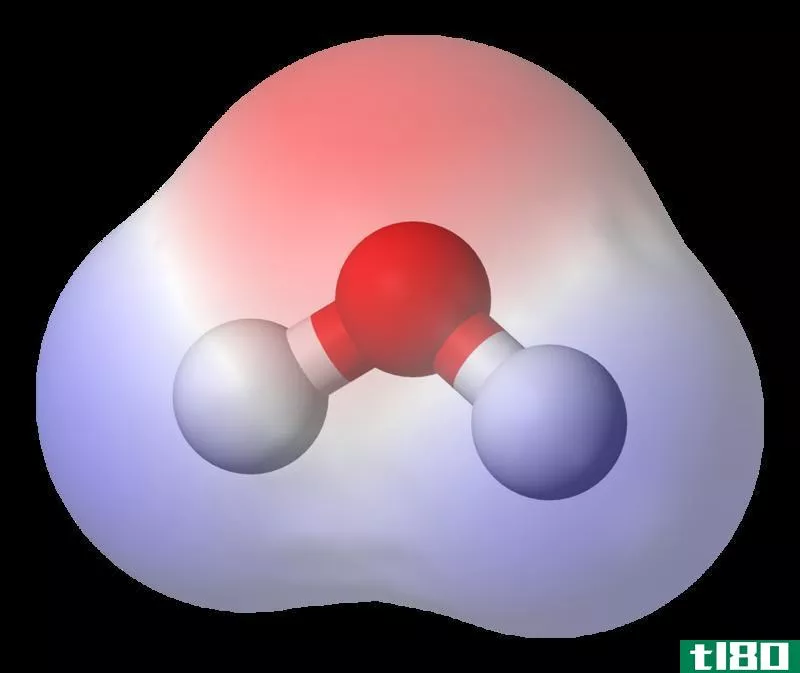
极性键是两个原子之间的共价键,其中形成键的电子分布不均匀。这使得分子有一个轻微的电偶极矩,一端略为正,另一端略为负。电偶极子的电荷小于一个完整的单位电荷,因此它们被认为是部分电荷,用δ+和δ-表示。因为正电荷和负电荷在键中分开,所以具有极性共价键的分子与其他分子中的偶极子相互作用。这会在分子之间产生偶极-偶极分子间作用力。
极性键是纯共价键和纯离子键的分界线。纯共价键(非极性共价键)在原子之间平均共享电子对。在技术上,非极性键只在原子彼此相同(例如H2气体)时发生,但化学家认为原子之间的键与电负性差小于0.4是非极性共价键。二氧化碳(CO2)和甲烷(CH4)是非极性分子。
但是离子键不是极性的吗?
在离子键中,键中的电子基本上由另一个原子(如NaCl)提供给一个原子。当原子间的电负性差大于1.7时,原子间形成离子键。从技术上讲,离子键是完全极性键,因此术语可能会混淆。
请记住,极性键指的是一种共价键,其中电子不是平均共享的,电负性值略有不同。极性共价键形成于电负性差在0.4和1.7之间的原子之间。
具有极性共价键的分子示例
水(H2O)是一种极性键合分子。氧的电负性值为3.44,而氢的电负性值为2.20。电子分布的不均匀性解释了分子的弯曲形状。分子的氧“侧”有净负电荷,而两个氢原子(在另一“侧”)有净正电荷。
氟化氢(HF)是具有极性共价键的分子的另一个例子。氟原子的电负性更强,因此键中的电子与氟原子的联系比与氢原子的联系更为密切。形成偶极子,其中氟侧具有净负电荷,氢侧具有净正电荷。氟化氢是线性分子,因为只有两个原子,所以不可能有其他几何结构。
氨分子(NH3)在氮原子和氢原子之间有极性共价键。偶极子使得氮原子带更多的负电荷,三个氢原子都在氮原子带正电荷的一侧。
哪些元素形成极性键?
极性共价键形成于两个彼此电负性完全不同的非金属原子之间。由于电负性值略有不同,原子之间的键电子对并不均等。例如,极性共价键通常在氢和任何其他非金属之间形成。
金属和非金属之间的电负性值很大,因此它们彼此形成离子键。通常氢作为非金属而不是金属。
来源
- 英戈尔德,C.K。;Ingold,E.H.(1926年)。“碳链中交替效应的性质。第五部分。芳香取代的讨论,特别是极性和非极性离解的各自作用;以及氧和氮的相对定向效率的进一步研究”。J.Chem。Soc:1310–1328。内政部:10.1039/jr9262901310
- 《化学键的性质》(第三版)。牛津大学出版社。第98-100页。ISBN 080140332。
- 齐埃·莫亚耶德、玛亚姆;爱德华·古德曼;威廉姆斯,彼得(2000年11月)。“极性液体流的电偏转:一个被误解的演示”,《化学教育杂志》。77 (11): 1520. 内政部:10.1021/ed077p1520
- 发表于 2021-09-09 13:33
- 阅读 ( 472 )
- 分类:化学
你可能感兴趣的文章
共价键(covalent bond)和与格键(dative bond)的区别
...两个氢原子之间共价键的形成 共价键主要有两种类型:极性键和非极性键。两个原子之间存在极性键,它们的电负性值相差在0.4到1.7之间。如果这个差值小于0.4,就会形成非极性键。这是因为,电负性值之间的高差异意味着,...
- 发布于 2020-10-17 17:57
- 阅读 ( 855 )
电负性(electronegativity)和极性(polarity)的区别
电负性和极性的关键区别在于,电负性是原子吸引键中电子的倾向,而极性意味着电荷的分离。 极性是由于电负性的不同而产生的。因此,这两个术语是密切相关的术语。然而,电负性和极性之间有明显的区别。电负性和极...
- 发布于 2020-10-22 10:07
- 阅读 ( 898 )
电解质(electrolytes)和非电解质(nonelectrolytes)的区别
...产生离子。介质中缺少离子使它们不导电。大多数具有非极性共价键的化合物/有机化合物都属于这一类。例如蔗糖、葡萄糖、乙烷等。 电解质(electrolytes)和非电解质(nonelectrolytes)的区别 电解质与非电解质的主要区别在于,电解...
- 发布于 2020-11-06 17:55
- 阅读 ( 266 )
独联体(cis)和反式(trans)的区别
...由于总偶极矩和分子形状的不平等造成的。 相对沸点由极性决定。它引起分子间作用力增加,从而导致沸点升高。顺式异构体比反式异构体具有更高的沸点。差别可能很小,例如在直链烯烃中。在有极性键的物质中观察到较大...
- 发布于 2021-06-25 06:33
- 阅读 ( 301 )
极地的(polar)和非极性键(nonpolar bonds)的区别
主要差异极性(main difference polar) vs. 非极性键(nonpolar bonds) 极性键和非极性键都是原子间的两种共价键。在共价键合中,电子在两种原子之间共享,而不是完全的电子的送出或接受。然而,根据所涉及的原子类型,共享的...
- 发布于 2021-06-27 10:16
- 阅读 ( 407 )
复合(compound)和混合物(mixture)的区别
...原子被类似的电子吸引(类似的电负性),则化合物是非极性的。然而,如果两个原子之间的电负性间隙很大,化合物就会变成极性化合物。水分子就是这种现象的最好例子。 非极性化合物–甲烷、氨、己烷 Polar Compounds – Wat...
- 发布于 2021-06-28 12:14
- 阅读 ( 502 )
极地的(polar)和非极性分子(nonpolar molecules)的区别
主要差异极性(main difference polar) vs. 非极性分子(nonpolar molecules) 不同或相同元素的原子聚在一起形成分子。由两个原子共用一对电子形成的键称为“共价键”。不同的原子对电子有不同程度的吸引力。它们把电子拉向它们...
- 发布于 2021-06-28 12:20
- 阅读 ( 1815 )
如何极性分子和非极性分子相互作用(polar and nonpolar molecules interact with each other)
共价物质中既有极性分子也有非极性分子。有些共价分子有极化的能力,有些则没有。极性分子和非极性分子以不同的方式相互作用。极性分子通过偶极-偶极相互作用等力相互作用,而非极性分子通过伦敦色散力相互作...
- 发布于 2021-06-28 12:27
- 阅读 ( 903 )
附加(addition)和取代反应(substitution reactions)的区别
...亲电,亲电加成,亲电取代,自由基加成,离去基团,非极性加成反应,亲核,亲核加成,亲核取代,极性加成反应,自由基取代,取代反应,底物 什么是加成反应(addition reaction)? 加成反应是两个或两个以上的原子或分子结...
- 发布于 2021-06-28 19:35
- 阅读 ( 287 )
键对(bond pair)和孤独的一对(lone pair)的区别
...耦合电子的两个术语。这些电子对引起化合物的反应性、极性、物理状态和化学性质。离子化合物可能有也可能没有键对和孤对。共价化合物和配合物本质上都有键对。它们可能有也可能没有单独的一对。键对和孤对的区别在于...
- 发布于 2021-06-29 09:14
- 阅读 ( 631 )