水溶液为什么导电?
水溶液为什么导电?
你可能已经知道,水是电的导体。“水或水溶液”一词确切地说是指“溶于水的任何东西”。并非所有溶液和“物质”都溶于水。有不同的因素决定了这是否可能。
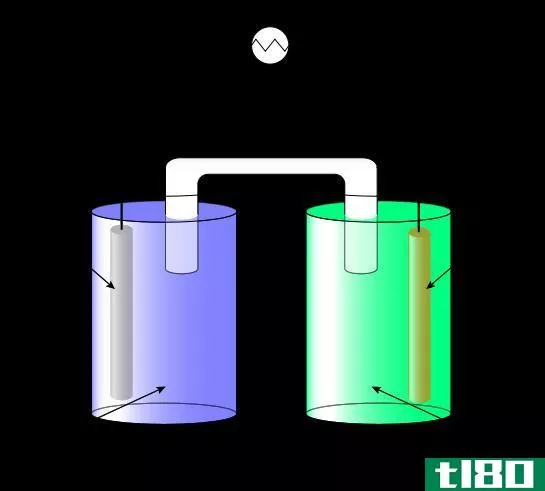
水溶液本质上可以导电或导电,因为它们具有强的“电解质”。还有其他溶液导电性差,因为它们的溶液中电解质较少。水中的离子会影响电流的强度。带电离子的数量越高,通过溶液的电流越强。因此,“如果溶液中有离子,它就会导电”的规则。
水溶液可以像溶解在水中的糖或溶解在水中的盐一样简单。这是一个过程,水是溶剂,其他物质在其中溶解。水溶液可分为两类(就导电溶液而言)电解溶液和非电溶液。
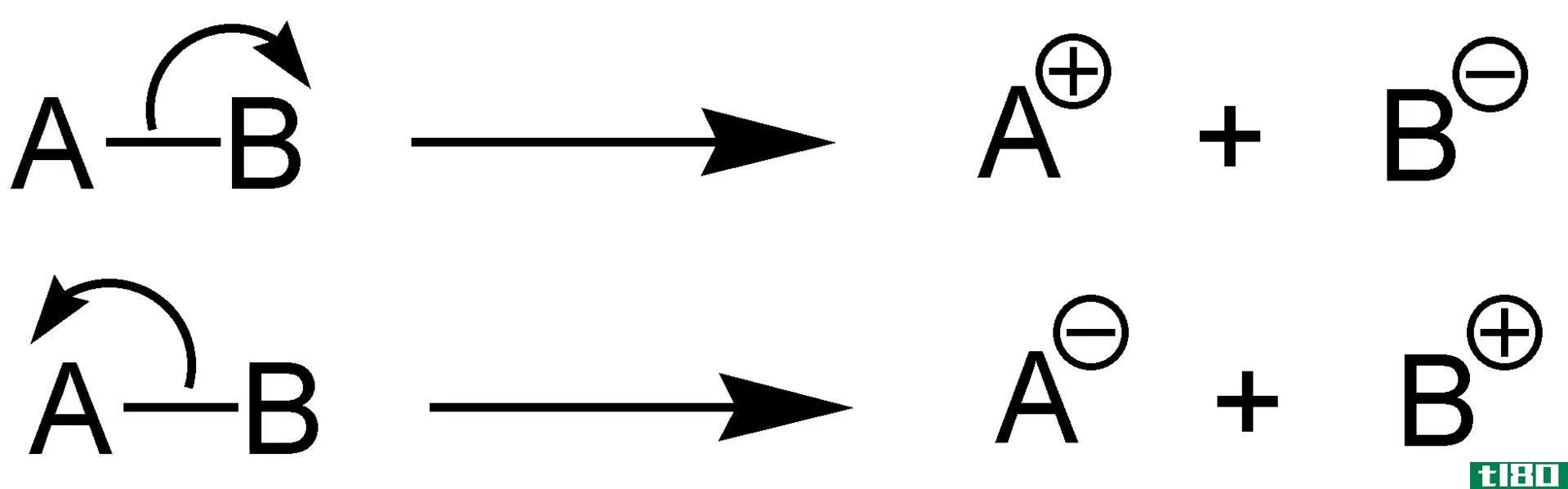
当某物溶于水时,它们的化学和分子化合物有时会分解并与水混合。其中一些溶解并保持在中性状态(分子)。据说有些分子不允许电子运动,这意味着它不利于导电。
就糖和盐而言,盐含有离子,糖含有中性分子。溶解的盐可以导电(特别是因为它含有大量离子),而糖则不导电。这就是离子化合物和分子化合物之间的区别。
还有其他化合物能溶于水并导电。根据它们的离子化合物,它可能导电,也可能不导电。水溶液也分为强电解质、弱电解质和非电解质。
- 发表于 2021-11-19 09:39
- 阅读 ( 228 )
- 分类:科学
你可能感兴趣的文章
涂层(coating)和电镀(plating)的区别
...子涂层。在化学镀方法中,在不使用外部电源的情况下,水溶液中会同时发生多个反应。除此之外,还有一些特定的电镀工艺,它们是根据覆盖层所用的金属命名的;例如,镀金、镀银、镀铬、镀锌、镀铑、镀锡等。 涂层(coating...
- 发布于 2020-09-16 08:59
- 阅读 ( 1811 )
是的(true)和电位电解液(potential electrolyte)的区别
... 潜在电解质是能部分分解成离子的物质。这意味着它在水溶液中不能完全分解成离子。因此,潜在电解质的水溶液中既含有离子物种,也含有未解离的分子。通常,电位电解液的解离度约为1-10%。它们也被称为弱电解质。一些常...
- 发布于 2020-09-21 00:04
- 阅读 ( 240 )
可溶的(soluble)和不溶性盐(insoluble salts)的区别
...在这里,盐的溶解在水中形成离子物种,这使得新形成的水溶液具有很高的导电性。溶解在水中的离子能通过它传导电。可溶盐的一个例子是食盐或氯化钠。食盐的水溶液含有钠离子和氯离子。 什么是不溶性盐(insoluble salts)? ...
- 发布于 2020-10-15 09:54
- 阅读 ( 1465 )
离子型(ionic)和胶体银(colloidal silver)的区别
...称之为银原子。这种补充剂是由水和单原子银离子组成的水溶液;我们称这种银为“溶解银”。因此,在这些溶液中没有银粒子。 由于银离子的存在,这种溶液是导电的。其电导率与溶液的离子浓度成正比。此溶液中的银离子...
- 发布于 2020-10-17 16:12
- 阅读 ( 539 )
电解质的综合性质(colligative properties of electrolytes)和非电解质(nonelectrolytes)的区别
...反比。电解质是能够形成溶液的物质,能够通过这种溶液导电。这种溶液被称为电解溶液。非电解质是不能形成电解溶液的物质。这两种类型(电解质和非电解质)都具有结合性质。电解液和非电解液之间的主要区别在于电解液...
- 发布于 2020-10-17 21:07
- 阅读 ( 274 )
积极的(active)和惰性电极(inert electrodes)的区别
...导体组成。电极通过电子传递电荷,而电解质通过离子传导电荷。电极是一种表面接触电解液的金属。电解液是一种非金属成分,可以是溶液或真空。离子化合物不能以固体形式导电。因此,为了导电,它们应该是液态的。这些...
- 发布于 2020-10-21 08:27
- 阅读 ( 780 )
电导率(conductivity)和摩尔电导率(molar conductivity)的区别
...率和摩尔电导率之间的关键区别在于,电导率是对电解液导电能力的测量,而摩尔电导率是测量每单位摩尔浓度的电解液的电导率。 导电性测量电解液导电的能力。换句话说,它是电解液电导的定量测量。电解质中的离子种类...
- 发布于 2020-10-21 22:22
- 阅读 ( 720 )
弱碱(weak base)和坚实的基础(strong base)的区别
...从而留下一个OH-离子。弱碱溶液的H+浓度高于强碱溶液。 水溶液的碱度由pH值决定。 pH=-log10[H+] 碱的pH值高于7.3。弱碱有条件地被认为是pH值低于10的碱。 由于碱是质子受体,碱从水中接受一个OH离子。弱碱的质子化程度低于强碱...
- 发布于 2021-06-25 17:49
- 阅读 ( 295 )
坚强的(strong)和弱电解质(weak electrolytes)的区别
...分解成离子。正电荷和负电荷离子可以通过这些化合物的水溶液导电。有些电解质是强化合物,另一些是弱电解质。强电解质和弱电解质的主要区别在于,强电解质几乎完全分解成离子,而弱电解质则部分分解成离子。 覆盖的...
- 发布于 2021-06-29 14:13
- 阅读 ( 292 )
电解质(electrolytes)和非电解质(nonelectrolytes)的区别
...ence electrolytes) vs. 非电解质(nonelectrolytes) 化合物根据其在水溶液中导电的能力可分为两类。这两类是电解质和非电解质。电解质是一种能溶于水形成离子的化合物。这些离子可以通过溶液导电。非电解质是在水中溶解时不导电的...
- 发布于 2021-06-29 15:50
- 阅读 ( 551 )