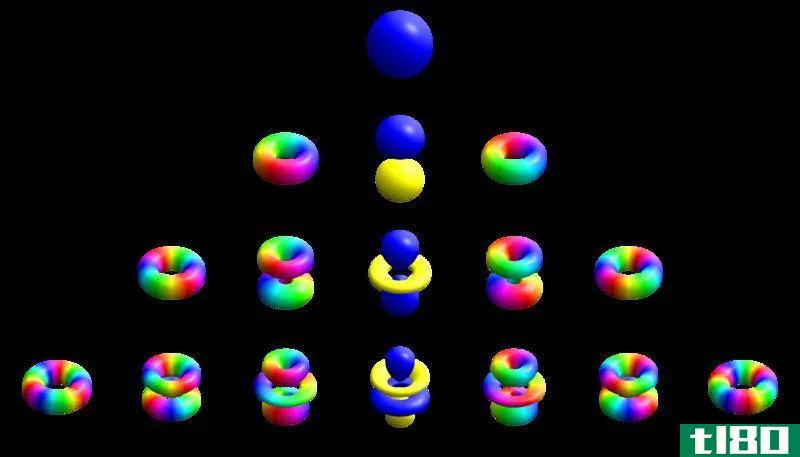方位角量子数和主量子数的关键区别在于,方位角量子数描述的是原子中电子的角动量,而主量子数描述的是电子轨道的大小。
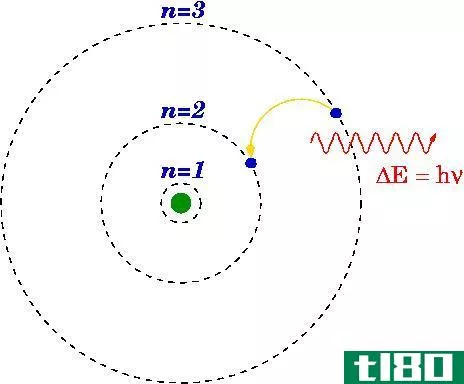
量子数是描述原子能级的重要数值。我们可以用四个量子数来描述电子在原子中的位置。它们是主量子数、方位量子数、磁量子数和自旋量子数。
目录
1. 概述和主要区别
2. 什么是方位量子数
3. 什么是主量子数
4. 并列比较-以表格形式显示方位角与主量子数
5. 摘要
什么是方位量子数(azimuthal quantum number)?
方位量子数是描述原子中电子的角动量的量子数。因此,我们也可以称之为轨道角动量量子数。字母“l”表示方位量子数。此外,这个量子数决定了电子存在的轨道的形状。它是四个量子数集合中的第二个。因此,我们可以用量子数来描述量子数(因为我们可以用第二个量子数来描述它)。方位量子数与角动量的关系式如下:
L2ψ=h2l(l+1)ψ
其中L2是轨道角动量算符,Ψ是电子的波函数,h是约化普朗克常数。在这里,我总是一个正整数。根据量子力学,每个能级有不同的次壳层。这些亚壳的形状和方向各不相同。一个能级的子壳层被命名为-I,0和+l。
| 方位角数 | 表示 | 轨道数 | 最大电子数 |
| 0 | s | 1 | 2 |
| 1 | p | 3(=-1,0,+1) | 6 |
| 2 | d | 5(=-2,-1,0,+1,+2) | 10 |
| 三 | f | 7(=-3,-2,-1,0,+1,+2,+3) | 14 |
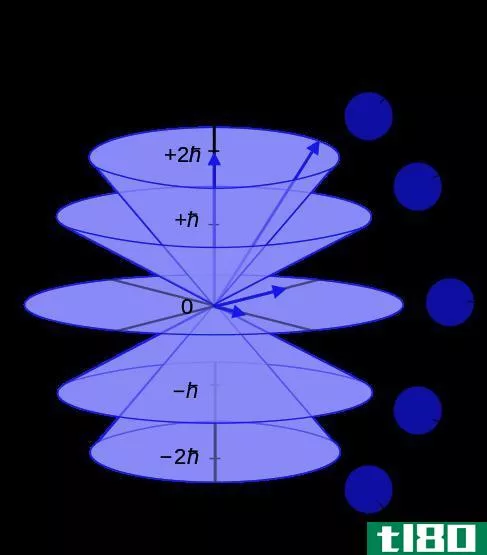
图02:方位角量子数从-l,0到+l
什么是主量子数(principal quantum number)?
主量子数是描述电子存在的主要能级的量子数。我们可以用“n”来表示。因为它是四个不同量子数中的第一个,所以我们也可以称之为第一个量子数。主量子数的值是从1开始的正整数,即n=1,2,3,…
主量子数的值越大,电子的能量就越高;因此,电子与原子松散地结合在一起。这意味着,高“n”值指的是更高的能量水平。此外,对于每个“n”值,方位量子数、磁量子数和自旋量子数都有不同的值。这是因为每个能级都有自己的子壳层、轨道和电子对。
方位角(azimuthal)和主量子数(principal quantum number)的区别
量子数是描述原子能级的重要数值。有四种不同的量子数,前两种是主量子数和方位量子数。方位角量子数和主量子数的关键区别在于,方位角量子数描述的是原子中电子的角动量,而主量子数描述的是电子轨道的大小。我们可以用“l”表示方位量子数,用“n”表示主量子数。
此外,方位量子数描述了轨道的角动量和轨道形状,而主量子数描述了电子存在的能级。
下面的信息图总结了方位角和主量子数之间的区别。
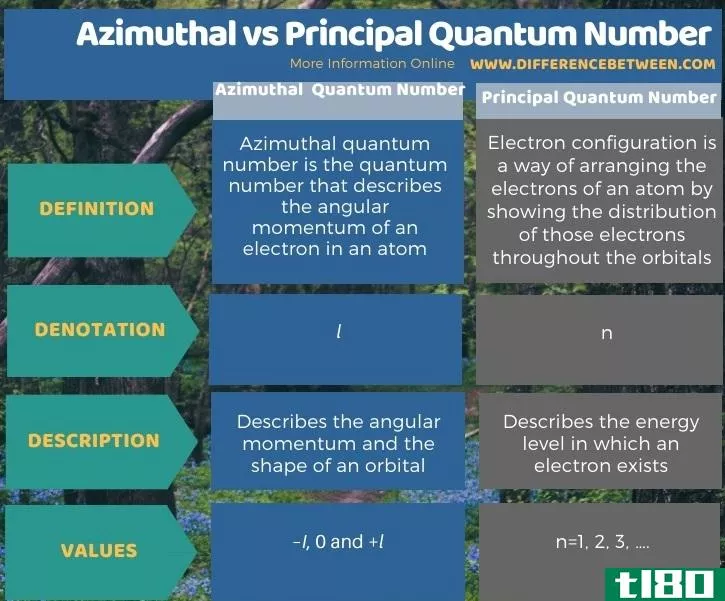
总结 - 方位角(azimuthal) vs. 主量子数(principal quantum number)
量子数是描述原子能级的值。有四种不同的量子数,前两种是主量子数和方位量子数。方位角量子数和主量子数的关键区别在于,方位角量子数描述的是原子中电子的角动量,而主量子数描述的是电子轨道的大小。
引用
1赫尔曼斯汀,安妮·玛丽。“方位量子数定义”,ThoughtCo,2018年6月22日,可在此处查阅。赫尔曼斯汀,安妮·玛丽。“主量子数定义”,ThoughtCo,2019年11月6日,可在此处查阅。
2赫尔曼斯汀,安妮·玛丽。“主量子数定义”,ThoughtCo,2019年11月6日,