SO2和SO3的主要区别在于,在室温下,SO2是无色气体,而SO3是无色到白色的晶体固体。
SO2是二氧化硫,而SO3是三氧化硫。两者都是硫的氧化物。
目录
1. 概述和主要区别
2. 什么是二氧化硫
3. 什么是SO3
4. 并列比较——SO2与SO3的表格形式
5. 摘要
什么是二氧化硫(so2)?
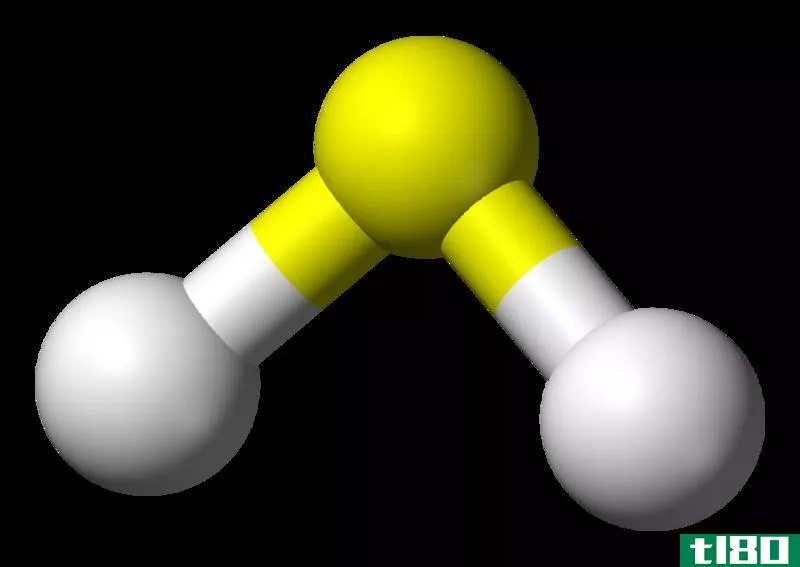
二氧化硫是二氧化硫。它是一种无色气态化合物,含有硫和氧原子。二氧化硫是这种化合物的化学式。因此,它含有一个硫原子通过共价键与两个氧原子结合。一个氧原子能与硫原子形成双键。因此,硫原子是化合物的中心原子。硫原子的最外层轨道上有6个电子。因此,在与氧原子形成两个双键后,还剩下两个电子;这些电子以单独的电子对的形式存在。
因此,我们可以确定SO2分子的几何结构,它是角几何。SO2是极性的,因为它的几何结构(角度)和一对孤电子对的存在。

图01:二氧化硫的结构
二氧化硫被认为是一种有毒气体。因此,如果大气中有二氧化硫,就说明空气污染了。而且,这种气体有一种非常**的气味。二氧化硫的分子量为64g/mol,在室温下是无色气体。熔点约为-71℃,而沸点为-10℃。
二氧化硫中硫的氧化态为+4。因此,二氧化硫也可以通过还原由处于较高氧化状态的硫原子组成的化合物而产生。其中一个例子就是铜和硫酸之间的反应。在这里,硫酸中的硫处于+6的氧化状态。因此,它可以还原为二氧化硫的+4氧化状态。
二氧化硫可用于硫酸生产,在工业规模和实验室规模都有许多应用。二氧化硫也是一种很好的还原剂。由于二氧化硫中硫的氧化态是+4,很容易被氧化到+6氧化态,从而使另一种化合物还原。
什么是三氧化硫(so3)?
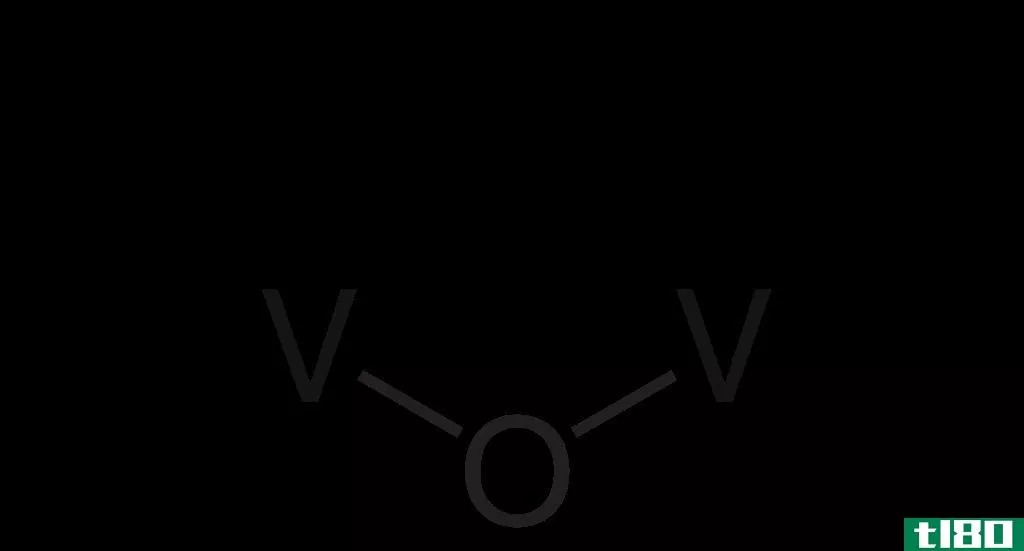
SO3是三氧化硫。它是一种固体化合物,含有一个硫原子,与三个氧原子结合。SO3是这种化合物的化学式。在这里,每个氧原子和硫原子都有一个双键。硫原子在分子的中心。硫原子的最外层轨道上有6个电子。因此,在与氧原子形成三个双键后,硫原子上就不再有像二氧化硫那样的电子了。因此,这决定了SO3分子的几何结构;它具有三角形的平面几何结构。SO3是非极性的,因为它的几何结构(三角平面)和没有一个单独的电子对。
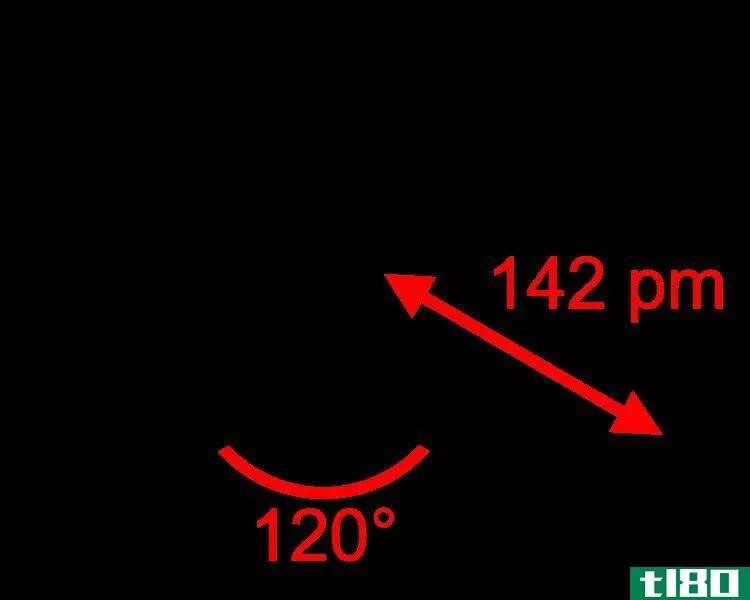
图02:三氧化硫的几何结构
三氧化硫的分子质量为80.057g/mol,SO3的熔点约为16.9℃,而沸点为45℃。在室温和常压下,三氧化硫是一种白色晶体固体化合物,在空气中会冒烟。它有刺鼻的气味。三氧化硫中硫的氧化态为+6。
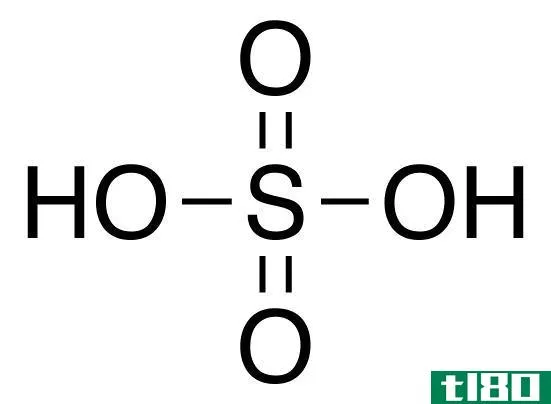
以气态形式存在的三氧化硫是一种空气污染物,是酸雨的主要成分。然而,在工业规模的硫酸生产中,三氧化硫是非常重要的。这是因为三氧化硫是硫酸的酸酐形式。
SO3(l)+H2O(l)→H2SO4(l)
上述反应非常迅速且放热。因此,在工业硫酸生产中使用三氧化硫时,应采取控制措施。此外,三氧化硫是磺化过程中的重要试剂。
二氧化硫(so2)和三氧化硫(so3)的区别
SO2是二氧化硫,而SO3是三氧化硫。两者都是硫的氧化物。SO2和SO3的主要区别在于,在室温下,SO2是无色气体,而SO3是无色到白色的晶体固体。此外,二氧化硫中硫的氧化态为+4,而在三氧化硫中为+6。由于存在一对孤电子及其几何结构,二氧化硫是一种极性化合物,而三氧化硫是一种非极性化合物。以下信息图总结了SO2和SO3之间的区别。

总结 - 二氧化硫(so2) vs. 三氧化硫(so3)
SO2是二氧化硫,SO3是三氧化硫。两者都是硫的氧化物。SO2和SO3的关键区别在于,在室温下,SO2是无色气体,而SO3是无色到白色的晶体固体。
引用
1Malt,Colm等人。“化学品储存、加药和控制”,Tworts Water Supply,2017年,第513-552页。,doi:10.1016/b978-0-08-100025-0.00012-0。