关键区别——协调实体与协调领域
配位体与配位球的主要区别在于配位体是中心原子及其周围配体的集合,而配位体是由配位化合物的电荷给定的配位体。
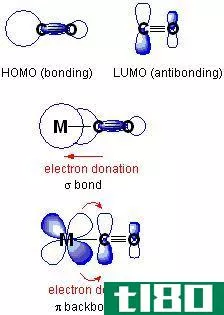
配位化合物是由一个中心原子(通常是一个亚原子或一个金属离子)围绕着被称为配体的分子或离子组成的复杂化合物。这些配体通过配位共价键与中心金属原子结合。当富含电子的分子或离子向金属原子(或离子)捐赠其孤电子对时,这些键就形成了。
目录
1. 概述和主要区别
2. 什么是协调实体
3. 什么是协调球
4. 并列比较-协调实体与表格形式的协调范围
5. 摘要
什么是配位体(coordination entity)?
配位体是配位化合物的组分的集合,包括中心原子和围绕中心原子的配体。配体通过配位共价键与中心原子结合。当一个富含电子的分子或离子将其孤电子对捐赠给一个缺电子的原子时,就形成了一个坐标共价键。
在d块中,中心原子大部分是金属原子。这是因为d块元素有许多空的d轨道(足够空间来容纳入射的孤电子对)。例如,[CoCl2(NH3)4]+的协调实体是CoCl2(NH3)4。中心金属原子是钴(Co)。
什么是协调球(coordination sphere)?
配位球是配位化合物组分的集合,它包括中心原子和围绕中心原子的配位体以及化合物的净电荷。在大多数情况下,中心金属原子是带正电荷的成分(阳离子)。有些配体是带中性电荷的(并且含有可以捐赠的孤电子对),而其他配体是带负电的(阴离子)。因此,配合物的净电荷由中心金属离子和配体电荷共同决定。
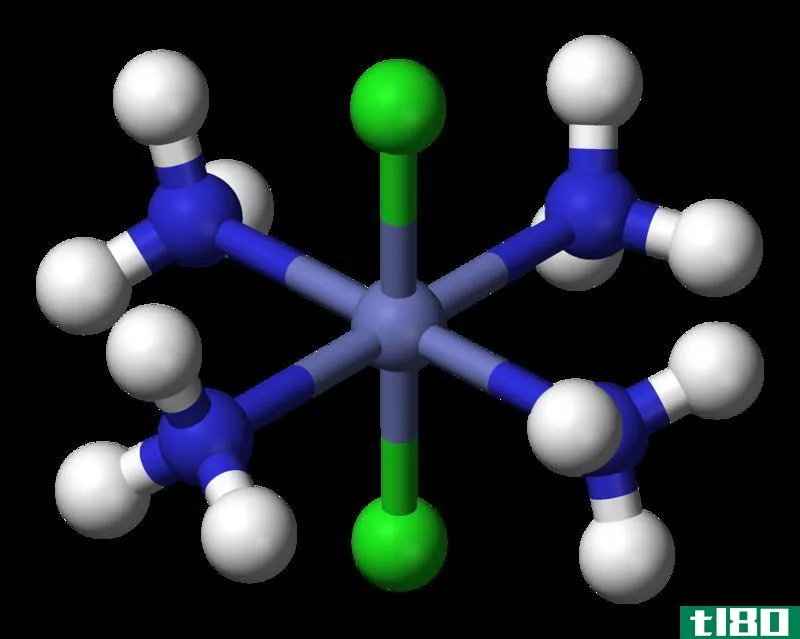
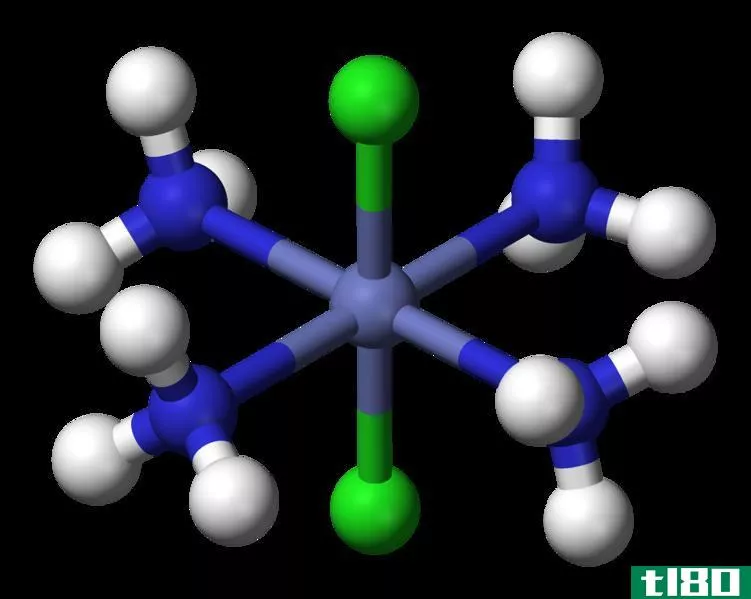
图01反式二氯四胺钴(III)的第一配位球
协调球有两种类型:第一协调球和第二协调球。第一配位球包括直接附着在金属离子上的配体,而第二配位球也包括间接结合的分子和离子。例如,[CoCl2(NH3)4]Cl的第一个配位球是[CoCl2(NH3)4]+,而第二个配位球是Cl-离子。
配位体(coordination entity)和协调球(coordination sphere)的区别
| 协调实体与协调领域 | |
| 配位体是配位化合物的组成部分,它包括中心原子和围绕中心原子的配体。 | 配位球是一种配位化合物的组分的集合,它包括中心原子和围绕中心原子的配体以及化合物的净电荷。 |
| 组件 | |
| 配位体包括配位体中的原子和离子。 | 配位球包括配位化合物中的原子和离子及其电荷。 |
| 电荷 | |
| 配位体中没有提到配位化合物的电荷。 | 配位化合物的电荷是在配位球中提到的。 |
总结 - 配位体(coordination entity) vs. 协调球(coordination sphere)
配位化合物包含一个中心金属原子或离子,被称为配体的分子或离子包围。这些配体是富含电子的组分,可以给金属原子提供电子对。配位体和配位圈是讨论配位化合物的两个术语。配位体与配位球的区别在于配位体是一个中心原子及其周围配位体的集合,而配位球是由配位化合物的电荷给定的配位体。
引用
1“协调领域”,维基百科,维基媒体基金会,2018年2月17日。这里有2个。歌词。《配位化学导论》,化学剧本,剧本,2017年4月20日。此处提供
2歌词。《配位化学导论》,化学剧本,剧本,2017年4月20日。