定域电子和离域电子的关键区别在于,定域电子位于原子之间,而离域电子位于原子的上方和下方。
在一般化学中,定域电子和离域电子是描述化合物化学结构的术语。定域电子是分子中的成键电子,而离域电子是非键电子,它们以电子云的形式出现在分子的上方和下方。
目录
1. 概述和主要区别
2. 什么是定域电子
3. 什么是离域电子
4. 并列比较-局域化和离域电子的表格形式
5. 摘要
什么是定域电子(localized electr***)?
定域电子是化合物中的键合电子。这些电子位于原子之间,在那里可以找到西格玛键。原子的轴心键由重叠的原子键组成。
因此,局域电子出现在具有共价化学键的共价化合物中。这些局域化电子属于两个特定的原子,而离域电子则是分子中所有原子所共有的。定域电子在原子之间共享,形成共价键、配位键等。
什么是离域电子(delocalized electr***)?
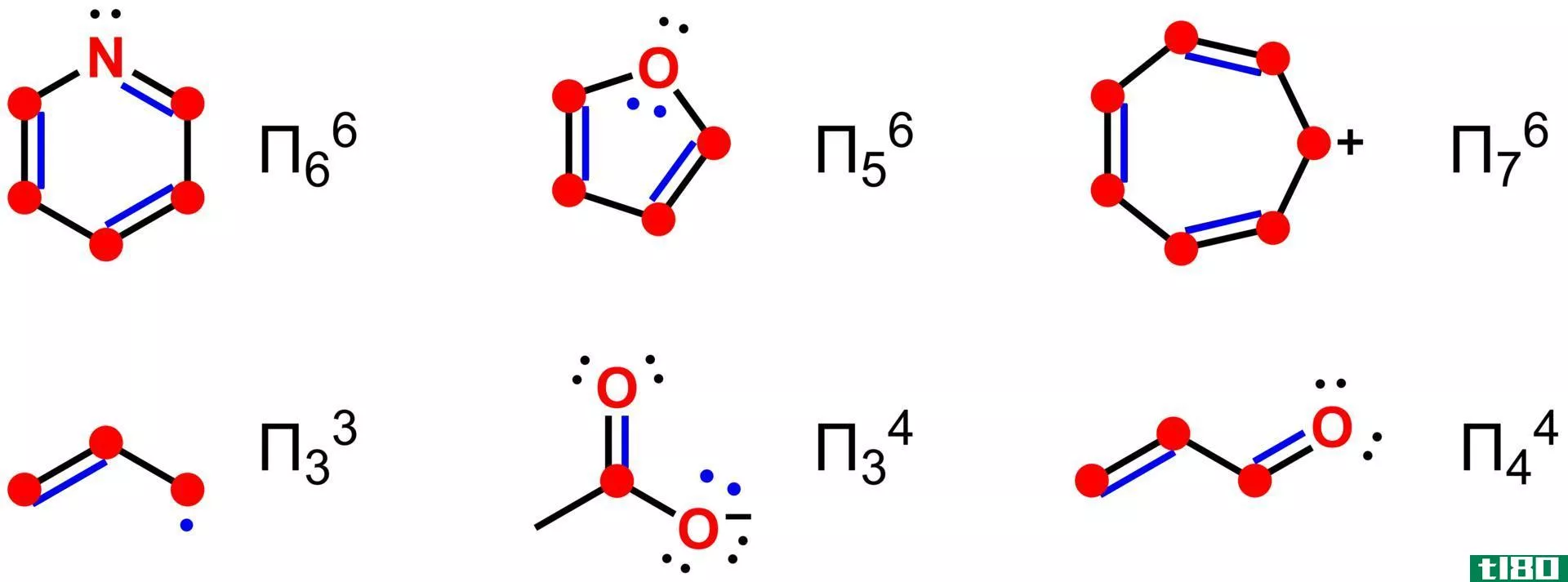
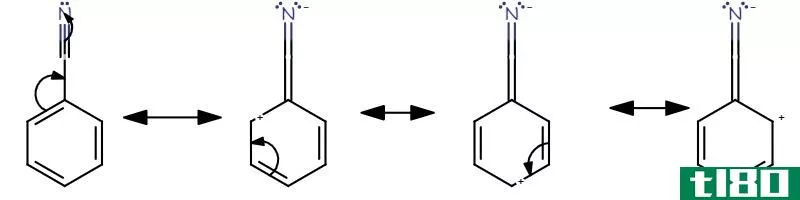
离域电子是化合物中的非键电子。这个术语是指不与单个原子或共价键结合的电子。然而,离域电子这一术语在不同的领域有不同的含义。例如,在有机化学中,离域电子存在于芳香族化合物共轭体系的共振结构中。在固体物理学中,离域电子是促进导电的自由电子。此外,量子物理学使用离域电子这个术语来指那些已经延伸到几个原子上的分子轨道电子。
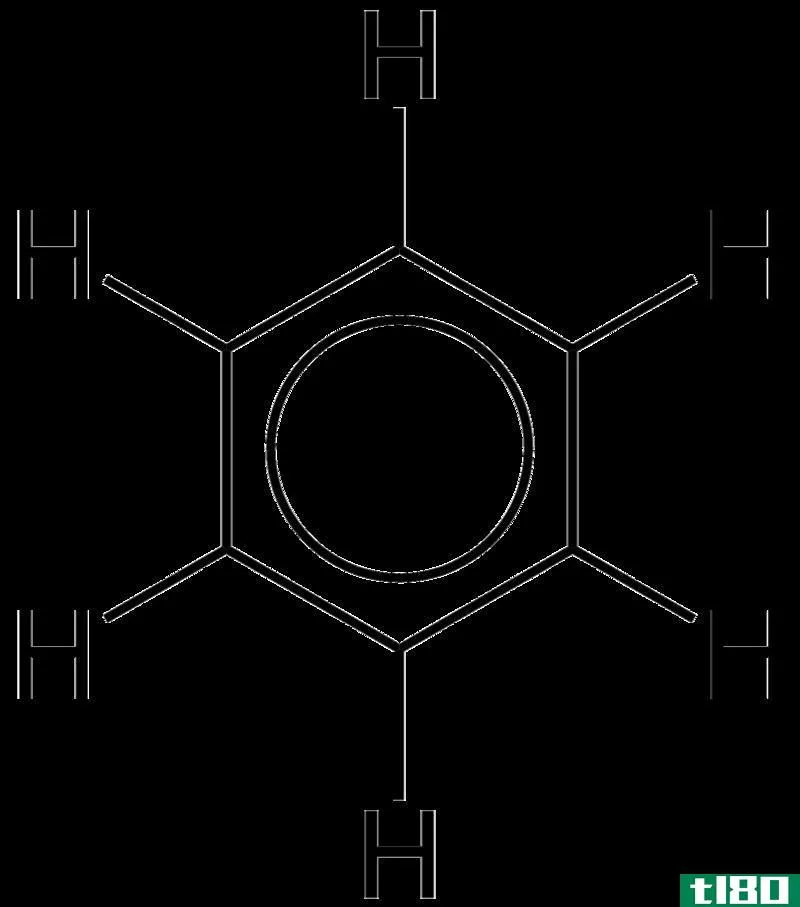
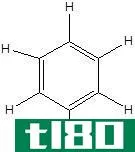
图01:苯(电子的离域用圆圈表示)
苯环是芳香族系统中电子离域最简单的例子。苯分子中有六个π电子;我们通常用一个圆来表示这些电子。这个圆圈意味着π电子与分子中的所有原子有关。这种离域作用使苯环具有具有相似键长的化学键。
本地化(localized)和离域电子(delocalized electr***)的区别
在一般化学的分支下,我们使用局域化和离域电子这两个术语来描述化合物的化学结构。定域原子是属于特定原子的电子,而离域电子是与任何单个原子或单个共价键无关的电子。定域电子和离域电子的关键区别在于,定域电子位于原子之间,而离域电子位于原子的上方和下方。电子被局限在两个特定的原子之间,而电子则分布在两个原子之间。
此外,定域电子与离域电子的另一个显著区别是,定域电子与化合物中的特定原子相关联,而离域电子与分子中的所有原子相关联。此外,定域电子用直线表示,离域电子用圆表示。
下表总结了局域化电子和非局域化电子之间的区别。
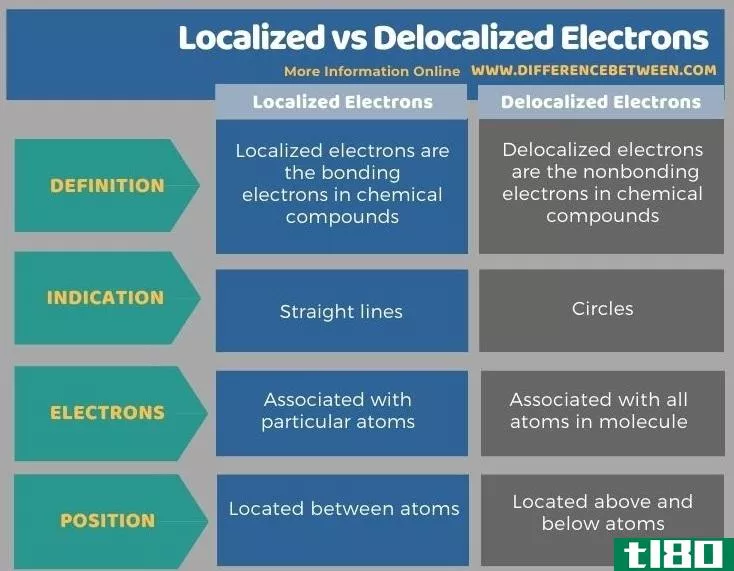
总结 - 本地化(localized) vs. 离域电子(delocalized electron)
在普通化学中讨论了定域和离域电子。定域电子和离域电子的关键区别在于,定域电子位于原子之间,而离域电子位于原子的上方和下方。此外,离域电子与化合物中的特定原子相关,而离域电子与分子中的所有原子相关。
引用
1“局域化和非局域化孤对和键”,《化学步骤》,2020年8月22日,可在这里查阅。“离域电子”,维基百科,维基媒体基金会,2020年7月13日,可在这里查阅。