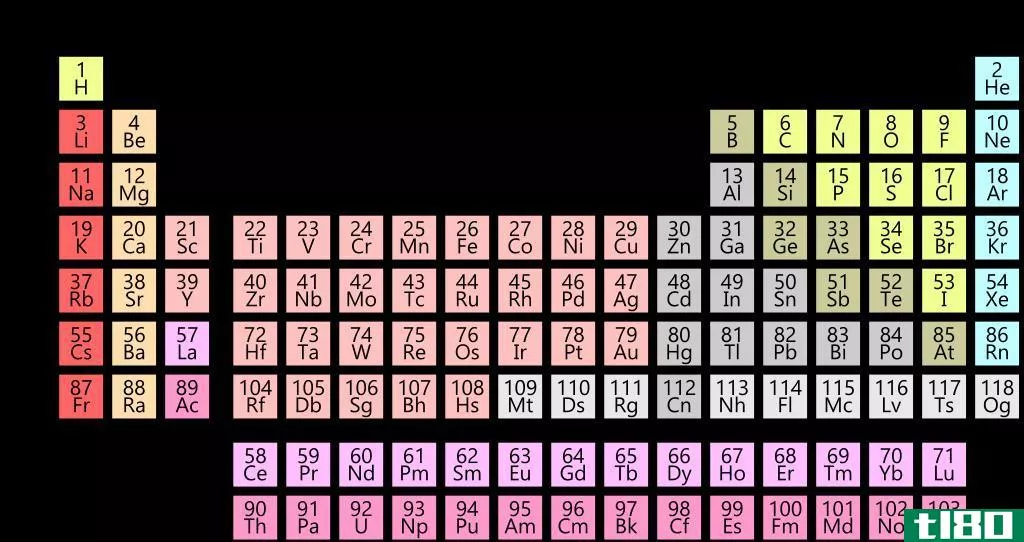
锕系元素与镧系元素的主要区别在于锕系元素填充电子至5f亚轨道,而镧系元素填充电子至4f子轨道。
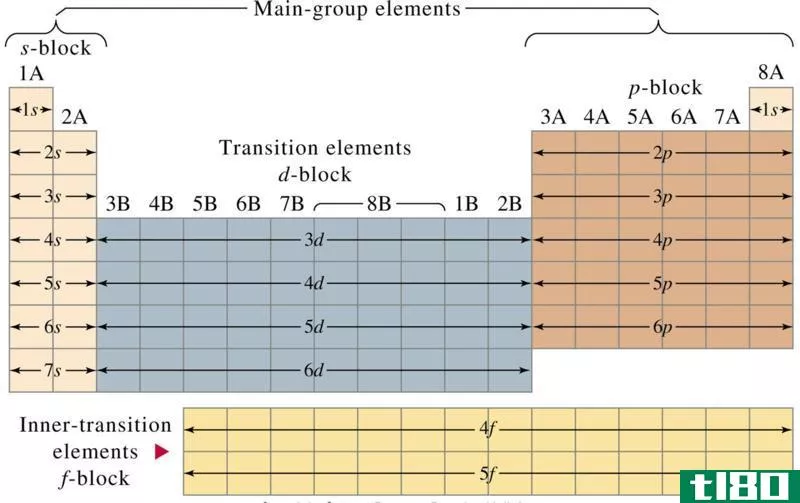
镧系元素和锕系元素在元素周期表中分为两行。因此,两者都属于f块。这是因为它们的最外层电子在f轨道上。因此,我们可以将它们命名为f块元素。
目录
1. 概述和主要区别
2. 什么是锕系元素
3. 什么是镧系元素
4. 并列比较——锕系元素与镧系元素的表格形式
5. 摘要
什么是锕系元素(actinides)?
锕系元素周期表中的一组元素,原子序数从90到103不等。因此,共有14种金属元素,包括:
- 钍钍(Z=90)
- 蛋白Pa(91)
- 铀U(92)
- 镎Np(93)
- 钚钚(94)
- 镅Am(95)
- 铯厘米(96)
- 伯克利乌姆Bk(97)
- 钙Cf(98)
- 爱因斯坦Es(99)
- 费米调频(100)
- 门捷列维医学博士(101)
- a单元Ї102
- Lawrentium Lr(103)。
我们把它们命名为f块元素,因为它们的最后一个电子在f亚轨道上。所有锕系元素都是不稳定的,因此都是放射性的。因为它们是金属,所以具有很强的电正性。此外,它们是致密的金属,并且存在许多同素异形体。这些金属在空气中容易变色,与沸水或稀酸反应释放氢气。
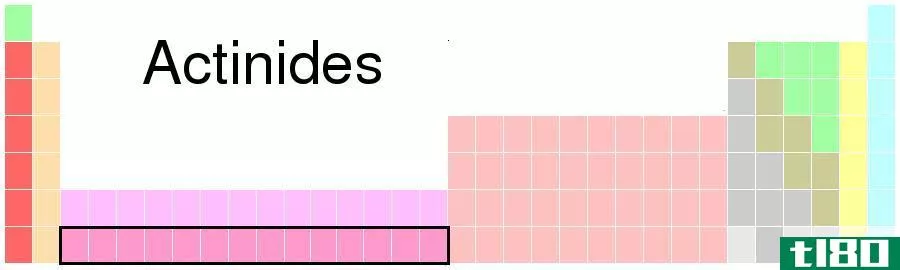
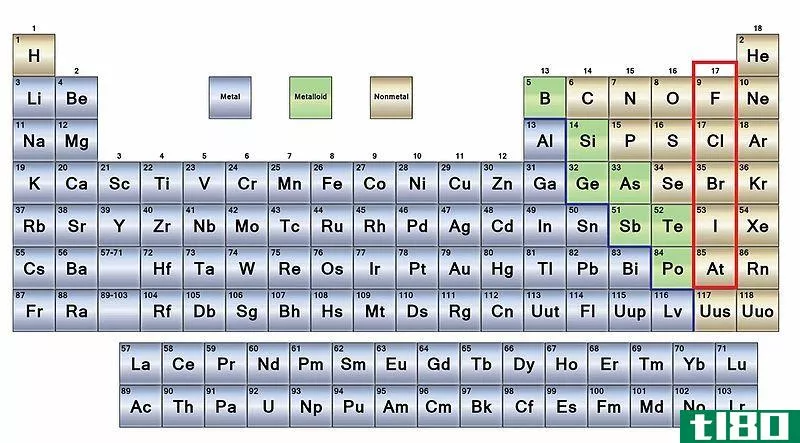
图01:锕系元素在元素周期表中的位置
像其他金属一样,它们也能与非金属元素形成化合物。此外,我们在自然环境中也能找到稀有的锕系元素。例如,在加拿大,铀和钍是以矿床的形式存在的。由于它们的放射性,大多数锕系元素在核能生产中是有用的。我们可以合成锕系元素,将其用于各种用途。除此之外,其中一些还可用于医学、矿物鉴定、中子照相术等。
什么是镧系元素(lanthanides)?
镧系元素的原子序数从57到71不等。有15种金属元素。这些要素包括:
- 镧镧(57)
- 铈铈(58)
- 镨镨(59)
- 钕钕(60)
- 镨Pm(61)
- 钐(62)
- 铕铕(63)
- 钆钆(64)
- 铽Tb(65)
- 镝镝(66)
- 钬(67)
- 钇铒(68)
- 铥Tm(69)
- 镱Yb(70)
- 镥(71)。
它们属于周期表中的f块,因此最终的电子填充到4f亚轨道中。在那里,其他的亚轨道覆盖了4f轨道,镧系元素的化学性质因原子的大小而不同。它们表现出氧化状态。此外,从周期表中一行的左到右,+3镧系离子的尺寸减小,我们称之为镧系收缩。
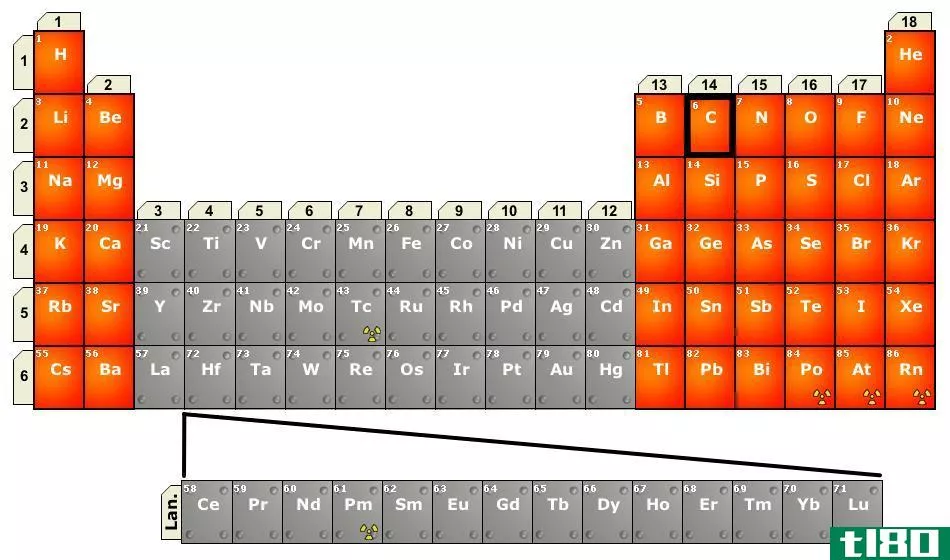
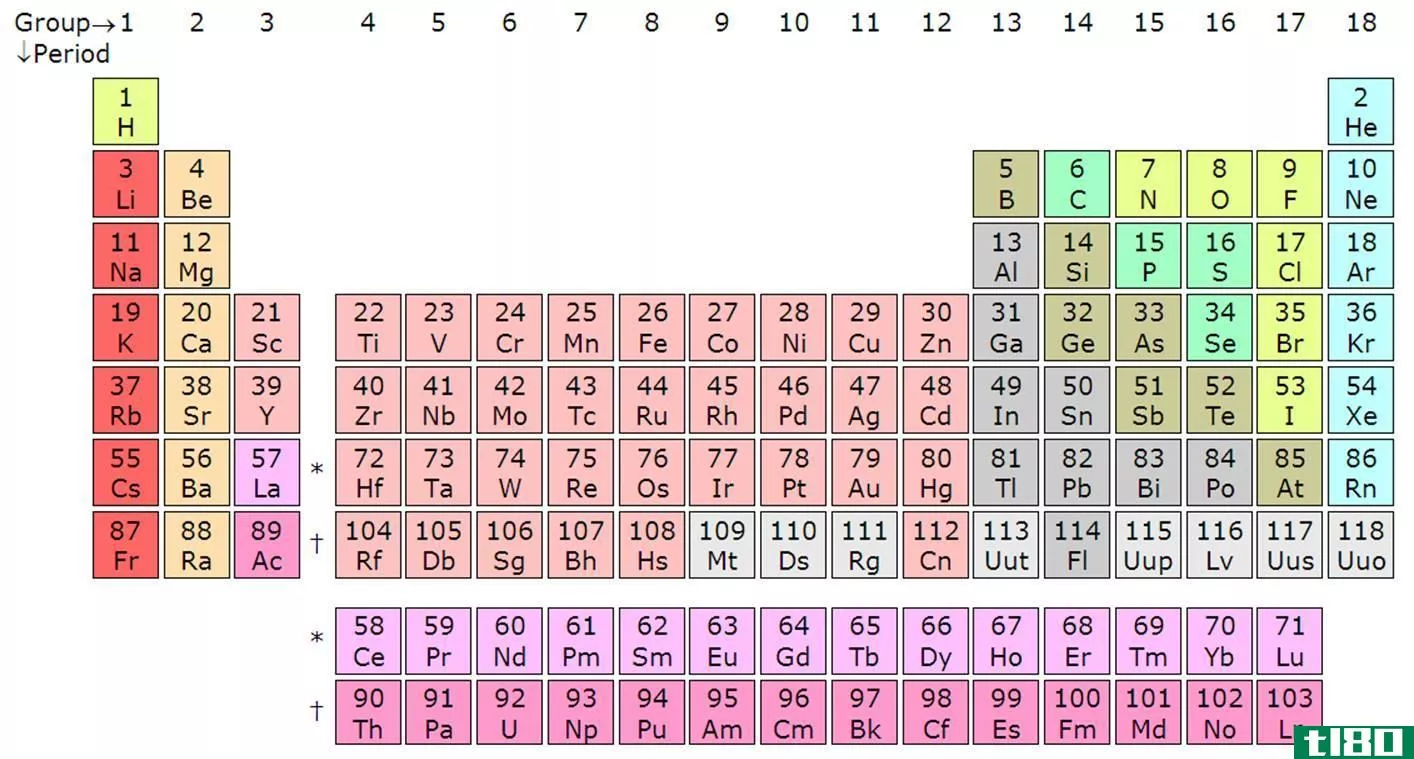
图02:元素周期表中镧系元素的位置
此外,镧系金属呈银色,容易与空气中的氧反应生成氧化物。它们是高活性、相对柔软的金属,熔点和沸点都很高。而且,它们很容易与非金属形成离子化合物。当与稀酸或水反应时,镧系元素产生氢气。
除此之外,这些元素还有未配对的电子(镥除外),这些电子对它们的顺磁性质负责。此外,由于地球表面的低丰度,我们将其命名为稀土金属。虽然它们很少见,但是这些元素有很多用法。因此,它们在玻璃生产、石油等方面可用作催化剂。此外,它们还可用于磁铁、磷光体、灯、超导体、光电应用等。
锕系元素(actinides)和镧系元素(lanthanides)的区别
锕系元素是元素周期表中的一组元素,原子序数在90到103之间,而镧系元素是周期表中的一组元素,原子序数为57到71。锕系元素与镧系元素的主要区别在于锕系元素填充电子至5f亚轨道,而镧系元素填充电子至4f子轨道。此外,所有锕系元素都具有放射性,而镧系元素则不具有放射性(除镨外)。作为锕系元素和镧系元素的另一个区别,我们可以说镧系元素表现出+4的最大氧化状态,而锕系元素则表现出+3、+4、+5、+6和+7氧化状态。
下面的信息图展示了锕系元素和镧系元素之间的比较总结。
总结 - 锕系元素(actinides) vs. 镧系元素(lanthanides)
锕系元素是元素周期表中的一组元素,原子序数在90到103之间,而镧系元素是周期表中的一组元素,原子序数为57到71。因此,它们的主要区别在于它们的电子构型。因此,锕系元素和镧系元素的关键区别在于锕系元素填充电子至5f亚轨道,而镧系元素填充电子至4f子轨道。
引用
1歌词。“镧系元素:性质与反应”,化学图书馆,国家科学基金会,2018年11月26日。这里有2个。歌词。“锕系元素”,化学剧本,国家科学基金会,2018年11月26日。可在这里查阅
2歌词。“锕系元素”,化学剧本,国家科学基金会,2018年11月26日