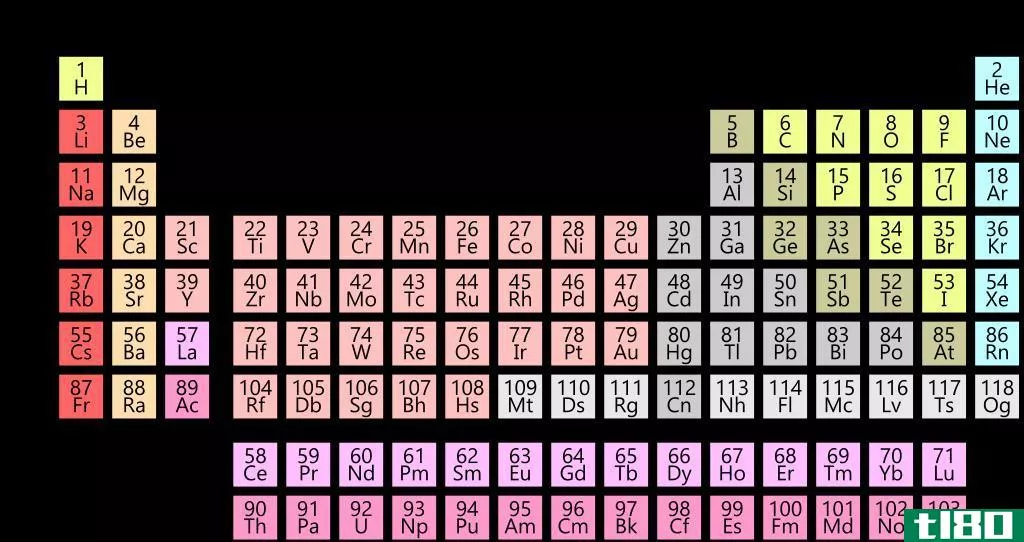
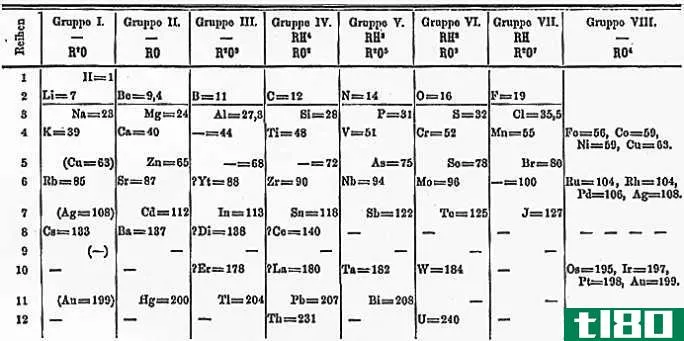
为什么镧系元素和锕系元素在元素周期表上是分开的
镧系元素和锕系元素与元素周期表的其余部分分开,通常在底部显示为单独的行。这种放置的原因与这些元素的电子构型有关。

3b元素组
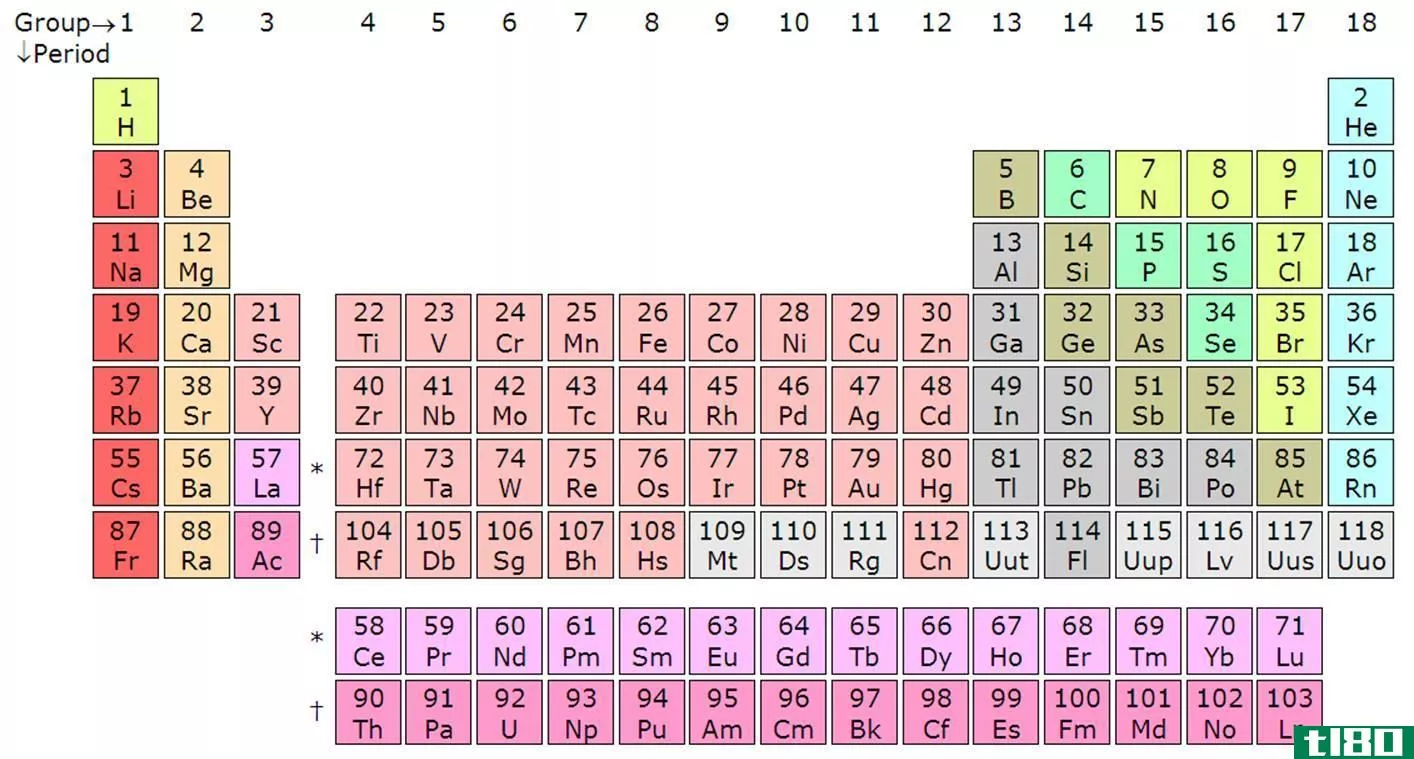
当你看元素周期表时,你会在3B元素组中看到奇怪的条目。3B组标志着过渡金属元素的开始。3B组的第三行包含所有元素57(镧)和元素71(镥)之间的元素。这些元素组合在一起称为镧系元素。类似地,组3B的第四行包含元素89(锕)和元素103(镧)之间的元素。这些元素被称为锕系元素。
第3b组(group 3b)和4b(4b)的区别
为什么所有的镧系元素和锕系元素都属于3B族?要回答这个问题,请查看第3B组和第4B组之间的差异。
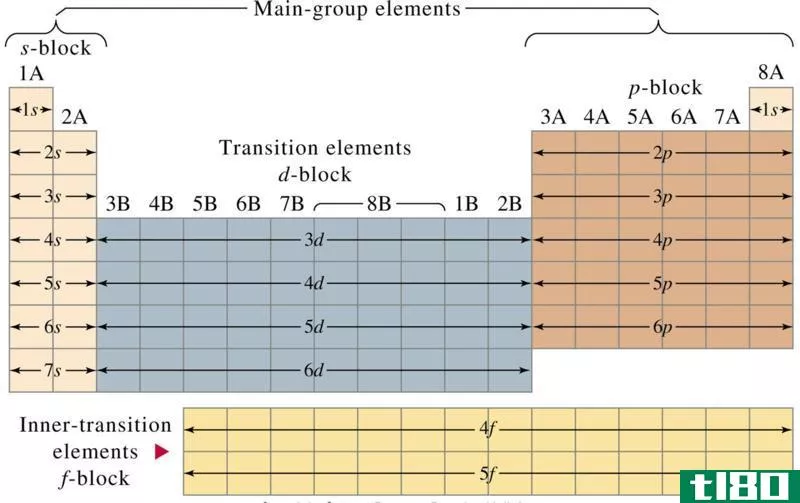
3B元素是第一个开始在其电子配置中填充d壳层电子的元素。4B群是第二个,下一个电子被放置在d2壳层中。
例如,钪是电子组态为[Ar]3d14s2的第一个3B元素。下一个元素是第4B组中的钛,电子构型为[Ar]3d24s2。
电子组态为[Kr]4d15s2的钇和电子组态为[Kr]4d25s2的锆之间也是如此。
第3B族和第4B族之间的区别在于在d壳层上增加了一个电子。
镧与其他3B元素一样具有d1电子,但d2电子直到元素72(铪)才出现。根据前几行中的行为,元素58应填充d2电子,但相反,该电子填充第一个f壳层电子。在第二个5d电子被填满之前,所有的镧系元素都填满了4f电子壳。由于所有镧系元素都含有5d1电子,因此它们属于3B族。
类似地,锕系元素包含一个6d1电子,并在填充6d2电子之前填充5f壳层。所有锕系元素都属于3B族。
镧系元素和锕系元素以符号形式排列在主体单元的下方,而不是为周期表主体中3B族中的所有这些元素腾出空间。由于f壳层电子,这两个元素组也被称为f-块元素。
- 发表于 2021-09-15 10:51
- 阅读 ( 426 )
- 分类:化学
你可能感兴趣的文章
镧系收缩(lanthanide contraction)和锕系收缩(actinide contraction)的区别
...收缩大于镧系收缩。 引用 1“什么是镧系收缩和锕系收缩为什么后者比前者少2kqs5x11化学。”com,可在这里获得。 img.centered,.aligncenter{display:block;margin:0 auto 24px}.gallery-caption,.wp-caption-text{font-size:14px;font-size:1.4rem;font-weight:600;ma...
- 发布于 2020-10-16 20:20
- 阅读 ( 901 )
代表(representative)和过渡元素(transition elements)的区别
关键区别——代表性要素与过渡要素 元素周期表是以原子序数为基础的所有已知化学元素的列表排列。周期表中有行或句点、列或组。元素周期表中有周期性的趋势。周期表中的元素可分为代表元素和过渡元素两类。代表元...
- 发布于 2020-10-19 10:23
- 阅读 ( 761 )
锕系元素(actinides)和镧系元素(lanthanides)的区别
...系元素填充电子至4f子轨道。 镧系元素和锕系元素在元素周期表中分为两行。因此,两者都属于f块。这是因为它们的最外层电子在f轨道上。因此,我们可以将它们命名为f块元素。 目录 1. 概述和主要区别 2. 什么是锕系元素 3. ...
- 发布于 2020-10-26 12:43
- 阅读 ( 401 )
门捷列夫(mendeleev)和现代元素周期表(modern periodic table)的区别
门捷列夫周期表与现代周期表的关键区别在于,现代周期表的基础主要是元素的电子构型,我们称之为原子序数,而在门捷列夫周期表中,它是元素的原子质量。 让我们看看什么是门捷列夫周期表和什么是现代周期表,然后...
- 发布于 2020-11-03 03:51
- 阅读 ( 230 )
镧系元素(lanthanides)和锕系元素(actinides)的区别
...。4f电子构型决定了镧系元素的磁性和光学性质。这就是为什么它可以用于阴极射线管。镧系元素的其他价态构型是四价和二价构型。四价镧系元素是铈、镨和铽。二价镧系元素是钐、铕和镱。 化学性质 镧系元素的区别在于它...
- 发布于 2021-06-24 20:22
- 阅读 ( 365 )
时期(periods)和组(groups)的区别
...段6和7是例外,因为它们总共包含32个元素。这就解释了为什么周期表被缩短了,去掉了周期6和周期7的一部分,并显示在周期表的正下方。如果不除去锕系元素和镧系元素,周期性会很大。这些分离出来的元素是内过渡金属,它...
- 发布于 2021-06-25 20:23
- 阅读 ( 513 )
门捷列夫(mendeleev)和现代周期表(modern periodic table)的区别
... 门捷列夫的主要区别(main difference mendeleev) vs. 现代周期表(modern periodic table) 元素周期表是化学元素按其化学和物理性质排列的表。现代元素周期表是在一系列不同版本的元素周期表之后产生的。俄罗斯化学家/教授德米特...
- 发布于 2021-06-27 12:49
- 阅读 ( 225 )
锕系元素(actinides)和镧系元素(lanthanides)的区别
...tinides) vs. 镧系元素(lanthanides) 锕系元素和镧系元素是元素周期表f区的化学元素。这意味着它们的价电子在原子的f轨道上。这些化学元素以金属形式存在,被称为内过渡金属。f区块仅由镧系和锕系组成。因为锕系元素是从一种叫...
- 发布于 2021-06-29 13:14
- 阅读 ( 525 )
过渡金属(transition metals)和内过渡金属(inner transition metals)的区别
...nce transition metals) vs. 内过渡金属(inner transition metals) 元素周期表由金属、非金属和类金属组成。如果化学元素具有金属性质,如延展性、良好的导电性、易去除电子等,则将其归类为金属。考虑到其电子构型,过渡金属和内部过...
- 发布于 2021-06-29 13:15
- 阅读 ( 616 )
d(d)和f块元素(f block elements)的区别
...部分。所有化学元素都按原子序数递增的顺序排列在元素周期表中。周期表中还有四组元素:s块、p块、d块和f块。元素根据它们的电子构型被分为这些组。例如,s块元素的最外层电子在s轨道上。p块元素在p轨道上有最外层的电...
- 发布于 2021-06-29 23:23
- 阅读 ( 455 )