Pauli不相容原理与Hund规则
在找到原子结构之后,有很多模型来描述电子是如何存在于原子中的。薛定谔提出了原子中有“轨道”的想法。提出了泡利不相容原理和Hund规则来描述原子的轨道和电子。
泡利不相容原理
泡利不相容原理认为一个原子中的两个电子不可能拥有相同的四个量子数。原子的轨道用三个量子数来描述。它们是主量子数(n)、角动量/方位量子数(l)和磁量子数(ml)。由此,主量子数定义了一个壳层。它可以是任何整数值。这与周期表中相关原子的周期相似。角动量量子数可以有0,1,2,3到n-1的值。子壳层的数量取决于这个量子数。我决定了轨道的形状。例如,如果l=o,那么轨道是s,对于p轨道,l=1,对于d轨道l=2,对于f轨道l=3。磁量子数决定了等效能量轨道的数目。换句话说,我们称这些简并轨道。ml的值可以是-l到+l。除了这三个量子数之外,还有另一个量子数定义了电子。这被称为电子自旋量子数(ms),其值为+1/2和-1/2。所以,要确定原子中电子的状态,我们需要指定所有四个量子数。电子位于原子轨道上,一个轨道上只能有两个电子。此外,这两个电子的自旋相反。因此,Pauli不相容原理中所说的是正确的。例如,我们取两个3p能级的电子。两个电子的主量子数都是3。l是1,因为电子位于p轨道上。ml是-1,0和+1。因此,存在3p退化轨道。所有这些数值对于我们正在考虑的两个电子都是相同的。但由于这两个电子位于同一轨道上,它们的自旋方向相反。因此,自旋量子数是不同的(一个是+1/2,另一个是-1/2)。
亨德法则
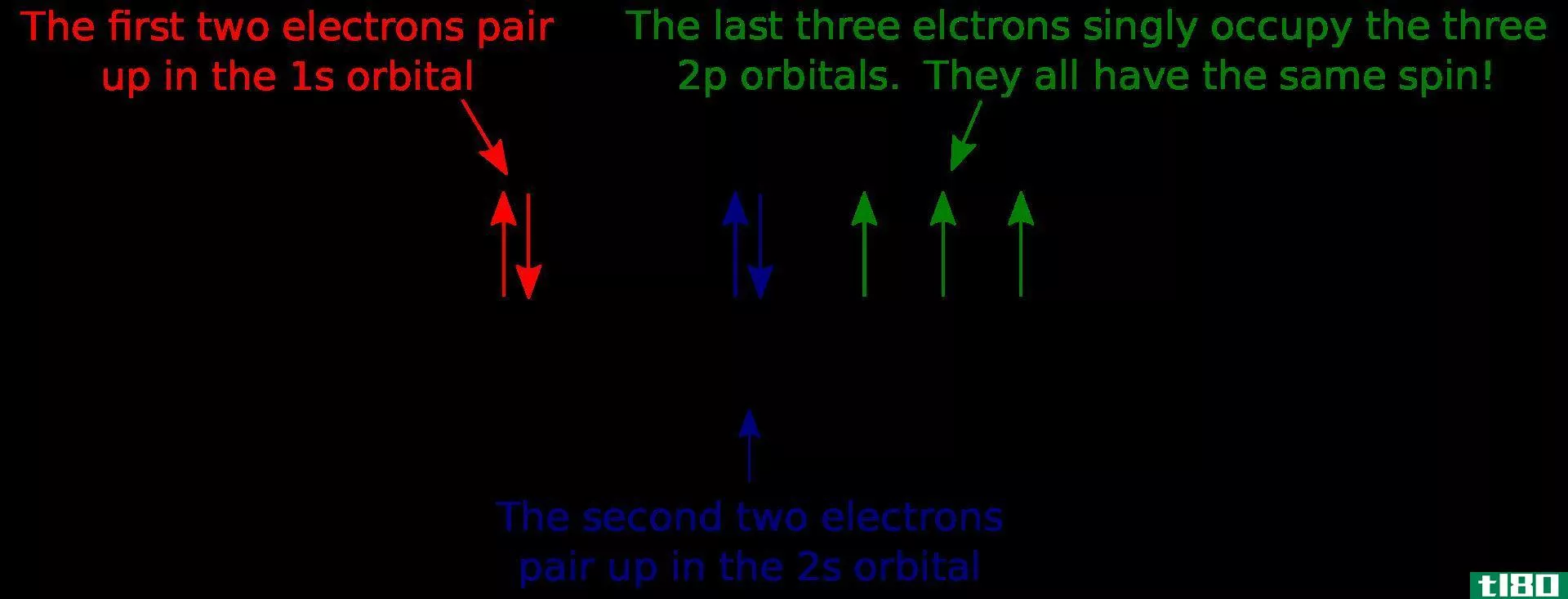
Hund规则可以描述如下。
电子在亚壳层(简并轨道)中最稳定的排列是平行自旋数最多的排列。它们具有最大的多样性。”
根据这一点,每个子壳层在被另一个电子加倍填充之前,都会填充一个平行自旋的电子。由于这种填充模式,电子与原子核之间的屏蔽作用较小;因此,它们具有最高的电子-核相互作用。
| Pauli不相容原理和Hund规则有什么区别?•泡利不相容原理是关于原子的量子数。Hund规则是关于电子如何填充到原子轨道上的。•泡利不相容原理说每个轨道只有两个电子。亨德定律说,只有在每个轨道上填充一个电子后,才会发生电子配对。•泡利排除原理描述了相同轨道上的电子如何具有相反的自旋。这可以用来解释匈奴规则。 |