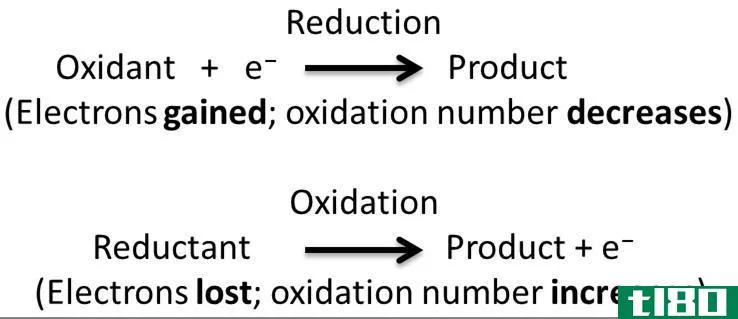
氧化反应vs还原反应
氧化和还原反应是相互关联的。当一种物质被氧化时,另一种物质就会减少。因此,这些反应统称为氧化还原反应。
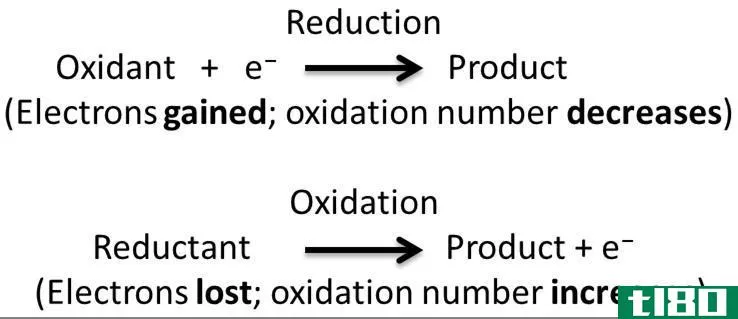
氧化反应
氧化反应最初被认为是氧气参与的反应。在这里,氧与另一个分子结合产生氧化物。在这个反应中,氧经历还原,另一种物质氧化。因此,氧化反应基本上就是向另一种物质中加入氧气。例如,在下面的反应中,氢经过氧化,因此,氧原子被添加到制氢水中。
2H2+O2->;2H2O
另一种描述氧化的方法是氢的损失。有些情况下,很难用加氧来描述氧化。例如,在下面的反应中,氧加入了碳和氢,但只有碳经历了氧化。在这种情况下,氧化可以用氢的损失来描述。当产生二氧化碳时,甲烷中的氢被除去,那里的碳被氧化了。
CH4+2O2->;CO2+2H2O
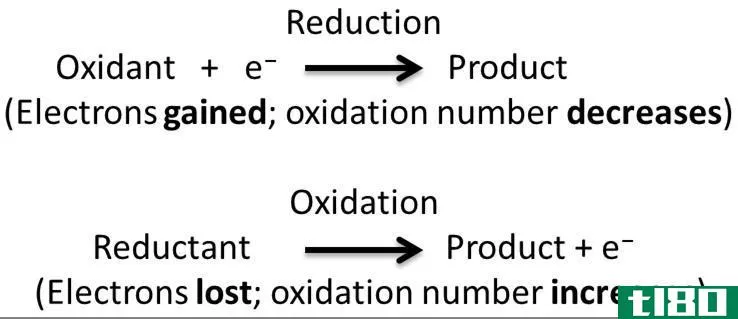
另一种描述氧化的方法是失去电子。这种方法可以用来解释化学反应,在那里我们看不到氧化物的形成或氢的损失。所以,即使没有氧气,我们也可以用这种方法来解释氧化。例如在下面的反应中,镁已经转化成镁离子。因为,镁失去了两个电子,它经历了氧化,氯气是氧化剂。
Mg+Cl2->;Mg2++2Cl–
氧化状态有助于识别氧化过的原子。根据IUPAC的定义,氧化状态是“物质中原子氧化程度的量度。氧化态是一个整数值,可以是正、负或零。化学反应使原子的氧化状态发生变化。如果氧化态增加,则称原子被氧化。在上述反应中,镁为零氧化态,镁离子为+2氧化态。由于氧化数增加,镁被氧化了。
还原反应
还原与氧化相反。就氧转移而言,在还原反应中,氧会丢失。在氢转移方面,还原反应发生在获得氢气时。例如,在上面的例子中,在甲烷和氧气之间,氧气减少了,因为它得到了氢气。就电子转移而言,还原就是获得电子。所以根据上面的例子,氯被还原了。
| 氧化反应和还原反应有什么区别?•在氧化反应中,得到了氧,在还原反应中,氧丢失了。•氧化过程中,氢损失了,但在还原过程中,氢得到了。•在氧化反应中,电子丢失,但在还原反应中,获得了电子。•在氧化反应中,氧化状态增加。被还原的物种降低了它们的氧化状态。 |