稀释和浓缩的关键区别在于,稀释是指添加更多的溶剂,而浓度是指溶剂的去除。
稀释和浓度的概念在化学溶液的研究中是非常重要的。因此,溶剂中溶质的量决定了溶液的性质,并且这个量保持不变;我们可以通过添加溶剂并从溶液中除去一些溶剂,使溶液“稀释”或“浓缩”。因此,在化学分析中,我们需要改变溶液的浓度,通常在不同的应用中。
目录
1. 概述和主要区别
2. 什么是稀释
3.什么是专注
4. 并列比较-稀释度与浓度的表格形式
5. 摘要
什么是稀释(dilution)?
稀释是通过添加更多溶剂来降低溶液中溶质浓度的过程。因此,我们可以减少单位体积溶液中存在的溶质量。如果我们提到“稀释”,它的意思是“添加更多的溶剂而不添加溶质”。但是,在加入溶剂后,我们应该彻底混合溶液,以获得均匀的溶液。
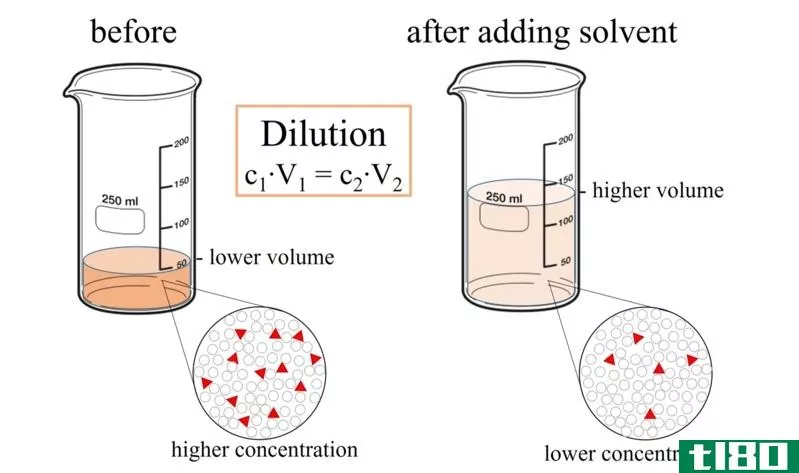
图01:稀释过程
根据下式,我们可以确定稀释后溶液的最终浓度。
C1V1=C2V2
式中:C1为初始浓度,V1为溶液初始体积,C2为稀释后浓度,V2为溶液最终浓度。例如,如果我们在95毫升NaCl水溶液(1摩尔/升)中加入5毫升水,则稀释得到0.95摩尔/升的溶液。因此浓度降低。
什么是浓度(concentration)?
浓缩是增加溶液中溶质浓度的过程。换句话说,它要么减少溶剂的量,要么增加溶质的量。因此,这是增加单位体积溶液中存在的溶质量的过程。

图02:浓缩过程使溶液变暗`
浓溶液比稀溶液含有大量的溶质。我们可以用上面给出的相同方程式(在副标题“稀释”下)确定溶液浓缩后的浓度。
稀释(dilution)和浓度(concentration)的区别
在稀释过程中,溶液浓度的增加是溶液浓度增加的过程。因此,稀释和浓缩的关键区别在于,稀释是指添加更多的溶剂,而浓度是指溶剂的去除。我们可以通过添加更多溶剂或除去溶质来稀释溶液,而浓缩过程既包括添加更多溶质,也包括去除溶剂。
下面的信息图提供了稀释和浓度之间差异的详细信息。

总结 - 稀释(dilution) vs. 浓度(concentration)
在化学中,稀释和浓缩对于制备所需浓度的溶液非常重要。此外,这些稀释和浓缩过程在分析化学中非常重要。稀释和浓缩的关键区别在于,稀释是指添加更多的溶剂,而浓度是指溶剂的去除。
引用
1“稀释(等式)”,维基百科,维基媒体基金会,2018年9月22日。此处提供