主要区别
理想溶液与非理想溶液的主要区别在于,理想溶液中所有分子之间的分子间连接是相同的,而非理想溶液中溶质分子和溶剂分子之间的分子连接是不同的。
理想溶液(ideal solution) vs. 非理想溶液(non ideal solution)
理想溶液中所有组分分子之间存在相同的联系,而非理想溶液中存在溶质-溶质、溶剂-溶质和溶剂-溶剂关系。
理想溶液在各种吸收条件下通常都遵循拉乌尔定律;相反,非理想溶液通常不服从拉乌尔定律。当溶液溶解在理想溶液中时,热量既不被吸收也不放出;另一方面,热在非理想溶液中被吸收或放出。
理想溶液的各种实例为溴乙烷和氯乙烷、苯和甲苯、正己烷和正庚烷、氯苯和溴苯、四氯化碳和四氯化碳、正丁基氯和正丁基溴、溴化乙基和碘乙基。一些非理想溶液的例子是甲醇和水、丙酮和乙醇、丙酮和二硫化碳、氯仿和苯、硝酸和水、盐酸和水。
比较图
什么是理想溶液(the ideal solution)?
理想溶液通常在各种吸收率,所有温度和浓度下都遵循拉乌尔定律。理想溶液是所有溶液中所有分子之间接触相同的溶液,即为理想溶液。理想溶液可以通过混合两种理想溶液得到,这两种溶液是具有相似结构和分子尺寸的溶剂和溶质。
在理想溶液中,溶液的分子组分之间通常不存在净力。所以,溶质分子之间的相对距离即使在溶剂混合后也不会改变。因为要改变溶液分子之间的距离,必须存在一个作用在分子上的净力。
当理想溶液过程为零或几乎为零时,焓发生变化,这意味着焓变为零。当溶液溶解在理想溶液中时,热量既不会被吸收也不会放出。认为理想溶液在现实中是存在的,如苯-甲苯、苯-苯、甲苯之间的相互关系基本相同。
示例
理想溶液的各种实例有溴乙烷和氯乙烷、苯和甲苯、正己烷和正庚烷、氯苯和溴苯。
什么是非理想溶液(non ideal solution)?
非理想溶液在各种吸收率、所有温度和浓度下通常不服从拉乌尔定律。非理想解之所以称为非理想解,是因为它们偏离了理想解。
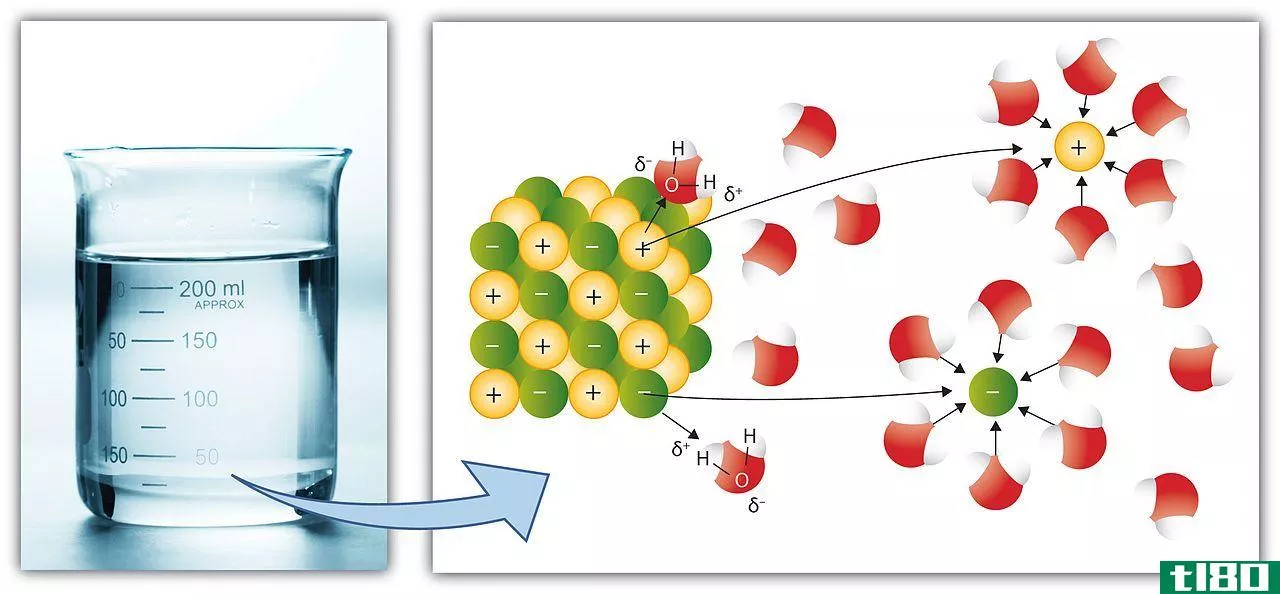
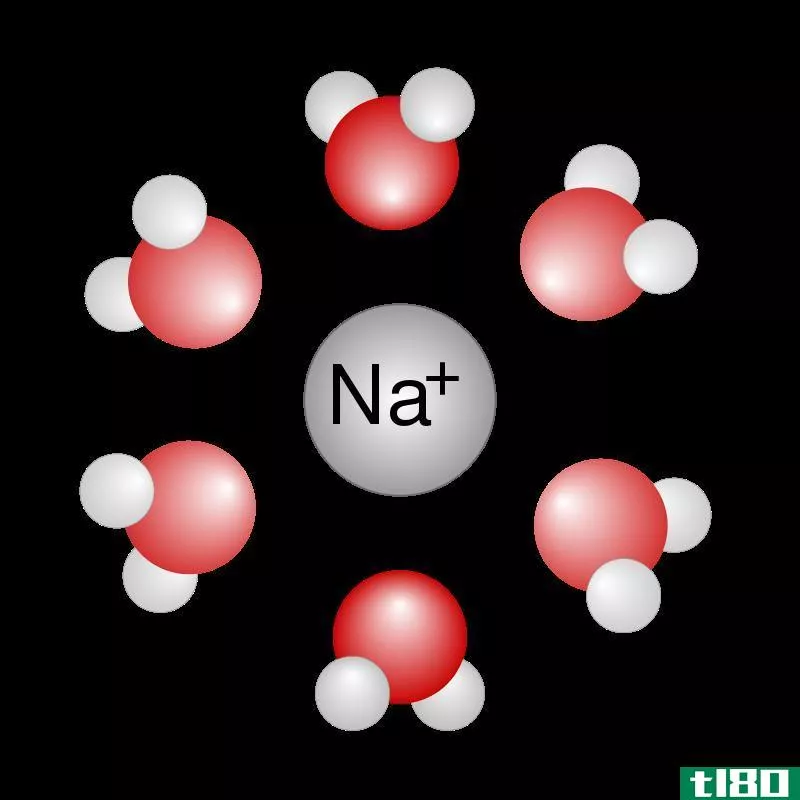
它是一种溶液,在不同组分的所有分子之间的相互关系上有差别。非理想溶液中存在溶质-溶质、溶剂-溶质和溶剂-溶剂关系。化学高度浓缩的溶液可以表现为非理想溶液,因为浓缩溶液通常表现出溶液的非理想行为。
当非理想溶液过程为正或负时,焓发生变化。热是在非理想溶液中吸收或放出的。发现了两种非理想解:正偏离拉乌尔定律和负偏离拉乌尔定律。
示例
一些非理想溶液的例子是甲醇和水、丙酮和乙醇、丙酮和二硫化碳、氯仿和苯、硝酸和水。
主要区别
- 在理想溶液中,所有分子之间存在相等的缔合关系,而在非理想溶液中,存在溶质溶质、溶剂溶质和溶剂溶剂之间的关系。
- 焓的变化发生在理想溶液过程为零或接近零时,而焓的变化发生在非理想溶液法为正或负时。
- 高稀溶液可以作为理想溶液,而高浓度溶液可以作为非理想溶液。
- 理想解通常持续遵循拉乌尔定律;相反,非理想解通常不遵循拉乌尔定律。
- 热既不在理想溶液中吸收,也不在理想溶液中析出;另一方面,热在非理想溶液中吸收或放出。
- 溴乙烷和氯乙烷、苯和甲苯、正己烷和正庚烷、氯苯和溴苯、四氯化碳和四氯化碳、溴化乙基和碘化乙酯是各种理想溶液的例子;另一方面,甲醇和水、丙酮和乙醇、丙酮和二硫化碳、氯仿和苯、硝酸和水,盐酸和水是非理想溶液的一些例子。
结论
通过以上讨论得出,理想溶液一般服从拉乌尔定律,所有分子之间的分子间连接是相同的,而非理想溶液通常不服从拉乌尔定律,溶质分子和溶剂分子之间存在不同的分子联系。