查尔斯定律的例子问题
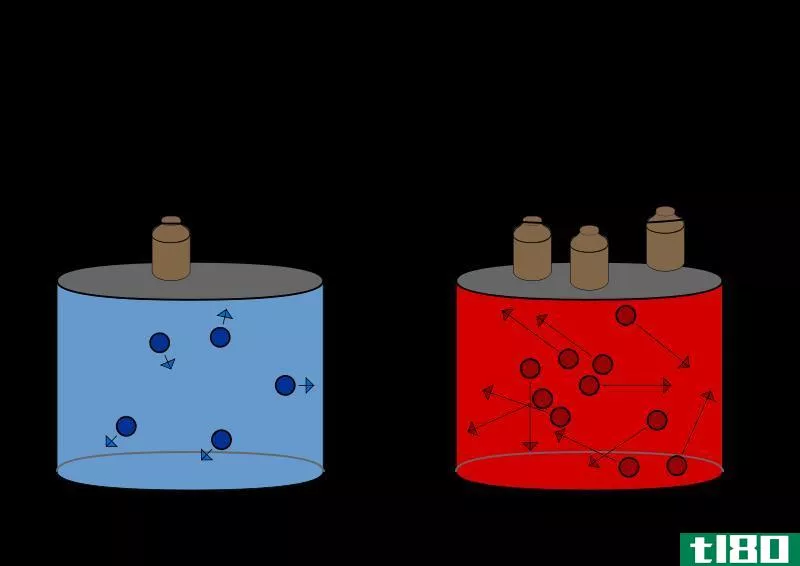
查尔斯定律是理想气体定律的一个特例,其中气体的压力是恒定的。查尔斯定律指出,体积与恒压下气体的绝对温度成正比。只要气体的压力和数量不变,气体的温度加倍,其体积就会加倍。

查尔斯定律的例子问题
该示例问题显示了如何使用查尔斯定律解决气体定律问题:在恒定压力下将600 mL氮气样品从27°C加热到77°C。最后一卷是什么?
解决方案:
解决气体定律问题的第一步应该是将所有温度转换为绝对温度。换句话说,如果温度以摄氏度或华氏度为单位,则将其转换为开尔文。(这是这类作业中最常见的错误。)
Tk=273+°CTi=初始温度=27°CTi K=273+27Ti K=300 KTf=最终温度=77°CTf K=273+77Tf K=350 K
下一步是使用查尔斯定律找到最终的卷。查尔斯定律的表述如下:
Vi/Ti=Vf/Tf,其中Vi和Ti是初始体积和温度Vf,Tf是最终体积和温度Vf:Vf=vtf/t求出Vf的方程,输入已知值并求解Vf。Vf=(600 mL)(350 K)/(300 K)Vf=700 mL答:加热后的最终体积为700 mL。
查尔斯定律的更多例子
如果你认为查尔斯定律似乎与现实生活无关,那就再想想吧!通过了解该定律的基本知识,你将知道在各种现实情况下会发生什么,一旦你知道如何使用查尔斯定律解决问题,你就可以做出预测,甚至开始计划新的发明。以下是查尔斯定律发挥作用的几个例子:
- 如果你在寒冷的天气带篮球出去,球会随着温度的降低而收缩。这也适用于任何充气物体,并解释了为什么在温度下降时检查汽车轮胎压力是一个好主意。
- 如果你在炎热的天气给游泳池浮子充气过度,它会在阳光下膨胀并破裂。
- 弹出式火鸡温度计是根据查尔斯定律工作的。火鸡烹饪时,温度计内的气体膨胀,直到它能“弹出”柱塞。
其他气体定律的例子
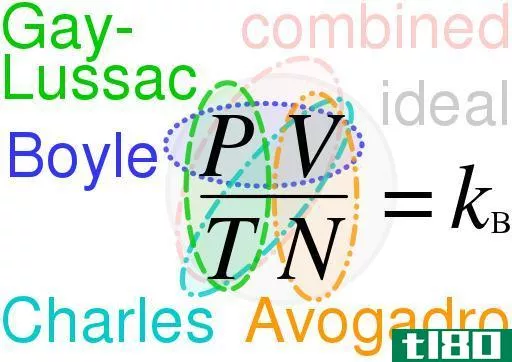
查尔斯定律只是你们可能遇到的理想气体定律的特例之一。每项法律都以制定者的名字命名。知道如何区分气体定律并能举出每个定律的例子是很好的。
- 阿蒙顿定律:在体积和质量不变的情况下,温度加倍,压力加倍。当你开车时,汽车轮胎受热,它们的压力就会增加。
- 波义耳定律:在恒定温度和质量下,压力加倍,体积减半。示例:当你在水下吹泡泡时,泡泡上升到水面时会膨胀。
- 阿伏伽德罗定律:在恒定温度和压力下,气体的质量或摩尔数加倍,体积加倍。例:吸入使肺部充满空气,使其容积增大。
- 发表于 2021-09-15 12:47
- 阅读 ( 343 )
- 分类:化学
你可能感兴趣的文章
理想气体定律(ideal gas law)和范德瓦尔斯方程(van der waals equation)的区别
关键区别——理想气体定律与范德瓦尔斯方程 理想气体定律是一个基本定律,而范德瓦尔斯方程是理想气体定律的修正版本。理想气体定律与范德瓦尔斯方程的主要区别在于,理想气体定律方程适用于理想气体,而范德瓦尔...
- 发布于 2020-10-19 04:40
- 阅读 ( 763 )
混合气体定律(combined gas law)和理想气体定律(ideal gas law)的区别
...正。组合气体定律是三种气体定律的组合:博伊尔定律、查尔斯定律和盖伊·卢萨克定律。组合气体定律与理想气体定律的主要区别在于,组合气体定律是三种气体定律的集合,而理想气体定律是单个气体定律的集合。 目录 1. ...
- 发布于 2020-10-19 04:51
- 阅读 ( 622 )
理想气体定律(ideal gas law)和真实气体定律(real gas law)的区别
...。此外,这项法律是其他几项法律的结合: 波义耳定律 查尔斯定律 阿伏加德罗定律 盖卢萨克定律 计算 基本上,我们可以给出理想气体定律如下:; PV=nRT 式中,P为压力,V为体积,T为理想气体的温度。这里,“n”是理想气...
- 发布于 2020-10-20 21:30
- 阅读 ( 865 )
gay-lussac气体定律示例
盖伊·卢萨克气体定律是理想气体定律的一个特例,其中气体的体积保持不变。当体积保持恒定时,气体施加的压力与气体的绝对温度成正比。简单来说,假设体积不变,提高气体温度会增加其压力,而降低温度会降低压力。这...
- 发布于 2021-09-06 23:15
- 阅读 ( 296 )
常见的一般化学问题列表
...热法和热流法 碳-14年代测定 摄氏度到开尔文温度的转换 查尔斯气体定律 克劳修斯-克拉佩龙方程 浓度和摩尔浓度根据已知质量的溶质确定浓度 配制储备溶液的浓度和摩尔浓度 浓度和摩尔浓度-测定水溶液中离子的浓度 共价键...
- 发布于 2021-09-08 10:26
- 阅读 ( 255 )
化学101-主题介绍和索引
...殊的性质。 理想气体简介 理想气体定律 波义耳定律 查尔斯定律 道尔顿分压定律 酸类及;基地 酸和碱与水溶液中氢离子或质子的作用有关。 酸碱定义 常见酸碱 酸碱强度 计算pH值 pH标度 负pH值 缓冲区 成盐 Henderson-Hasse...
- 发布于 2021-09-15 11:49
- 阅读 ( 287 )
化学的主要规律
...,受限气体的体积与气体承受的压力成反比: PV = k 查尔斯定律在恒定压力下,受限气体的体积与绝对温度成正比,单位为开尔文: V = kT 结合体积比盖伊·卢萨克定律更重要。 节约能源既不能创造也不能破坏能源;宇...
- 发布于 2021-09-15 12:45
- 阅读 ( 183 )
气体研究指南
...终压力,压力降低或随着体积减小,压力将升高。 查尔斯气体定律 查尔斯定律指出,当压力保持恒定时,气体的体积与其绝对温度成正比。V=kt其中V=volumek=constantT=绝对温度查尔斯定律也可以表示为Vi/Ti=Vf/Ti,其中Vi和Vf是...
- 发布于 2021-09-15 12:46
- 阅读 ( 229 )
高中化学课程概述
...殊的性质。 理想气体 理想气体定律问题 波义耳定律 查尔斯定律 道尔顿分压定律 酸碱 酸和碱与水溶液中氢离子或质子的作用有关。 酸碱定义 常见酸碱 酸碱强度 计算pH值 缓冲区 成盐 Henderson-Hasselbalch方程 滴定基础 滴...
- 发布于 2021-09-15 17:41
- 阅读 ( 267 )