3种分子间作用力
分子间作用力或IMF是分子间的物理作用力。相反,分子内作用力是单个分子中原子之间的作用力。分子间作用力比分子内作用力弱。


关键收获:分子间作用力
- 分子间作用力作用于分子之间。相反,分子内的力作用于分子内部。
- 分子间作用力比分子内作用力弱。
- 分子间作用力的例子包括伦敦色散力、偶极-偶极相互作用、离子-偶极相互作用和范德华力。
分子如何相互作用
分子间作用力之间的相互作用可以用来描述分子之间如何相互作用。分子间作用力的强弱决定了物质的状态(如固体、液体、气体)和某些化学性质(如熔点、结构)。
分子间作用力有三种主要类型:伦敦色散力、偶极-偶极相互作用和离子-偶极相互作用。下面我们将详细介绍这三种分子间作用力,以及每种类型的示例。
伦敦分散部队
伦敦色散力也称为LDF、伦敦力、色散力、瞬时偶极力、诱导偶极力或诱导偶极诱导偶极力
伦敦色散力,即两个非极性分子之间的力,是分子间作用力中最弱的。一个分子的电子被另一个分子的原子核吸引,而被另一个分子的电子排斥。当分子的电子云被吸引和排斥的静电力扭曲时,就会产生偶极子。
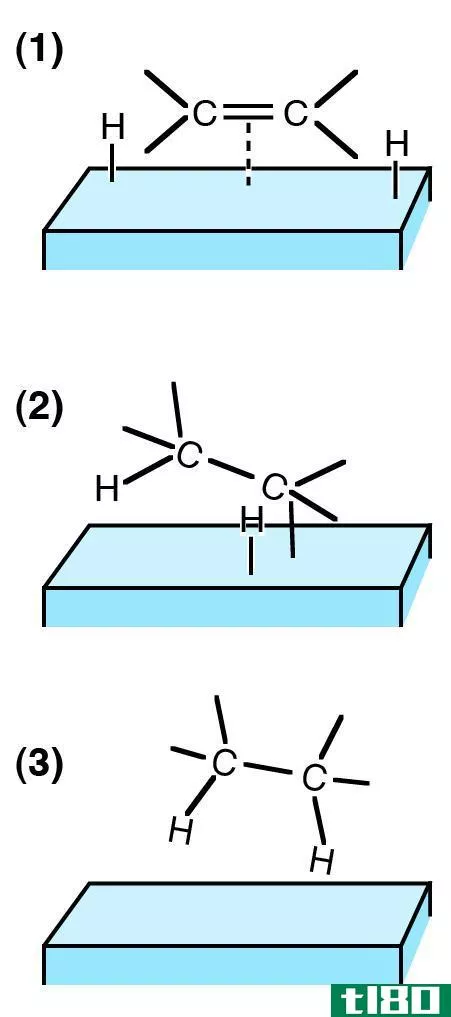
示例:伦敦分散力的一个示例是两个甲基(-CH3)基团之间的相互作用。
示例:伦敦色散力的第二个示例是氮气(N2)和氧气(O2)分子之间的相互作用。原子的电子不仅被吸引到自己的原子核上,而且也被吸引到其他原子核中的质子上。
偶极-偶极相互作用
当两个极性分子彼此靠近时,就会发生偶极-偶极相互作用。一个分子的正电荷部分被另一个分子的负电荷部分吸引。由于许多分子是极性的,这是一种常见的分子间作用力。
例子:偶极-偶极相互作用的一个例子是两个二氧化硫(SO2)分子之间的相互作用,其中一个分子的硫原子被另一个分子的氧原子吸引。
例:H氢键被认为是偶极-偶极相互作用的一个具体例子,它总是涉及氢。一个分子的氢原子被另一个分子的电负性原子吸引,例如水中的氧原子。
离子偶极相互作用
离子与极性分子发生偶极相互作用。在这种情况下,离子的电荷决定了分子的哪个部分吸引,哪个部分排斥。阳离子或正离子会被分子的负部分吸引,并被正部分排斥。阴离子或负离子会被分子的正部分吸引,并被负部分排斥。
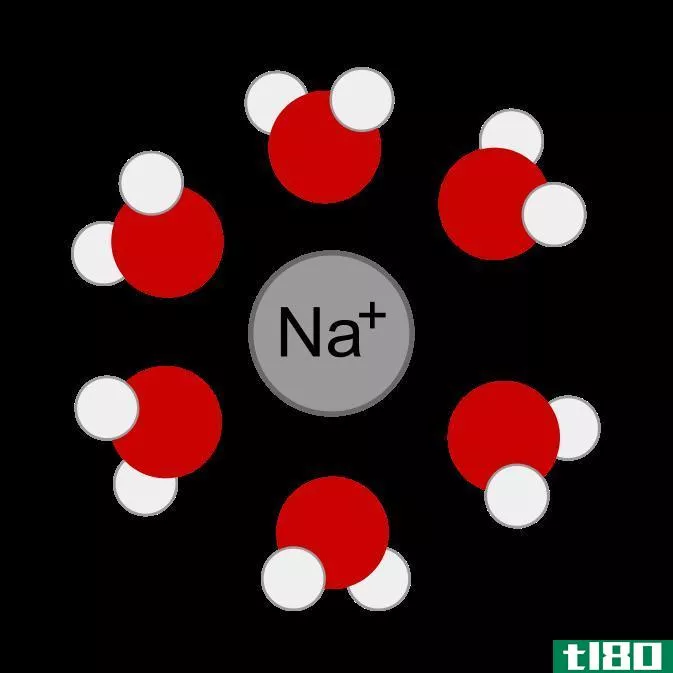
示例:离子偶极相互作用的一个示例是钠离子和水(H2O)之间的相互作用,其中钠离子和氧原子相互吸引,而钠和氢相互排斥。
范德瓦尔斯力
范德华力是不带电原子或分子之间的相互作用。这些力被用来解释物体之间的普遍吸引力、气体的物理吸附和凝聚相的内聚。范德瓦尔斯力包括分子间力以及一些分子内力,包括Keesom相互作用、德拜力和伦敦色散力。
来源
- Ege,Seyhan(2003年)。有机化学:结构与反应性。霍顿·米夫林学院。ISBN 0618318097。第30-33、67页。
- Majer诉和Svoboda诉(1985年)。有机化合物的蒸发焓。布莱克威尔科学出版社。牛津。ISBN 0632015292。
- Margenau,H.和Kestner,N.(1969年)。分子间作用力理论。国际自然哲学专著系列。佩加蒙出版社,ISBN 1483119289。
- 发表于 2021-10-14 04:56
- 阅读 ( 200 )
- 分类:数学
你可能感兴趣的文章
凝聚(cohesion)和表面张力(surface tension)的区别
...内聚力和表面张力的关键区别在于,内聚力描述的是相同分子之间发生的分子间作用力,而表面张力则描述液体表面的弹性。 表面张力是液体的一种性质,它是由相同液体分子之间的内聚力引起的。凝聚力可以描述为相似分子...
- 发布于 2020-09-24 01:41
- 阅读 ( 560 )
化学吸附(chemisorption)和物理吸附(physisorption)的区别
...学键固定,而物理吸附是一种吸附,其中被吸附的物质由分子间的作用力保持。 化学吸附和物理吸附是描述物质在表面吸附机理的重要化学概念。化学吸附是化学吸附,物理吸附是物理吸附。 目录 1. 概述和主要区别 2. 什么是...
- 发布于 2020-10-16 18:34
- 阅读 ( 460 )
离子偶极(ion dipole)和偶极-偶极力(dipole dipole forces)的区别
关键区别-离子偶极与偶极-偶极力 分子间作用力是不同分子之间存在的吸引力。离子偶极力和偶极-偶极力是分子间作用力的两种形式。其他一些分子间力的例子包括离子诱导的偶极力、氢键和范德华力。这些力是静电吸引,...
- 发布于 2020-10-19 06:14
- 阅读 ( 3173 )
胶粘剂(adhesive)和凝聚力(cohesive forces)的区别
...内聚力 附着力使不同的表面互相吸引。粘着力可以是使分子粘在一起的机械力,也可以是存在于正负电荷之间的静电力。相似表面之间存在凝聚力。因此,这些力导致类似分子团的形成。内聚力可以是氢键或范德华力。氢键发...
- 发布于 2020-10-21 07:05
- 阅读 ( 562 )
液态(liquid state)和气态(gaseous state)的区别
液态和气态之间的关键区别在于,与气态相比,液态分子间的分子间作用力更强。事实上,气态分子间的作用力较小或没有。 物质有三种主要状态或相,即气相、液相和固相。物质的这些状态在外观、物理性质和化学性质等...
- 发布于 2020-10-23 18:53
- 阅读 ( 468 )
粘附(adhesion)和凝聚(cohesion)的区别
... 粘着和粘聚力的关键区别在于,粘着是不相似的物质或分子之间的吸引力,而凝聚力是相似的分子或物质之间的吸引力。 有许多现象可以解释我们在日常生活中观察到的事情。虽然有时我们不关注这些小细节,但它们是帮助...
- 发布于 2020-11-04 17:17
- 阅读 ( 1108 )
独联体(cis)和反式(trans)的区别
...顺式和反式异构体的物理性质不同,这是由于总偶极矩和分子形状的不平等造成的。 相对沸点由极性决定。它引起分子间作用力增加,从而导致沸点升高。顺式异构体比反式异构体具有更高的沸点。差别可能很小,例如在直链...
- 发布于 2021-06-25 06:33
- 阅读 ( 323 )
蒸发(evaporation)和汽化(vaporization)的区别
...到沸点时发生的汽化。 什么是蒸发(evaporation)? 液体中的分子有一系列的动能。在蒸发过程中,液体表面的分子有足够的动能来克服水分子之间的分子间作用力,这些分子从液体表面逸出成为气体。其中一些分子最终可能与液体...
- 发布于 2021-06-27 03:25
- 阅读 ( 286 )
摩擦(friction)和粘度(viscosity)的区别
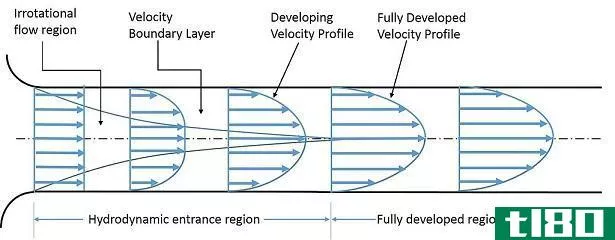
...么是粘度(viscosity)? 粘度是指流体中试图抵抗流体运动的分子间作用力。我们可以认为流体是由“层”构成的。当流体流动时,不同层中的分子以不同的速度运动。考虑流体通过圆形管道。在管道的内边缘,有一个流动非常缓慢...
- 发布于 2021-06-27 07:00
- 阅读 ( 192 )
表面张力(surface tension)和表面能(surface energy)的区别
...区别-表面张力与表面能 表面张力和表面能是组成材料的分子间作用力的测量值。由于这些分子间的作用力,液体表面总是被向内拉。如果要拉伸表面,就必须克服分子间的作用力。液体表面的张力和拉伸该表面所需的功可以测...
- 发布于 2021-06-27 09:24
- 阅读 ( 962 )