根据反应热计算熵的变化
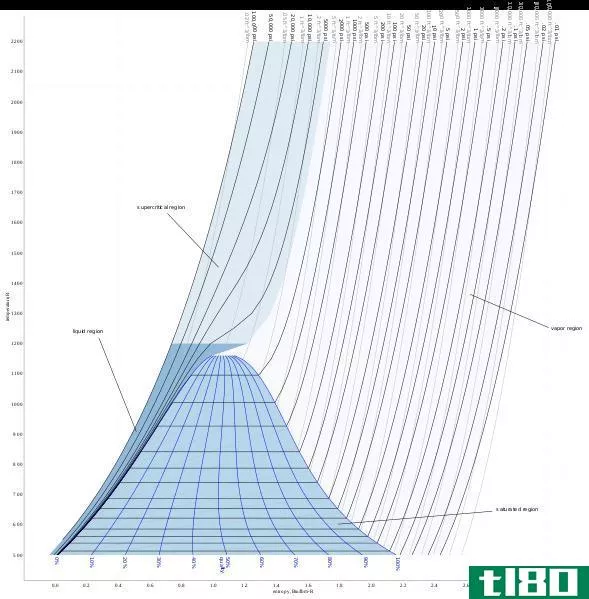
“熵”一词是指系统中的无序或混沌。熵越大,无序度越大。熵存在于物理和化学中,但也可以说存在于人类组织或情境中。一般来说,系统倾向于更大的熵;事实上,根据热力学第二定律,孤立系统的熵永远不会自发降低。这个示例问题演示了如何计算在恒定温度和压力下化学反应后系统周围环境的熵变化。


熵的变化意味着什么
首先,请注意,你们从不计算熵S,而是计算熵的变化ΔS。这是对系统无序性或随机性的度量。当ΔS为正时,意味着环境增加了熵。反应是放热的或(火用的)(假设能量可以以除热以外的形式释放)。当热量释放时,能量增加了原子和分子的运动,导致无序度增加。
当ΔS为负值时,意味着环境的熵减小或环境获得有序。熵的负变化从环境中吸热或能量,从而减少了随机性或混沌性。
需要记住的一点是,ΔS的值适用于周围环境!这是一个观点问题。如果你把液态水变成水蒸气,水的熵会增加,即使周围环境的熵会减少。如果你考虑燃烧反应,那就更令人困惑了。一方面,似乎将燃料分解成其组分会增加无序度,但反应中还包括形成其他分子的氧。
熵例子
计算以下两个反应的环境熵。a.)C2H8(g)+5 O2(g)→ 3 CO2(g)+4H2O(g)ΔH=-2045 kJb.)H2O(l)→ H2O(g)ΔH=+44 kJ溶液在恒定压力和温度下进行化学反应后,环境熵的变化可用公式ΔSsurr=-ΔH/T表示,其中ΔSsurr是环境熵的变化-ΔH是反应热T=凯尔文反应中的绝对温度aΔSsurr=-ΔH/TΔSsurr=-(-2045 kJ)/(25 + 273)**记住将°C转换为K**ΔSsurr=2045 kJ/298 KΔSsurr=6.86 kJ/K或6860 J/KNote。由于反应是放热的,因此周围熵的增加。放热反应由正ΔS值表示。这意味着热量被释放到周围环境或环境获得能量。该反应是C的一个例子燃烧反应。如果你认识到这种反应类型,你应该总是期待放热反应和熵的正变化。反应bΔSsurr=-ΔH/TΔSsurr=-(+44 kJ)/298 KΔSsurr=-0.15 kJ/K或-150 J/K该反应需要来自周围环境的能量才能进行,并降低了周围环境的熵。负ΔS值表示发生了吸热反应,吸收了周围环境的热量。答:反应1和2周围环境的熵变为6860 J/K和-150 J/K意味深长地。
- 发表于 2021-10-14 06:41
- 阅读 ( 136 )
- 分类:数学
你可能感兴趣的文章
构型熵(configurational entropy)和热熵(thermal entropy)的区别
...有相同的尺寸和能量。因此,我们可以使用以下关系式来计算构型熵。它被称为玻尔兹曼熵公式: S=K低 构型熵由“S”给出,其中kB是Boltzmann常数,W是物质可能的构型数。 什么是热熵(thermal entropy)? 热熵是热力学系统的一个广...
- 发布于 2020-09-26 17:30
- 阅读 ( 1577 )
稳态(steady state)和瞬态热分析(transient thermal analysis)的区别
...析。首先,我们应该理解化学中定义的稳态。稳态是化学反应的阶段,中间产物的浓度是恒定的。如果某个化学反应是通过几个步骤(基本步骤)发生的,我们可以用速率测定步骤来确定反应的速率。而且,这一步是其他步骤中...
- 发布于 2020-10-15 11:21
- 阅读 ( 889 )
焓(enthalpy)和熵(entropy)的区别
...它说:“宇宙的熵在自发过程中增加。”熵和产生的热量根据系统使用能量的程度相互关联。事实上,由给定热量q引起的熵变或额外无序度的大小取决于温度。如果它已经很热了,一点额外的热量不会造成更多的混乱,但是如...
- 发布于 2020-11-04 20:59
- 阅读 ( 1883 )
焓(enthalpy)和热(heat)的区别
...为热(q);也就是说,能量以热的形式传递。 热传递是根据温度梯度从高温到低温进行的。此外,这一过程一直持续到系统和周围环境之间的温度达到相同水平。有两种类型的传热过程。它们是吸热过程和放热过程。吸热过程...
- 发布于 2020-11-05 19:40
- 阅读 ( 894 )
熵(entropy)和焓(enthalpy)的区别
...y)? 如上所述,熵度量化学过程中的随机性或无序程度。根据热力学第二定律,认为孤立系统的熵总是增加的。这意味着化学反应将倾向于把自己推向更无序的方向。这是一个过程变得稳定的时候。反应的随机性或无序性随着分...
- 发布于 2021-06-27 08:16
- 阅读 ( 1278 )
焓(enthalpy)和内能(internal energy)的区别
...是吸热的还是放热的。 系统的温度对焓有很大的影响。根据上面给出的方程,焓随内能的变化而变化。当温度升高时,由于分子的动能增加,内能就会增加。系统的焓也随之增加。 什么是内能(internal energy)? 系统的内能是该系...
- 发布于 2021-06-29 08:17
- 阅读 ( 943 )
吸热的(endothermic)和放热反应(exothermic reactions)的区别
...别(main difference endothermic) vs. 放热反应(exothermic reacti***) 根据环境与反应体系之间的能量传递,化学反应可分为吸热反应和放热反应。为了将一个特定的化学反应分为吸热反应和放热反应,我们可以计算反应物和产物之间的焓变...
- 发布于 2021-06-29 08:53
- 阅读 ( 1317 )
内源性(endergonic)和火用的(exergonic)的区别
...焓的差值)。由于新产品的形成,系统的熵减小。然后,根据上述方程ΔG是正值。内源性反应包括吸热反应。 什么是火用的(exergonic)? 火用反应是一种吉布斯自由能为负的反应。这表明火用反应是自发反应,因为当用下面给出...
- 发布于 2021-06-29 14:25
- 阅读 ( 290 )
等熵(isentropic)和绝热的(adiabatic)的区别
...气体压缩机等。 Figure 1: Entropy is C***tant for Isentropic Systems 根据热力学第二定律, dS=dQ/T dS是熵的变化,dQ是热能或传热的变化,T是温度。为了保持恒定的熵,系统和周围环境之间不发生热传递(因为根据上述定律,增加能量会增...
- 发布于 2021-06-29 21:23
- 阅读 ( 728 )
生成热(heat of formation)和反应热(heat of reaction)的区别
...of formation is ΔHf°. It can be calculated using the following equation. 根据这个方程,标准生成热等于产品标准生成焓和反应物标准生成焓之和的差。 什么是反应热(heat of reaction)? 反应热是化学反应过程中应添加或释放的净能量。换句话说...
- 发布于 2021-06-30 11:58
- 阅读 ( 640 )