强酸和关键事实清单
化学中有七种“强酸”。使它们“强大”的是,当它们与水混合时,完全分解成离子(H+和阴离子)。其他酸都是弱酸。因为只有七种常见的强酸,所以很容易将列表保存到内存中。


关键收获:强酸列表
- 强酸是在其溶剂中完全解离的酸。在大多数定义下,酸分解成带正电的氢离子(质子)和带负电的阴离子。
- 七种最常见的强酸是盐酸、硝酸、硫酸、氢溴酸、氢碘酸、高氯酸和氯酸。人们遇到的大多数其他酸都是弱酸。
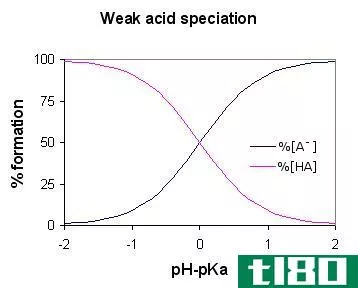
- 强酸的pKa值小于-2。
强酸清单
请注意,一些化学教师可能只提及六种强酸。这通常意味着该列表中的前六种酸:
- 盐酸:盐酸
- 硝酸
- 硫酸:硫酸
- HBr:氢溴酸
- HI:氢碘酸(也称为氢碘酸)
- HClO4:高氯酸
- HClO3:氯酸
其他强酸
还有其他强酸,但在日常生活中不会遇到。示例包括三氟磺酸(H[CF3SO3])和氟锑酸(H[SbF6])。
强酸总是很强吗?
当强酸变得更浓时,它们可能无法完全解离。经验法则是强酸在浓度为1.0 M或更低的溶液中100%解离。
解离和pka值
强酸离解反应的一般形式如下:
HA+S↔ SH++A-
在这里,S是一种溶剂分子,如水或二甲基亚砜(DMSO)。
例如,这里是盐酸在水中的离解:
盐酸(aq)→ H+(aq)+Cl-(aq)
强酸的pKa值小于-2。酸的pKa值取决于溶剂。例如,盐酸在水中的pKa值约为-5.9,在DMSO中为-2.0,而氢溴酸在水中的pKa值约为-8.8,在DMSO中为-6.8。
近距离观察一些强酸
- 盐酸:盐酸也被称为盐酸。这种酸无色,有刺激性气味。人类和大多数其他动物在消化系统中分泌盐酸。这种酸有许多商业用途。它用于生产无机化合物、精炼金属、酸洗钢和调节普通强酸的pH值。对于普通强酸而言,它是处理危险性最小、价格最低、最容易储存的产品之一。
- 硝酸:硝酸也被称为富通水。它是一种腐蚀性很强的酸。虽然纯硝酸无色,但随着时间的推移,它会分解成氮氧化物和水而变黄。在化学中,它的主要用途之一是硝化作用。这是一个硝基被添加到分子中(通常是有机的)。硝酸被用作尼龙生产中的氧化剂、火箭燃料中的氧化剂和分析试剂。
- 硫酸:硫酸(美国拼法)或硫酸(英联邦拼法)也称为硫酸油。它无色、无味、粘稠。纯硫酸不是自然存在的,因为这种酸对水蒸气有很强的吸引力。这是一种危险的酸,因为它具有很强的腐蚀性,接触后会使皮肤严重脱水,导致酸性化学灼伤和热灼伤。它的主要用途是生产肥料。它还用于制造洗涤剂、染料、树脂、杀虫剂、纸张、炸药、醋酸盐、电池和药品。硫酸也用于水处理。
来源
- 贝尔,R.P.(1973)。《化学中的质子》(第二版)。纽约州伊萨卡:康奈尔大学出版社。
- Guthrie,J.P.(1978年)。“含氧酸酯的水解:强酸的pKa值”。可以J.化学。56 (17): 2342–2354. 内政部:10.1139/v78-385
- 豪斯克罗夫特,C.E。;夏普,A.G.(2004)。无机化学(第二版)。普伦蒂斯大厅。ISBN 978-0-13-039913-7。
- 米斯勒。;Tarr D.A.(1998年)。无机化学(第二版)。普伦蒂斯大厅。ISBN 0-13-841891-8。
- 佩特鲁奇,R.H。;哈伍德,R.S。;赫林,F.G.(2002年)。普通化学:原理和现代应用(第8版)。普伦蒂斯大厅。ISBN 0-13-014329-4。
- 发表于 2021-10-21 06:37
- 阅读 ( 260 )
- 分类:化学
你可能感兴趣的文章
均衡(equalization)和中和(neutralization)的区别
...,也可以是弱碱。根据这一事实,反应各不相同。 图01:强酸-强碱中和滴定 中和反应有四种不同类型:强酸强碱反应、强酸弱碱反应、弱酸弱碱反应和弱酸弱碱反应。根据酸和碱的强度,这些反应在不同程度上经历中和。 均衡...
- 发布于 2020-10-03 12:46
- 阅读 ( 235 )
弱酸(weak acid)和稀酸(dilute acid)的区别
...离子)的化合物。因此,酸的pH值低于7。根据酸的强度有强酸和弱酸两种类型。但根据酸的浓度,有浓酸和稀酸两种酸溶液。 目录 1. 概述和主要区别 2. 什么是弱酸 3. 什么是稀酸 4. 并列比较-弱酸与稀酸的表格形式 5. 摘要 什么...
- 发布于 2020-10-16 18:33
- 阅读 ( 562 )
浓酸(concentrated acid)和强酸(strong acid)的区别
关键区别-浓酸与强酸 酸是一种化合物,它可以通过酸分子的离子化将氢离子(质子)释放到其所在的介质中。酸有两种主要类型,即强酸和弱酸。强酸是在水溶液中完全离解,释放H+离子的酸。强碱是在水溶液中完全离解形...
- 发布于 2020-10-19 14:49
- 阅读 ( 380 )
虚弱的(weak)和强酸(strong acid)的区别
弱酸和强酸的关键区别在于弱酸在水中部分电离,而强酸则完全电离。 酸的强度是它在水溶液中与水发生反应时电离或提供氢离子的能力。酸离子化得越多,它就越强,氢离子的生成越少,说明酸是弱酸。这就是强酸和弱酸...
- 发布于 2020-10-23 09:57
- 阅读 ( 340 )
费希尔酯化(fischer esterification)和斯特格利希酯化(steglich esterification)的区别
...ischer酯化和Steglich酯化的关键区别在于,Fischer酯化涉及在强酸作为催化剂存在下羧酸和醇之间的反应,而Steglich酯化涉及在强酸存在下羧酸和醇之间的反应以二甲氨基吡啶(DMAP)为催化剂。 酯化反应是化学中一个重要的有机合...
- 发布于 2021-03-04 18:48
- 阅读 ( 1344 )
坚强的(strong)和弱酸(weak acid)的区别
...酸释放出的质子的数量实际上决定了酸的强度——无论是强酸还是弱酸。为了了解酸的强度,我们需要比较它们向类似的碱(主要是水)提供质子的倾向。强度由一个称为pKA的数字表示。 什么是强酸(a strong acid)? 如果一种...
- 发布于 2021-06-25 16:37
- 阅读 ( 409 )
坚强的(strong)和弱酸(weak acids)的区别
...反应中提供质子或接受电子对的分子或其他物质。酸分为强酸和弱酸两类。强酸和弱酸的主要区别在于强酸在水溶液中完全解离,而弱酸在水溶液中部分解离。 覆盖的关键领域 1.什么是强酸-定义、性质、示例2。什么是弱酸-定...
- 发布于 2021-06-28 19:21
- 阅读 ( 1030 )
盐酸(hydrochloric acid)和硫酸(sulfuric acid)的区别
... 酸是能够将质子或H+离子提供给水溶液的分子。酸主要有强酸和弱酸两种。盐酸和硫酸是两种强酸。盐酸和硫酸的主要区别在于盐酸是一元的,而硫酸是二元的。 覆盖的关键领域 1.什么是盐酸-定义、性质2。什么是硫酸-定义、...
- 发布于 2021-06-28 19:31
- 阅读 ( 674 )
盐酸(hydrochloric acid)和盐酸(muriatic acid)的区别
...中和碱溶液和腐蚀性等特性。与其他酸相比,盐酸是一种强酸。人们常常把盐酸和盐酸混淆,认为两者是相同的;然而,盐酸和盐酸之间有细微差别。盐酸和盐酸的主要区别在于盐酸只由HCl分子组成,而盐酸是由杂质和HCl分子组...
- 发布于 2021-06-28 19:45
- 阅读 ( 440 )
巴基斯坦航空公司(pka)和酸碱度(ph)的区别
...下。 pKa=–log10[Ka]通过观察pKa值,我们可以确定一种酸是强酸还是弱酸。如果pKa值高,酸就弱。这是因为较高的pKa值表明Ka较低。为了使Ka的值较低,[A–][H+]值应低于[HA]值。这意味着酸被部分解离。但如果[A–][H+]的值高于[HA],...
- 发布于 2021-06-28 20:09
- 阅读 ( 324 )