主要区别
原子和离子的主要区别在于原子是物质的基本单位。它的原子核中含有相等数量的电子和质子,因此带有净的中性电荷,而离子则是一个原子,其中含有不相等数量的质子和电子,因此带有净的正电荷或负电荷。
原子(atom) vs. 离子(ion)
原子是宇宙中所有物质的基本单位,因此产生了所有的成分。相反,离子是带电荷的原子,即含有正电荷或负电荷。原子没有进一步的分类,它是宇宙中物质组成的基本单位,但是,根据离子携带的正电荷或负电荷,离子又分为阳离子和阴离子两类。
原子是由等量的质子和电子组成的,就像它们现有的自然形态一样,有不同数量的电子和不同原子序数的质子。然而,离子包含奇数个或不相等数量的电子和质子,因为原子在最外层吸引一个电子,或失去一个电子给另一个原子而成为离子。
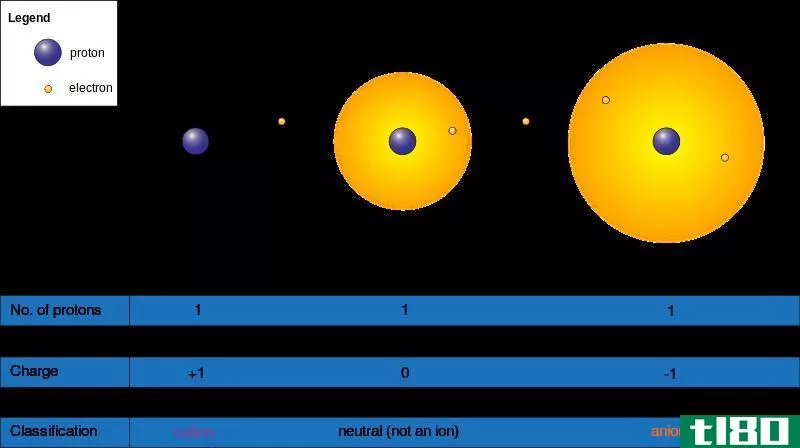
由于携带正电荷的质子和带负电荷的电子数量相等,原子带有净中性电荷。而离子由于电子和质子的数目不等而带有净正电荷或负电荷,即它们在最外层吸引一个电子或将一个电子输给另一个原子。原子不带任何电荷,即净中性电荷,因此对电场没有任何吸引力或排斥。然而,由于离子带有一个净的正电荷或负电荷,因此,它们对电场的吸引力或排斥性取决于它们的承载电荷。
由元素的简单分子式表示的原子由于没有电荷而呈中性。相反,离子用负电荷或正电荷来表示,根据其携带电荷,表示过量或丢失电子的数量。原子有氖以氖表示,铁以铁和分别表示的例子,而离子有钴离子用二氧化碳+和氮化物-N3-和分别表示的例子。
比较图
什么是原子(an atom)?
原子是宇宙中所有物质的基本单位,因为它们衍生出所有的成分。在早期,科学家们认为原子不能进一步分裂,而质子、电子和原子核的发现使原子无法进一步分裂。原子理论把原子的结构描述为原子是如何由电子和质子组成的。在现代,这一理论先于现代原子理论,根据现代原子理论,原子由两个成分组成。这些成分是原子核和亚原子粒子。
原子没有进一步的分类,是宇宙中物质组成的基本单位。如前所述,由相同的质子和电子组成,其存在的自然形式具有不同的原子序数。由于携带正电荷的质子和带负电荷的电子的数量相等,原子带有净中性电荷。它们对电场也没有任何吸引力或排斥。
原子之间可以形成化学键,形成分子和化合物。这些键可以是共价键、离子键或金属键。由于电子相互交换,原子间形成了这些键。
然而,质子和中子并不直接参与键的形成。由元素的简单分子式表示的原子,由于没有电荷而呈中性。一些常见的原子例子包括氖原子,它们分别用氖和氢来表示。
什么是离子(ion)?
离子是带有净电荷的原子或分子,即含有正电荷或负电荷。因为当一个原子或一个分子在最外层吸引一个电子,或者把一个电子输给另一个原子,它就变成了离子。根据它们带有正电荷或负电荷,它们又分为阳离子和阴离子两类。
负离子是指由于原子核中的质子无法中和所获得的电子的影响而从周围的原子或分子中获得过量电子而带净负电荷的离子。阳离子是一种原子或分子,在暴露在环境中的最外层失去电子,从而带上净正电荷。
离子带有一个净的正电荷或负电荷,因此根据它们的承载电荷对电场表现出吸引或排斥。它们也能形成离子键。这些离子键是在这些被吸引的离子的作用下形成的,由于这些原子上有两个相反的电荷,这些离子被静电吸引而相互吸引。这些离子用一个电荷来表示,不管是负电荷还是正电荷,它代表过量或丢失的电子的数量。常见的离子有钴(用Co 2+表示)和氮化物(分别用N3-和表示)。
主要区别
- 原子是宇宙中所有物质的基本单位;相反,离子是带正电荷或负电荷的原子。
- 原子是由等量的质子和电子组成的,就像它们存在的自然形态一样;另一方面,离子通过吸引或失去最外层的电子而包含数量不等的电子和质子。
- 由于质子和电子的数量相等,原子带有净中性电荷,另一方面,由于电子和质子数量不相等,离子带有净正电荷或负电荷。
- 原子对电场不表现出任何吸引力或排斥力,然而,由于离子带有净的正电荷或负电荷,它们对电场的吸引力或排斥力取决于它们的承载电荷。
- 由于没有电荷,原子由一种元素的中性分子式表示。相反,离子是用电荷来表示的,电荷是负的,也可能是正的,这取决于相对于质子的电子数。
- 另一方面,原子没有进一步的分类,根据离子携带的正电荷或负电荷,离子进一步分为阳离子和阴离子两类。
- 原子的例子有氢原子用H表示,铁用铁表示,而离子的例子是;钴,用Co 2+表示,氮化物用N3-表示。
结论
原子是物质的基本单位,它含有等量的电子和质子,并带有净中性电荷。然而,由于质子和电子的数量不等,由带有净正电荷或负电荷的原子组成的离子。