均相反应与非均相反应的关键区别在于参与均相反应的反应物和产物处于同一相,而非均相反应的反应物和产物处于不同的相。
同质性和异质性是我们描述的关于一个物体的均匀性的两个化学概念。主体可以是成分、反应等的混合物。术语“同质”指“相同”,而“异质”指“不同”。
目录
1.概述和主要区别
2. 什么是均相反应
3. 什么是多相反应
4. 并列比较-均相反应与非均相反应的表格形式
5. 摘要
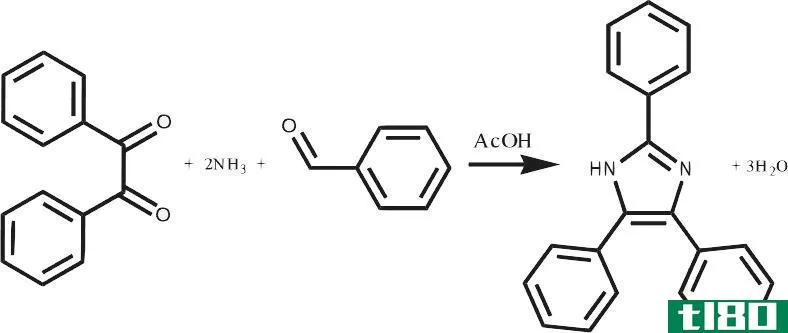
什么是均相反应(homogeneous reacti***)?
均相反应是指反应物和产物处于物质同一相的化学反应。物质有三个相:固相、液相、气相。如果一个均相反应的反应物处于气相,那么该反应所得到的产物也处于气相。
最重要的均相反应是气体之间的反应和液体或溶解在液体中的物质之间的反应。

图01:氧乙炔火炬燃烧
这些反应与非均相反应相比是非常简单的反应。这是因为在这些反应过程中发生的化学变化只取决于反应物之间相互作用的性质。
示例:
- 空气中一氧化碳和氧气的反应
- 盐酸与氢氧化钠在水中的反应
- 氧乙炔火炬燃烧
什么是多相反应(heterogeneous reacti***)?
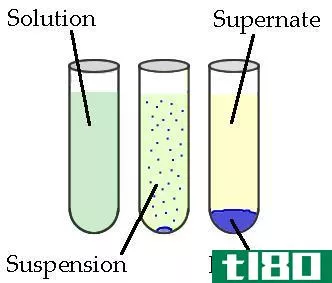
非均相反应是指反应物和产物处于两个或多个相的化学反应。因此,任何反应物和产物都可以处于三相中的一种:固相、液相或气相。因此,多相反应缺乏均匀性。

图02:盐和水之间的反应是不均匀的
此外,在不同相的催化剂表面发生的反应也是非均相的。这些反应更为复杂,因为它们考虑了物质的相以及反应物之间相互作用的性质。
示例:
- 煤在空中燃烧
- 盐和水的反应
- 铁锈水下
- 金属钠与水的反应
同种类的(homogeneous)和多相反应(heterogeneous reacti***)的区别
均相反应是指反应物和产物处于物质同一相的化学反应。而非均相反应是指反应物和产物处于两个或多个相的化学反应。因此,这是均相反应和非均相反应的关键区别。此外,均相反应和非均相反应的另一个区别是均相反应具有均匀性,而且非常简单。这是因为这些反应只取决于反应物之间相互作用的性质。另一方面,非均相反应缺乏均匀性。而且,这些反应非常复杂。除此之外,这些反应还考虑了物质的相态以及反应物之间相互作用的性质。
在下表中,均相反应和均相反应之间的差异以表格形式呈现。

总结 - 同种类的(homogeneous) vs. 多相反应(heterogeneous reacti***)
化学反应可分为均相反应和非均相反应两类。均相反应与非均相反应的关键区别在于参与均相反应的反应物和产物处于同一相,而非均相反应的反应物和产物处于不同的相。
引用
1“同质性和异质性”,维基百科,维基媒体基金会,2018年7月28日。这里有2个。大英百科全书的编辑。“均相反应”,《大英百科全书》,大英百科全书,2016年12月21日。此处提供
2大英百科全书的编辑。“均相反应”,《大英百科全书》,大英百科全书,2016年12月21日。