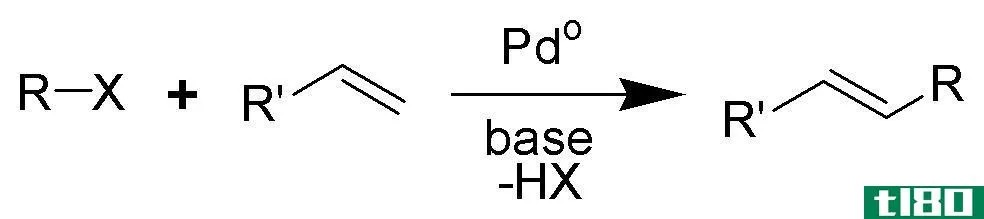催化反应与非催化反应的关键区别在于,催化反应在化学反应过程中涉及催化剂,而非催化反应在反应过程中不涉及催化剂。
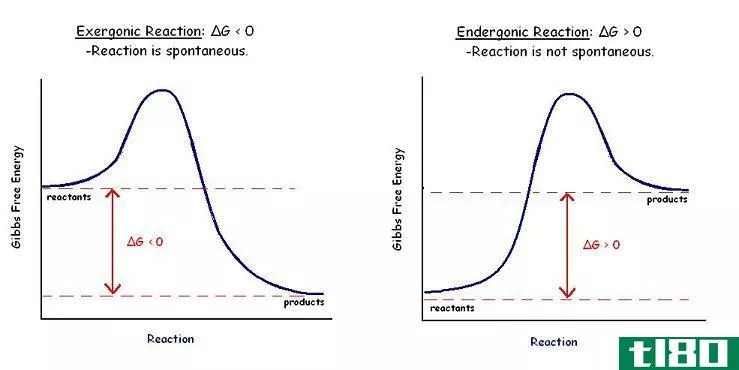
化学反应是通过化学方法将反应物转化为产物。一些化学反应在正常条件下是自发的,而另一些则是非自发的。有些化学反应需要催化剂来提高反应速率。这些催化剂可以是生物成分,也可以是化学成分。
目录
1. 概述和主要区别
2. 什么是催化反应
3. 什么是非催化反应
4. 并列比较-表格式的催化反应与非催化反应
5. 摘要
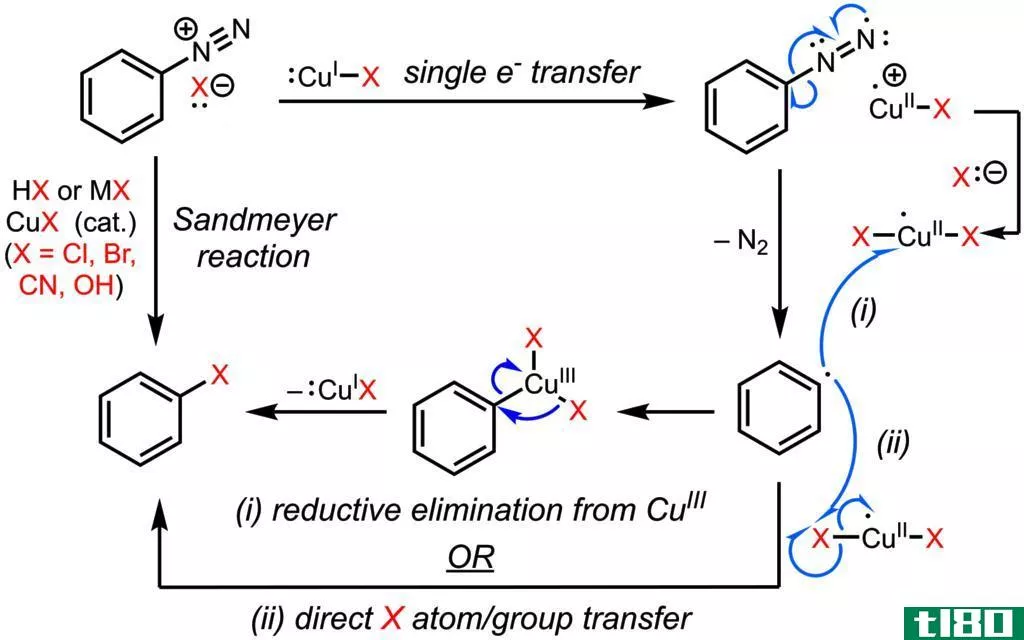
什么是催化反应(catalytic reaction)?
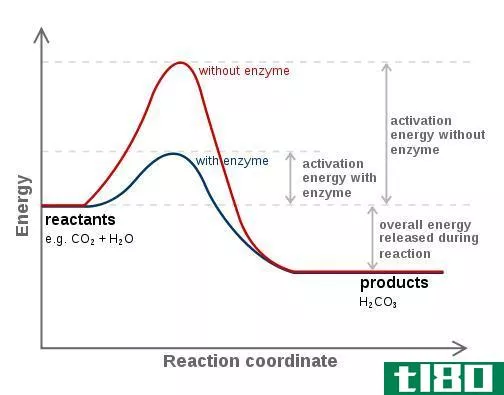
催化反应是催化剂提高反应速率的化学反应。催化剂可以是生物化合物,也可以是化学化合物。这些化合物通过降低反应的活化能来提高反应速率。化学反应过程中催化剂从不消耗。因此,我们可以再生催化剂。通常在这些反应中,在反应物阶段和产物形成阶段之间形成中间络合物。
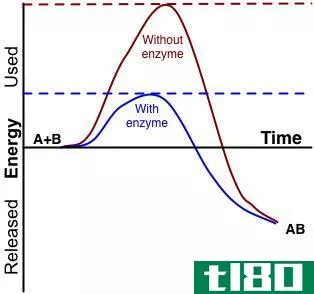
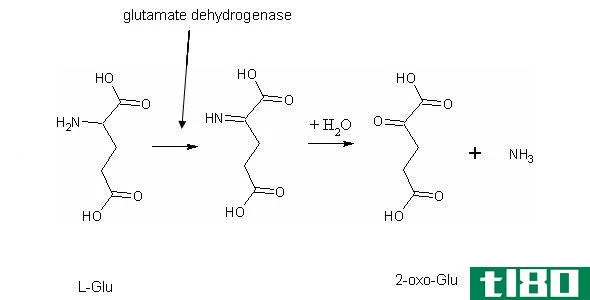
图01:酶降低反应速率
这种中间产物是一种暂时的复合物。这种中间产物的形成导致催化剂的再生。催化剂可以是均相催化剂,也可以是非均相催化剂。均相催化剂与反应物处于同一相,而非均相催化剂与反应物处于不同的相。酶是生物催化剂。
什么是非催化反应(non catalytic reaction)?
非催化反应是指在反应过程中没有催化剂参与的化学反应。因此,在这些反应中,反应速率不会因任何外部影响而增加。
非催化反应有两种类型:均相反应和非均相反应。在均相非催化反应中,反应物和产物处于同一相,而在非均相非催化反应中,反应物和产物处于不同的相。
催化的(catalytic)和非催化反应(non catalytic reaction)的区别
催化反应是催化剂提高反应速率的化学反应。也就是说,这些反应需要催化剂。但是,非催化反应是指不需要催化剂参与反应过程的化学反应。这是催化反应和非催化反应的主要区别。此外,这两种反应有均相和非均相两种形式。均相催化反应是指反应物、产物和催化剂处于同一相的物质。多相催化反应涉及物质不同相的反应物、产物和催化剂。同理,均相非催化反应涉及物质同相的反应物和产物,非均相非催化反应涉及物质不同相的反应物和产物。

总结 - 催化的(catalytic) vs. 非催化反应(non catalytic reaction)
化学反应分为催化型和非催化型两种。催化反应与非催化反应的区别在于,催化反应在化学反应过程中涉及催化剂,而非催化反应在反应过程中不涉及催化剂。
引用
1“催化作用”,维基百科,维基媒体基金会,2018年7月1日。可在此处查阅。普**德,肖希。“Shoshi催化和非催化反应”,LinkedIn SlideShare,2017年10月22日。此处提供
2普**德,肖希。“Shoshi催化和非催化反应”,LinkedIn SlideShare,2017年10月22日。