自发反应与非自发性反应的关键区别在于自发反应具有负的Gibbs自由能,而非自发反应具有正的Gibbs自由能。
反应可以是化学反应,也可以是生物反应。我们可以把这些反应分为两类:自发反应和非自发反应。自发反应没有任何外部影响。但是,没有外部的影响,非自发的反应就无法进行。让我们讨论这些反应的更多细节,并将自发反应和非自发性反应的区别制成表格。
目录
1. 概述和主要区别
2. 什么是自发反应
3. 什么是非自发性反应
4. 并列比较-自发反应与非自发反应的表格形式
5. 摘要
什么是自发反应(spontaneous reacti***)?
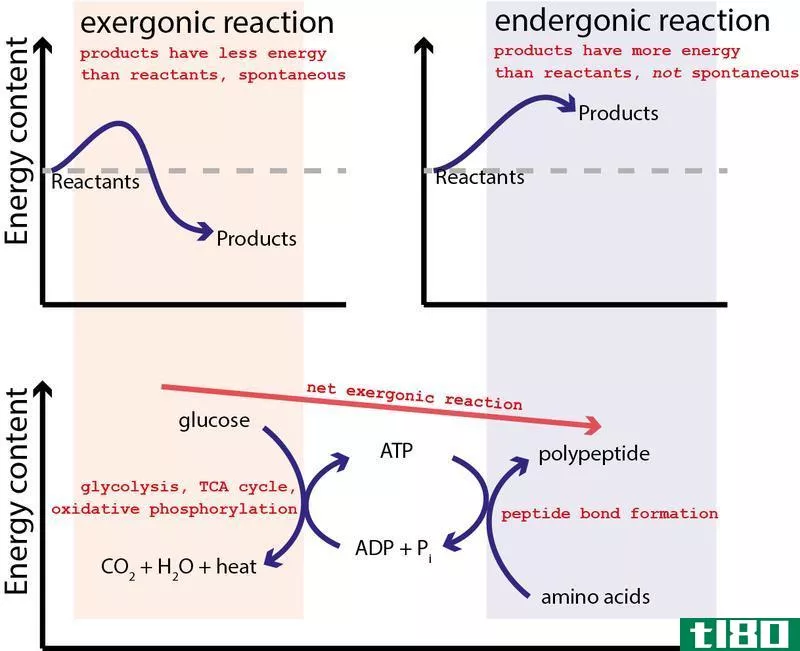
自发反应是指不受外界因素影响而发生的化学或生物反应。此外,这些反应有利于增加熵,同时降低热力学系统的焓。由于这些反应不需要外界因素,它们自然发生。因此,这些反应有利于在反应发生的条件下生成产物。自发反应的吉布斯自由能是负值。
大多数自发反应发生得很快,因为它有利于形成产物,而不是保持反应物原样。例:氢气燃烧。但有些反应非常缓慢。把石墨转化成钻石。此外,在一些可逆反应中,一个反应方向优于另一个反应方向。例如,在碳酸生成二氧化碳和水的过程中,正反应是有利的;二氧化碳和水的形成是自发的。
H2CO3↔ 二氧化碳+水
什么是非自发性反应(n***pontaneous reacti***)?
非自发反应是指没有任何外部因素的影响而不能发生的化学或生物反应。因此,这些反应在自然条件下不会发生。
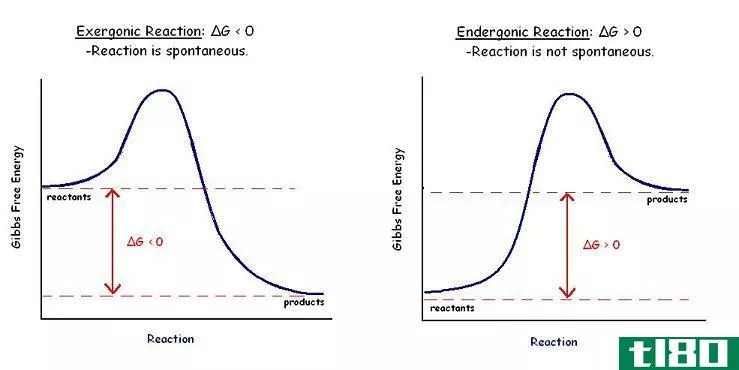
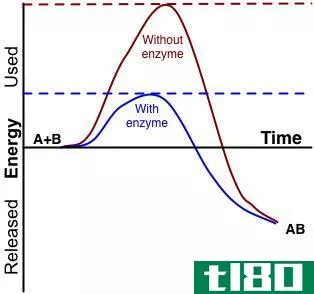
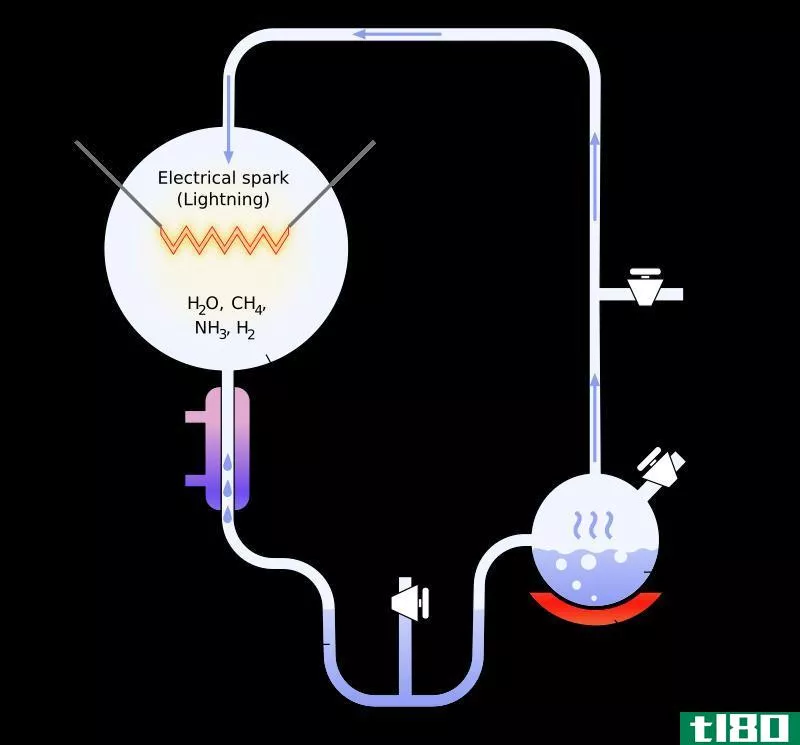
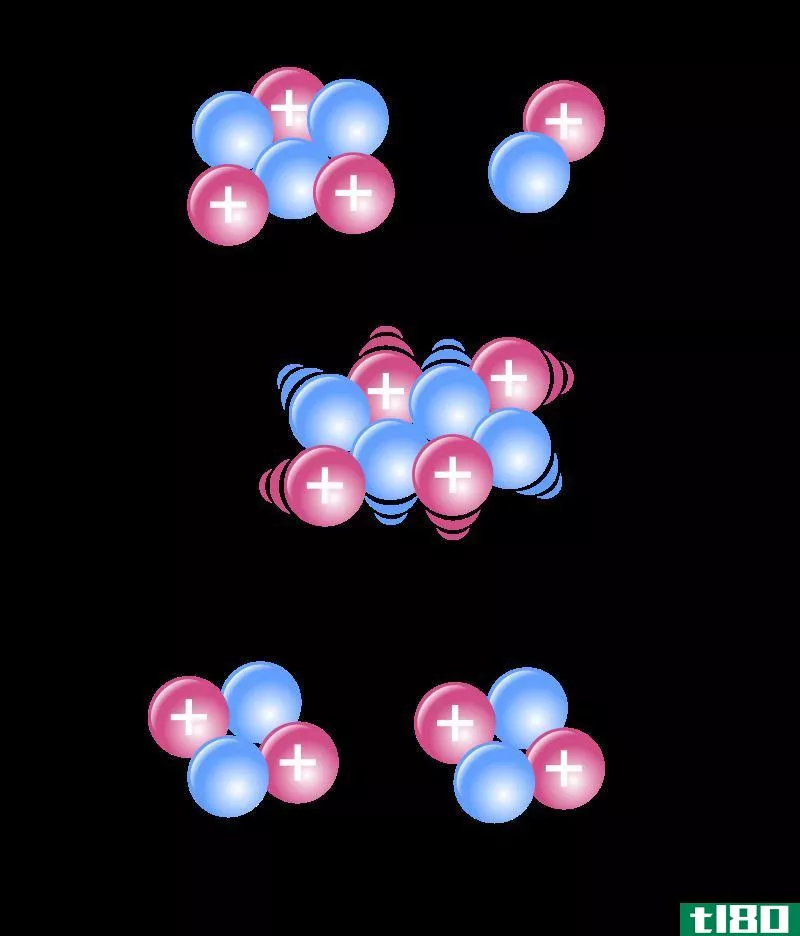
图01:自发和非自发反应的比较
因此,我们必须为这些对进步的反应提供一些外部因素。例:我们可以提供热量,给一些压力,加催化剂等等。而且,吉布斯自由能对这些反应是正的。
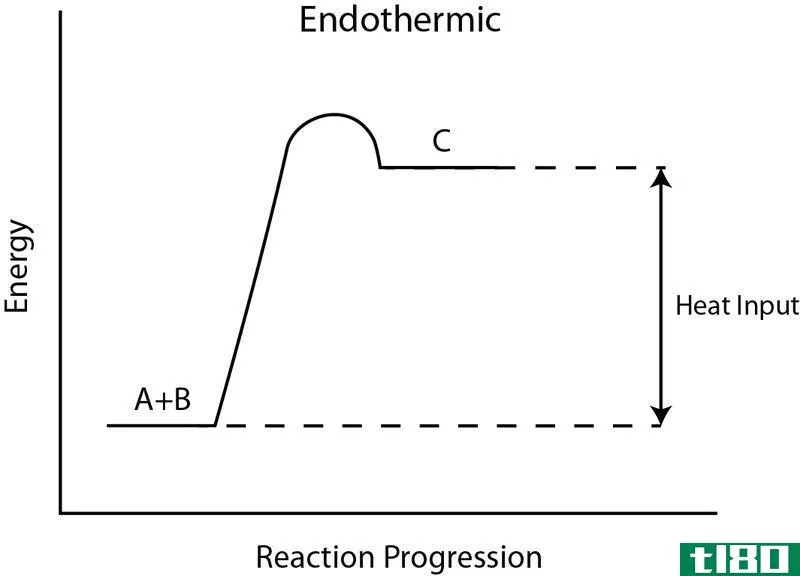
几乎所有的非自发反应都是吸热的,它们向外界释放能量。这些反应伴随着熵的减少。例:在正常温度和压力条件下,我们大气中的氧和氮反应生成一氧化氮(NO气体)是非自发的。然而,这种反应发生在非常高的温度下。
自发的(spontaneous)和非自发性反应(n***pontaneous reacti***)的区别
自发反应是指不受外界因素影响而发生的化学或生物反应。它们有利于增加热力学系统的熵,同时降低热力学系统的焓。此外,自发反应的吉布斯自由能是负值。而非自发反应是指没有任何外部因素的影响而不能发生的化学或生物反应。它们不赞成在正常情况下增加熵或降低焓。此外,非自发反应的吉布斯自由能为正值。

总结 - 自发的(spontaneous) vs. 非自发性反应(n***pontaneous reacti***)
所有的反应都属于自发反应和非自发反应两类。自发反应和非自发反应的区别在于,自发反应具有负吉布斯自由能,而非自发反应具有正吉布斯自由能。
引用
1歌词。“11.5:自发反应和自由能”,《化学文摘》,歌词,2018年7月13日。可在此处查阅2。科学,Ck12。“自发和非自发性反应”,CK-12基金会,CK-12基金会,2017年3月28日。此处提供
2科学,Ck12。“自发和非自发性反应”,CK-12基金会,CK-12基金会,2017年3月28日。