H2O与H2O2 |水与过氧化氢的特性、用途、差异
水(H2O)和过氧化氢(H2O2)是氧和氢元素的分子。
水
众所周知,水是一种水,没有它我们就无法生存。两个氢共价键合在氧上形成水。分子的形状是弯曲的,以使电子孤对键的排斥作用最小,H-O-H角为104o。水是一种清澈、无色、无味、无味的液体,可以有雾、露水、雪、冰、蒸汽等各种形式。水在正常大气压下加热到100℃以上时,就会进入气相。
水确实是一种神奇的分子。它是生物中含量最丰富的无机化合物。我们身体75%以上是由水组成的。它是细胞的组成部分,起溶剂和反应物的作用。水在室温下是一种液体,尽管它的分子量很低,只有18 gmol-1。水形成氢键的能力是它的独特特性。单个水分子可以形成四个氢键。氧比氢更具电负性,使水中的O-H键极性。由于极性和形成氢键的能力,水是一种强大的溶剂。由于其溶解大量物质的能力,它被称为通用溶剂。此外,水具有高表面张力、高附着力、内聚力。水可以承受温度的变化而不会变成气体或固体。这被称为具有高热容,这反过来又对生物体的生存很重要。
过氧化氢
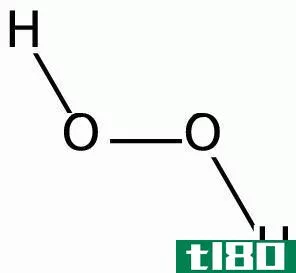
过氧化氢是过氧化氢的最简单形式,用过氧化氢表示。它是一种沸点为150℃的透明液体。它与水完全混溶,但可以通过蒸馏完全分离,因为它的沸点比水高。过氧化氢是一种强氧化还原剂。过氧化氢是一种平面的非线性分子。它有一个开放的书籍结构。
过氧化物是各种化学反应的副产品或中间体。这种反应在我们体内也会发生。过氧化物在我们的细胞内有毒性作用。因此,它们一旦产生就必须被中和。我们的细胞有一种特殊的机制。在我们的细胞中有一种叫做过氧化物酶体的细胞器,它含有过氧化氢酶。这种酶催化过氧化氢分解成水和氧;因此,有解毒功能。过氧化氢具有危险特性,如随着热的演化分解为氧气和水,由于污染或与活性表面接触而分解,由于氧气压力的形成而在容器内增加,还可形成爆炸性混合物。过氧化氢的漂白作用是由于氧的氧化和释放。这种氧会与有色物质发生反应,使其无色。
H2O2→H2O+O
O+色素→无色物质
除漂白外,过氧化氢还用作火箭燃料的氧化剂,用于生产环氧化物、药品和食品,用作防腐剂等。过氧化氢储存在涂有石蜡的玻璃瓶、塑料瓶或聚四氟乙烯瓶中。
| 水(H2O)和过氧化氢(H2O2)有什么区别?•在水中,H:O比为2:1,而在过氧化氢中为1:1。•在水中,氧为-2氧化状态。然而,在H2O2中,氧具有-1氧化状态。•H2O2比水具有更高的沸点。•与水相比,H2O2是一种强氧化和还原剂。•与H2O2相比,水是一种很好的溶剂。 |