有效核电荷与核电荷
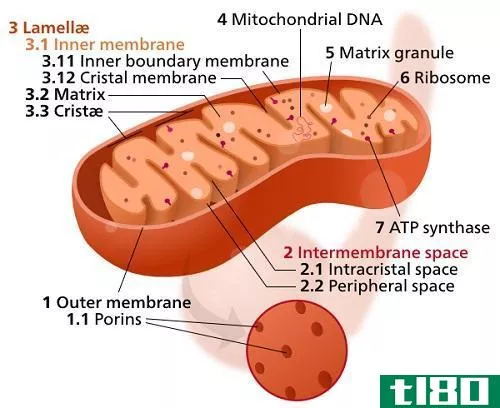
原子主要由质子、中子和电子组成。原子核含有质子和中子。有电子绕着原子核绕轨道旋转。元素的原子序数是它在原子核中的质子数。表示原子序数的符号是Z。当原子为中性时,它的电子数与质子相同。因此,在这种情况下,原子序数等于电子数。
什么是核电荷?
在原子核中,主要有两个亚原子粒子,中子和质子。中子没有电荷。但是每个质子都带正电荷。如果原子核中只有质子,它们之间的排斥力会更高(就像电荷互相排斥一样)。因此,中子的存在对于将质子结合在原子核中是很重要的。原子核中所有质子的总正电荷称为核电荷。由于原子中质子的数量与原子序数相似,原子核电荷也与元素的原子序数相似。因此,原子核电荷是元素所特有的。我们可以看到核电荷是如何通过周期表的周期和群发生变化的。在一段时间内,核电荷从左到右增加,在一个群中也会增加。原子核电荷对原子来说很重要,因为正是静电力吸引并将轨道电子与原子核结合。由于电子带负电,它们被原子核的正电荷吸引。
什么是有效核电荷?
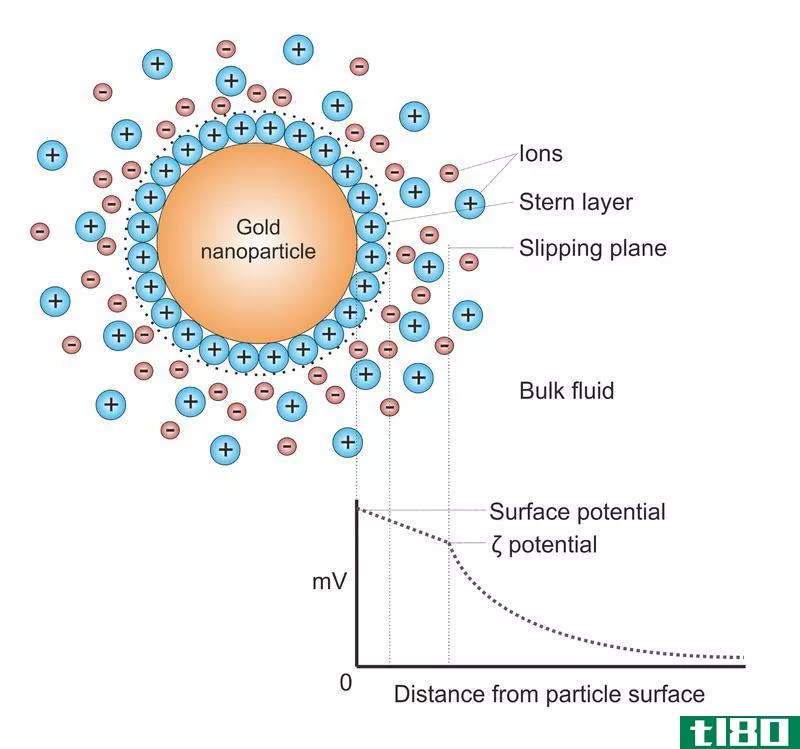
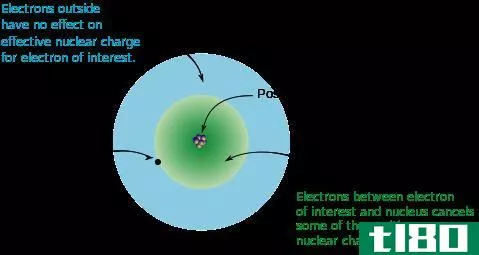
原子中的电子排列在不同的轨道上。在主轨道内,还有其他的子轨道。对于每个亚轨道,两个电子被填满。最后一个轨道上的电子称为价电子,它们距离原子核较远。由于电子带负电,在原子中,它们之间存在电子-电子排斥。原子核中的质子和轨道电子之间也有静电吸引。然而,核电荷对所有电子的影响并不相同。价壳层中的电子感受到最小的核电荷效应。这是因为原子核和外壳之间的电子干涉并屏蔽了核电荷。有效核电荷是外层电子所经历的核电荷。这个值比实际的核电荷要低。例如,氟有九个电子和九个质子。它的核电荷是+9。然而,由于两个电子的屏蔽作用,它的有效核电荷为+7。原子的有效核电荷可用下列公式计算。
有效核电荷=原子序数-非价电子数
| 核电荷和有效核电荷有什么区别?•核电荷是原子核中所有质子的总正电荷。有效核电荷是外层电子经历的核电荷。•有效核电荷低于核电荷值。(有时也可以类似) |