主要区别
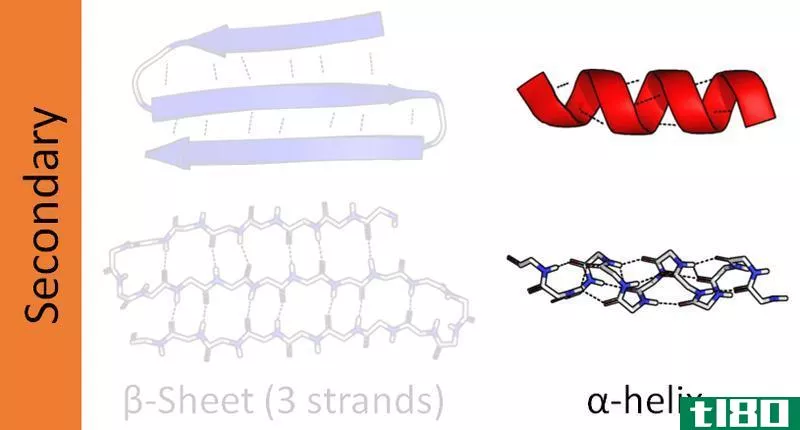
这个基序位于蛋白质的二级结构上,变成规则的螺旋状或螺旋状,这使它具有螺旋的优点,这一事实通常被称为α螺旋。另一方面,β-折叠片(通常称为b-折叠片)将被概括为蛋白质中存在的属性二级结构的标准基序。
比较图
什么是α螺旋(alpha helix)?
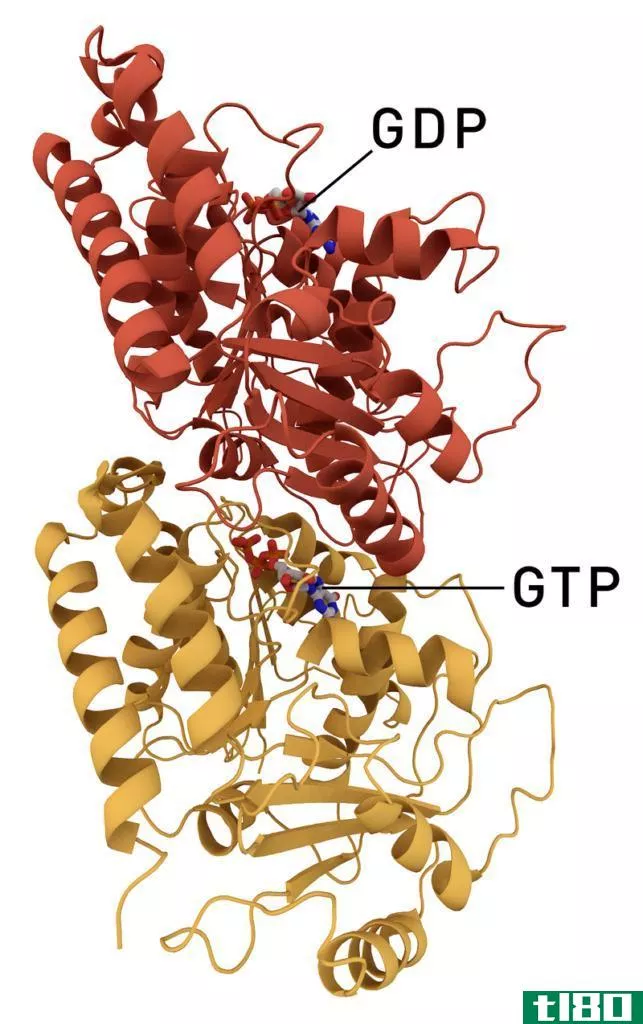
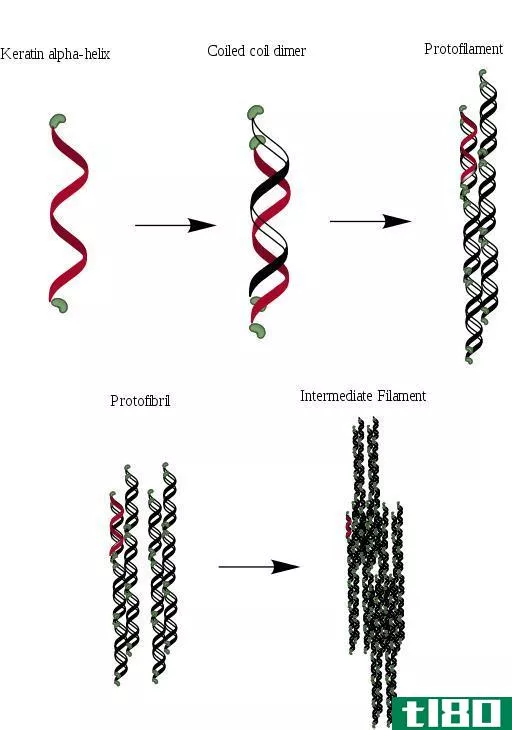
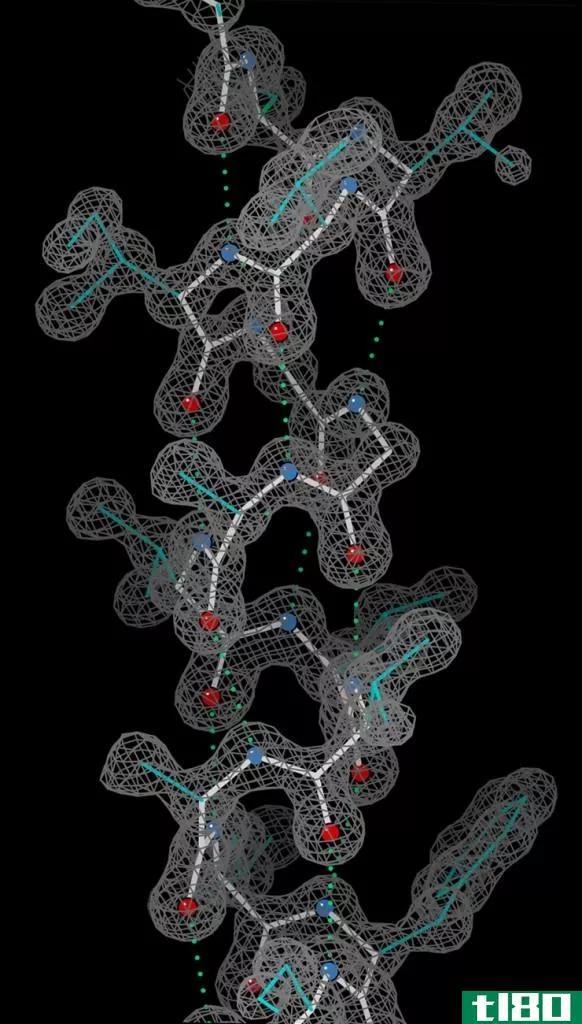
这个基序位于蛋白质的二级结构上,变成规则的螺旋状或螺旋状,这使它具有螺旋的优点,这一事实通常被称为α螺旋。在这里,在整个发育过程中,N-H基团表示与C=O基团的氢键,通常被称为氨基酸的主链,它比蛋白质序列更快地以四个残基存在。目前α-螺旋的两个关键进展是:由于氨基酸和肽的昂贵的石质判断和鲍林对平面肽键的期望,形成了键几何;以及他放弃了对螺旋每一次翻转都有重要数量的沉积的怀疑。在1948年早春,关键时刻就发生在这里,当时鲍林带着一只虫子来到这里,来到床垫上。筋疲力尽后,他在一张纸上画了一条正常测量值正确的多肽链,并将其正确地折叠成螺旋状,敏锐地意识到要处理好平面肽键。α螺旋基本上是自然界中最著名的螺旋电流。它由一条缠绕的多肽链组成,在这条链上,氨基酸的侧链从中心向外扩展,这使得它能够维持它的类型。它们也可能存在于很多种蛋白质中,从球状蛋白质,例如肌红蛋白到角蛋白,后者是一种坚韧的蛋白质。它可以是一个特权给予或左手螺旋,但它肯定已经证明,阿尔法螺旋环是支持的,因为侧链不战斗。这个知识赋予了α螺旋的稳定性。α-螺旋卷曲的每一次翻转都有3.6个氨基的腐蚀性沉积物。
什么是贝塔褶皱床单(beta pleated sheet)?
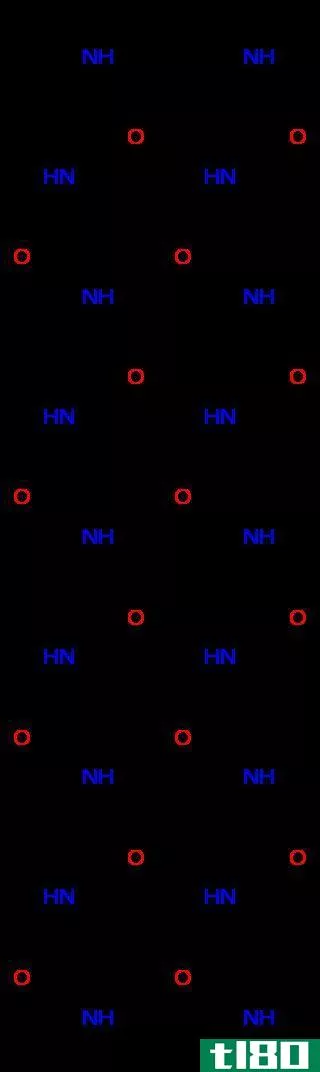
β-折叠片,通常被称为b-折叠片,将被概括为蛋白质中存在的属性二级结构的标准基序。它与完全不同的蛋白质之间的区别变成了一个困难:它是由链组成的,这些链的参考值不低于两个或三个氢原子,而这些氢原子是在对褶皱片进行分类的过程中出现的。β-链是多肽锚定的一个范围,一般有3~10个氨基酸随着脊柱的延长而在一个扩大的适应范围内延长。β-表的超分子关系一直牵扯到蛋白质总量和纤维之间的联系,在相当少数的人类疾病中,尤其是淀粉样变性,例如阿尔茨海默病。当一个多肽链的两个组成部分互相套在一起形成一系列氢键时,就会形成这种结构。这种运动可以发生在平行运动计划中,也可以发生在敌对平行运动计划中。平行的和在同等运动计划的方向上是多肽链方向性的迅速结果。与β折痕薄板相对应的建筑物是α折痕薄板。这座建筑热情地远没有β折痕纸那么完美,在蛋白质方面也是史无前例的。α-折痕纸可以用其羰基和氨基**的从属关系来描述;羰基在一个标题中全部调整,而所有的N-H**都是用替代技术调整的。
主要区别
- 这个基序位于蛋白质的二级结构上,变成规则的螺旋状或螺旋状,这使它具有螺旋的优点,这一事实通常被称为α螺旋。另一方面,β-折叠片(通常称为b-折叠片)将被概括为蛋白质中存在的属性二级结构的标准基序。
- 氨基酸的-R基团存在于螺旋体的底部,而-R基团则存在于螺旋体的底部和内层。
- α-螺旋是一种多肽链,由极模成型,缠绕在弹簧状建筑中,由氢键固定。另一方面,贝塔褶皱床单是由贝塔链制成的,它的侧边不少于两个氢键形成脊柱。
- 螺旋线也可以是左手(beta)或右手-α螺旋线总是右手的地方。在另一种情况下,在β-褶裥床单中,链在替代品之后一个接一个地被调整成另一个串。
- α-螺旋的形成使得氢键在整个多肽链中产生,从而形成螺旋结构。另一方面,β折叠片是通过氢键连接两条或两条以上的β链而存在的。