溶液的依数性
依数性质定义

依数性质是溶液的性质,它取决于溶剂体积中粒子的数量(浓度),而不是溶质粒子的质量或特性。依数性质也受温度的影响。性质的计算只适用于理想解。在实践中,这意味着当非挥发性溶质溶解在挥发性液体溶剂中时,依数性质方程应仅适用于稀释真实溶液。对于任何给定的溶质与溶剂的质量比,任何依数性质都与溶质的摩尔质量成反比。“colligative”一词来自拉丁语colligatus,意思是“结合在一起”,指溶剂的性质如何与溶液中溶质的浓度结合。
依数性质如何工作
当溶质被添加到溶剂中形成溶液时,溶解的颗粒会置换液相中的部分溶剂。这降低了每单位体积溶剂的浓度。在稀溶液中,粒子是什么并不重要,只是有多少粒子存在。例如,完全溶解CaCl2会产生三个粒子(一个钙离子和两个氯离子),而溶解NaCl只会产生两个粒子(一个钠离子和一个氯离子)。氯化钙比食盐对依数性质的影响更大。这就是为什么氯化钙在较低温度下比普通盐更有效的除冰剂。
什么是依数性(the colligative properties)?
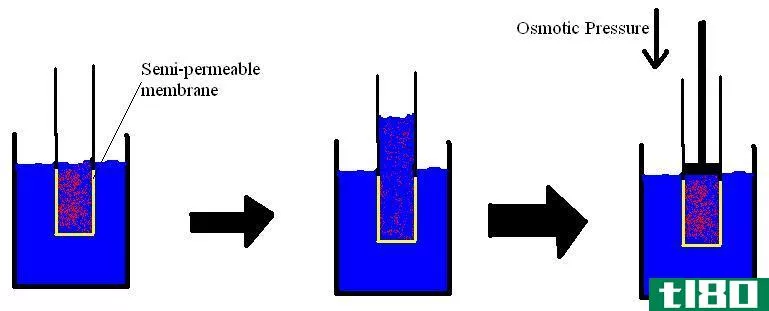
依数性质的例子包括蒸汽压降低、冰点降低、渗透压和沸点升高。例如,向一杯水中加入一小撮盐会使水在比正常情况下更低的温度下结冰,在更高的温度下沸腾,具有更低的蒸汽压,并改变其渗透压。虽然通常认为非挥发性溶质具有依数性质,但这种效应也适用于挥发性溶质(尽管可能更难计算)。例如,向水中添加酒精(一种挥发性液体)会将冰点降低到通常情况下纯酒精或纯水的冰点以下。这就是为什么酒精饮料在家里的冰箱里不会结冰。
冰点降低和沸点升高方程
凝固点降低可通过以下方程式计算:
ΔT=Ikfm,其中ΔT=温度变化,单位为°Ci=van'T Hoff系数kf=摩尔冰点降低常数或冰点降低常数,单位为°C kg/molm=摩尔溶质/kg溶剂中溶质的摩尔浓度
沸点升高可通过以下方程式计算:
ΔT=Kbm
式中,kb=沸点常数(水为0.52°C kg/mol),m=摩尔溶质/kg溶剂中溶质的摩尔浓度
奥斯特瓦尔德的三类溶质性质
Wilhelm Ostwald在1891年引入了依数性质的概念。他实际上提出了三类溶质性质:
- 依数性质仅取决于溶质浓度和温度,而不取决于溶质粒子的性质。
- 组成性质取决于溶液中溶质颗粒的分子结构。
- 附加特性是粒子所有特性的总和。添加剂的性质取决于溶质的分子式。添加特性的一个示例是“质量”。
- 发表于 2021-09-15 17:07
- 阅读 ( 257 )
- 分类:化学
你可能感兴趣的文章
摩尔浓度(molarity)和摩尔浓度(molality)的区别
...物质(称为溶质)的摩尔数,这种物质精确地溶解在1升溶液中(溶剂和溶质的结合)。 因此,计算摩尔浓度的公式如下: M=摩尔溶质/L溶液 摩尔浓度通常也被称为摩尔浓度。因此,摩尔浓度的量度是基于物质溶解在其中的液体...
- 发布于 2021-06-25 05:46
- 阅读 ( 568 )
渗透压(osmotic pressure)和膨胀压(oncotic pressure)的区别
...压之间的主要区别在于,渗透压是阻止水通过分隔溶剂和溶液的渗透膜的净运动所需的压力,而溶胀压是胶体对总渗透压的贡献。在这篇文章中,将讨论渗透压和溶胀压之间的差异。 什么是渗透压(o**otic pressure)? 渗透压是指阻...
- 发布于 2021-06-27 10:21
- 阅读 ( 780 )
静水压(hydrostatic)和渗透压(osmotic pressure)的区别
...水压存在于任何类型的均质流体中,而渗透压不存在于纯溶液中。 覆盖的关键领域 1.什么是静水压-定义、特征、方程和计算2.什么是渗透压-定义、特征、方程和计算3.静水压和渗透压的区别是什么-主要区别的比较 Key Terms: Homogen...
- 发布于 2021-06-28 20:11
- 阅读 ( 1042 )
真正的解决方案(true solution)和胶体溶液(colloidal solution)的区别
主要差异真解(main difference true solution) vs. 胶体溶液(colloidal solution) 化学中的溶液是含有两种或两种以上物质的液体混合物。有些溶液是无色的,有些是彩色的。一些解决方案是透明的,而另一些解决方案是不透明的。同...
- 发布于 2021-06-28 20:49
- 阅读 ( 560 )
理想溶液(ideal solution)和非理想溶液(non ideal solution)的区别
主差理想解(main difference ideal solution) vs. 非理想溶液(non ideal solution) 理想溶液是具有与理想气体混合物相似性质的溶液。然而,理想气体中气体分子之间没有相互作用。但是我们不能在溶液中考虑同样的情况,因为溶液中...
- 发布于 2021-06-29 11:30
- 阅读 ( 704 )
初级的(primary)和二级标准溶液(secondary standard solution)的区别
主要差异主要(main difference primary) vs. 二级标准溶液(secondary standard solution) 标准化是指以标准溶液为参照物,求出配制溶液的准确浓度。标准溶液是使用标准物质制备的精确已知浓度的溶液。有两种标准溶液,称为一次溶液和二...
- 发布于 2021-06-29 17:29
- 阅读 ( 636 )
渗透作用(osmosis)和透析(dialysis)的区别
...何液体通过选择性渗透膜的物理相,该膜将两种不同量的溶液分开。使渗透作用发挥作用是可能的。施加外部压力的方式必须确保溶剂不会通过被称为渗透压的膜发生绝对运动。渗透压是一种具有依数性质的现象。这意味着它是...
- 发布于 2021-07-11 17:05
- 阅读 ( 203 )
为什么用摩尔浓度代替摩尔浓度?
摩尔浓度(m)和摩尔浓度(m)都表示化学溶液的浓度。摩尔浓度是每千克溶剂中溶质的摩尔数。摩尔浓度是每升溶液中溶质的摩尔数。如果溶剂为水且溶质浓度相当低(即稀释溶液),则摩尔浓度和摩尔浓度大致相同。然而,...
- 发布于 2021-09-06 21:49
- 阅读 ( 121 )
凝固点下降示例问题
此示例问题演示如何使用水中的盐溶液计算冰点降低。 关键要点:计算冰点下降 凝固点降低是溶液的一种性质,溶质会降低溶剂的正常凝固点。 冰点降低仅取决于溶质浓度,而不是其质量或化学特性。 冰点降低的一个常...
- 发布于 2021-09-07 23:26
- 阅读 ( 281 )
你为什么在沸水里加盐?
...热盐水时,你会得到溶质(盐,它的热容很低)在水中的溶液。基本上,在20%的盐溶液中,你失去了太多的加热阻力,盐水沸腾得更快。 煮沸后加盐 有些人喜欢在水煮沸后加盐。显然,这根本不会加快沸腾的速度,因为盐是...
- 发布于 2021-09-08 07:35
- 阅读 ( 316 )