凝固点下降示例问题
此示例问题演示如何使用水中的盐溶液计算冰点降低。

关键要点:计算冰点下降
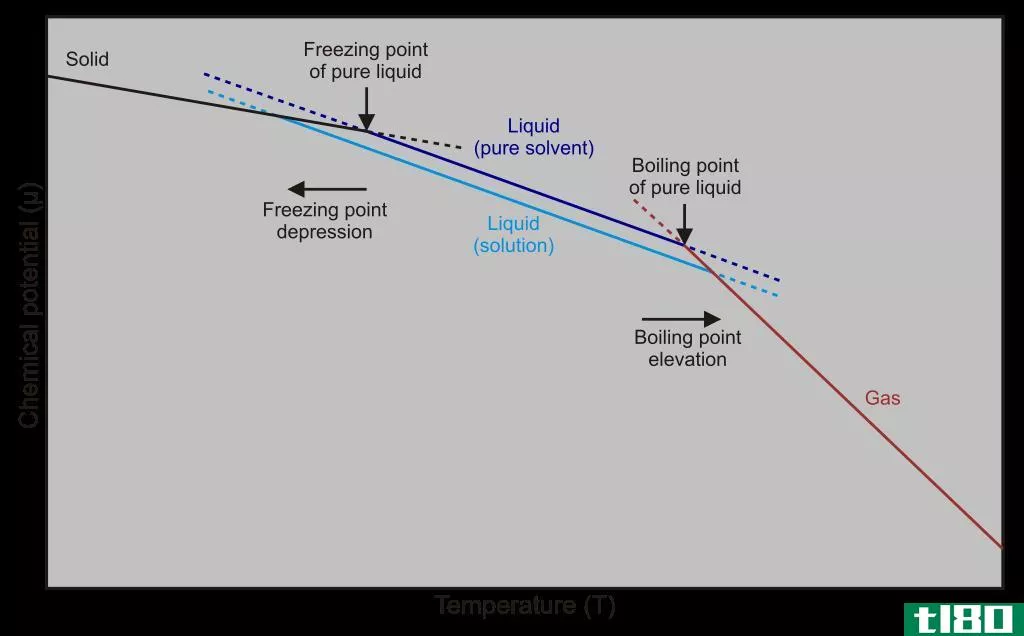
- 凝固点降低是溶液的一种性质,溶质会降低溶剂的正常凝固点。
- 冰点降低仅取决于溶质浓度,而不是其质量或化学特性。
- 冰点降低的一个常见例子是盐降低水的冰点,以防止道路上的冰在低温下结冰。
- 该计算使用了一个称为Blagden定律的方程,它结合了拉乌尔定律和克劳修斯-克拉佩龙方程。
冰点降低的快速回顾
凝固点降低是物质的依数性质之一,这意味着它受粒子数量的影响,而不是粒子的化学特性或它们的质量。当溶质添加到溶剂中时,其凝固点会从纯溶剂的原始值降低。溶质是液体、气体还是固体并不重要。例如,当向水中添加盐或酒精时,会发生冰点降低。事实上,溶剂也可以是任何相。凝固点降低也发生在固体混合物中。
使用拉乌尔定律和克劳修斯-克拉佩龙方程计算冰点下降,并写出一个称为布拉格登定律的方程。在理想溶液中,冰点降低仅取决于溶质浓度。
冰点下降问题
将31.65 g氯化钠添加到温度为34°C的220.0 mL水中。这将如何影响水的冰点?假设氯化钠在水中完全解离。给定:35°C下的水密度=0.994 g/mLKf水=1.86°C kg/mol
解决方案
为了找出溶质引起的溶剂温度变化升高,使用冰点降低方程:ΔT=IKfm,其中ΔT=温度变化,单位为°Ci=van’T Hoff系数Kf=摩尔冰点降低常数或冰点降低常数,单位为°C kg/molm=溶质摩尔浓度/kg溶剂。
步骤1:计算氯化钠的摩尔浓度
NaCl的摩尔浓度(m)=周期表中NaCl的摩尔数/kg水,求元素的原子质量:原子质量Na=22.99原子质量Cl=35.45摩尔氯化钠=31.65克x1摩尔/(22.99+35.45)摩尔氯化钠=31.65克x1摩尔/58.44克氯化钠=0.542摩尔千克水=密度x体积克水=0.994克/毫升x220毫升x1千克/1000克水=0.219千克氯化钠=0.542摩尔/0.219千克水2.477 mol/kg
步骤2:确定范特霍夫系数
范特霍夫系数i是一个常数,与溶剂中溶质的离解量有关。对于在水中不解离的物质,如糖,i=1。对于完全解离成两个离子的溶质,i=2。对于本例,NaCl完全解离成两个离子,Na+和Cl-。因此,对于本例,i=2。
步骤3:找到δt
ΔT=iKfmΔT=2 x 1.86°C kg/mol x 2.477 mol/kgΔT=9.21°C罐:向220.0 mL水中添加31.65 g NaCl将使冰点降低9.21°C。
凝固点下降计算的局限性
计算冰点下降具有实际应用,例如制作冰淇淋、药品和道路除冰。然而,这些方程式仅在某些情况下有效。
- 溶质的含量必须比溶剂低得多。凝固点降低计算适用于稀溶液。
- 溶质必须是非挥发性的。原因是当液体和固体溶剂的蒸汽压处于平衡状态时,会出现凝固点。
来源
- 彼得·阿特金斯(2006)。阿特金斯的物理化学。牛津大学出版社。第150-153页。ISBN 0198700725。
- 戈登·艾尔沃德;特里斯坦芬德利(2002年)。SI化学数据(第五版)。瑞典:约翰·威利父子公司。P202.ISBN 0-470-80044-5。
- 葛新雷,;王希东(2009)。”电解质溶液冰点降低、沸点升高和蒸发焓的估算”。工业与工程化学研究。48(10):5123.内政部:10.1021/ie900434h
- 约瑟夫·威廉·梅勒(1912年)。”布莱登定律”。现代无机化学。纽约:朗曼、格林和公司。
- 佩特鲁奇,拉尔夫H。;威廉·S·哈伍德。;海岭,F。杰弗里(2002年)。普通化学(第8版)。普伦蒂斯大厅。第557-558页。ISBN 0-13-014329-4。
- 发表于 2021-09-07 23:26
- 阅读 ( 277 )
- 分类:数学
你可能感兴趣的文章
融合(fusion)和凝固(solidification)的区别
...查阅。赫尔曼斯汀,安妮·玛丽。“化学中凝固的定义和示例”,ThoughtCo,2019年8月11日,可在此处查阅。2赫尔曼斯汀,安妮·玛丽。“化学中凝固的定义和实例”,ThoughtCo,2019年8月11日, img.centered,.aligncenter{display:block;mar...
- 发布于 2020-10-15 02:09
- 阅读 ( 200 )
冰点降低(freezing point depression)和沸点升高(boiling point elevation)的区别
关键区别——冰点降低与沸点升高 由于添加了溶质,凝固点降低导致溶液在低于纯溶剂冰点的温度下冻结。由于溶质的加入,使溶液在比纯溶剂沸点更高的温度下沸腾。因此,冰点降低和沸点升高之间的关键区别在于,冰点...
- 发布于 2020-10-19 04:06
- 阅读 ( 535 )
如何找到摩尔质量(find the molar mass)
...算摩尔质量 方法3:从沸点升高计算摩尔质量 方法4:从凝固点下降计算摩尔质量 方法5:根据渗透压计算摩尔质量 下面将详细讨论这些方法。 1.如何用原子质量求摩尔质量 分子的摩尔质量可以用原子质量来确定。这可以简单地...
- 发布于 2021-06-28 19:41
- 阅读 ( 264 )
消化(peptization)和凝结(coagulation)的区别
...*体的形成。 覆盖的关键领域 1.什么是消化-定义,过程,示例2.什么是凝固-定义,过程3.消化和凝固的区别是什么-关键区别的比较 关键词:混凝,胶体,胶体分散体,电解质,胶溶,胶溶剂 什么是消化(peptization)? 胶溶是在分...
- 发布于 2021-06-29 17:56
- 阅读 ( 272 )
火成岩沉积岩,(igneous, sedimentary,)和变质岩(metamorphic rocks)的区别
...岩。变质岩可分为两大类:叶理变质岩和非叶理变质岩。示例侵入火成岩包括花岗岩、闪长岩、伟晶岩;喷出火成岩包括玄武岩、凝灰岩、浮石、火山渣等。石灰石、铁矿石、白垩、煤、砂岩、粉砂岩、页岩、燧石等。板岩、大...
- 发布于 2021-07-10 04:26
- 阅读 ( 400 )
岩石(rocks)和矿物(minerals)的区别
...体机能,帮助骨骼和牙齿的形成,血液凝固,肌肉收缩 示例 花岗岩、石灰岩、砾岩、砂岩等。 金、银、氟化物、石英、云母、长石等。
- 发布于 2021-07-14 00:43
- 阅读 ( 161 )
冰点(freezing point)和冰点降低(freezing point depression)的区别
...冰点降低是由于溶剂中加入溶质而使溶剂的冰点降低。 凝固点是物质从液相向固相发生相变的温度值。在大多数情况下,它类似于固体转化为液态的物质的熔点。 目录 1. 概述和主要区别 2. 冰点是多少 3. 什么是冰点降低 4. ...
- 发布于 2021-07-14 05:29
- 阅读 ( 559 )
用盘子检查你的肉汁是否“做好”
...了五分钟的盘子上,然后把盘子竖直放着。如果果酱慢慢下降,就结束了(你也可以把果酱放在盘子上,然后把盘子放进冰箱。如果几分钟后就凝固了,你应该很好。)对于酱汁和肉汁,你不需要盘子这么冷。这两种食物通常都...
- 发布于 2021-08-03 08:32
- 阅读 ( 156 )
菠萝破坏明胶背后的科学
...凝固。幸运的是,很容易使酶失活,这样它们就不会引起问题。 用菠萝加热 你仍然可以使用新鲜水果和明胶,你只需要先加热使蛋白质分子变性。菠萝蛋白酶在加热到约158°F(70°C)时会失活,因此新鲜菠萝可以防止果冻凝...
- 发布于 2021-09-06 23:21
- 阅读 ( 392 )
常见的一般化学问题列表
...压强 自由能与反应自发性 形式电荷路易斯结构共振结构 凝固点降低 频率-波长转换 格雷厄姆定律 克摩尔转换 盖伊·卢萨克气体定律 h:焦耳到e的半衰期:电子伏特转换 半衰期 生成热 Henderson-Hasselbalch方程 亨利定律 赫斯定...
- 发布于 2021-09-08 10:26
- 阅读 ( 255 )