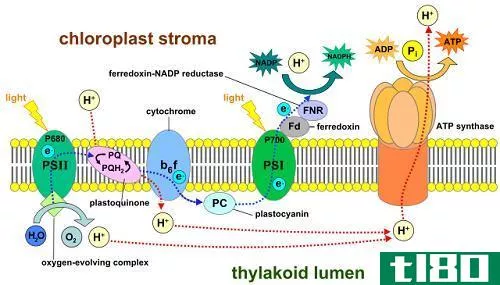
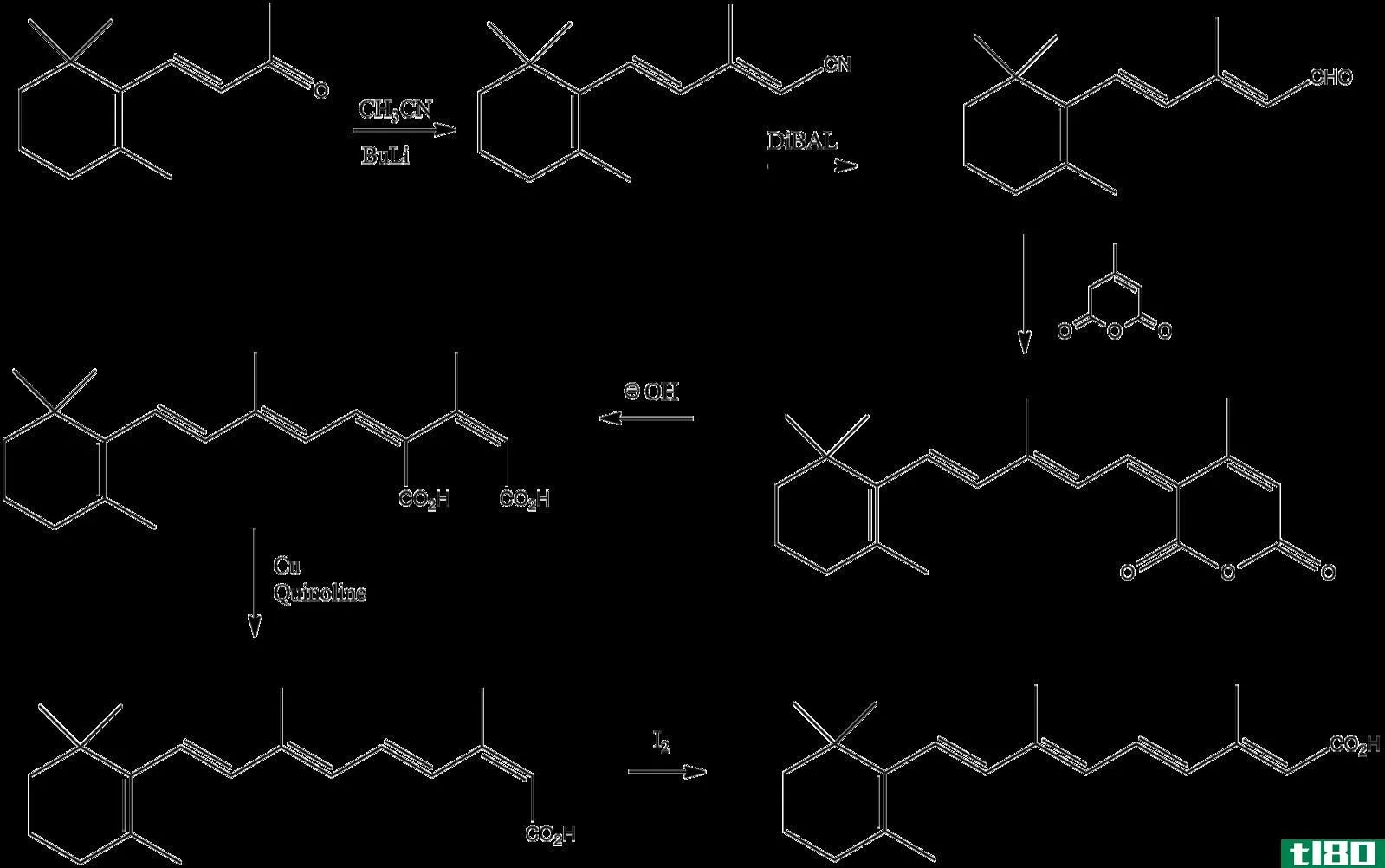
铁氧还蛋白和红霉素之间的关键区别在于,铁氧还蛋白的氧化还原电位比红细胞还原素低得多。
铁氧还蛋白和红霉素都是含铁蛋白。然而,我们可以在细菌和植物中发现铁氧还蛋白,因为它是一种叶绿体蛋白。然而,Rubredoxin是一种只存在于细菌和古细菌中的蛋白质。这两种化合物的结构非常相似。
目录
1. 概述和主要区别
2. 什么是铁氧还蛋白
3. 什么是红霉素
4. 并列比较-铁氧还蛋白与红霉素的表格形式
5. 摘要
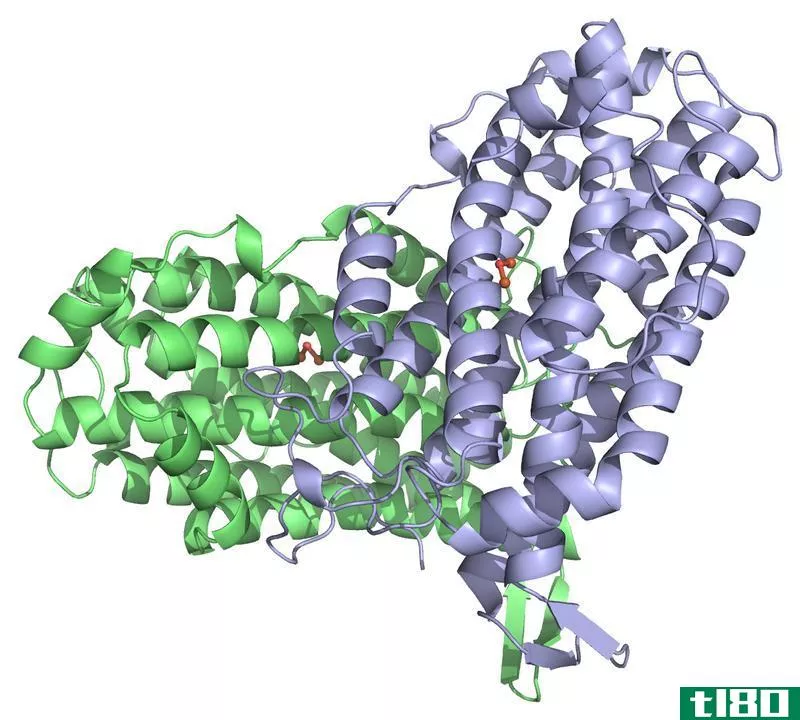
什么是铁氧还蛋白(ferredoxin)?
铁氧还蛋白是一种含铁硫的蛋白质。它参与调节各种代谢反应中的电子转移。这些是水溶性的小蛋白质,存在于叶绿体中。这种蛋白质中的铁和硫原子排列成铁硫簇。它们可以通过接受和释放电子来充当生物电容器。在这里,铁原子的氧化状态从+2变为+3。因此,它们在生物环境中的氧化还原反应中充当电子转移剂。相对而言,该蛋白的氧化还原电位较低。一个铁氧还蛋白分子可以包含两个,三个或四个铁原子每个蛋白质分子。铁氧还蛋白有三种常见类型:Fe2S2铁氧还蛋白、Fe4S4铁氧还蛋白和Fe3S4铁氧还蛋白。
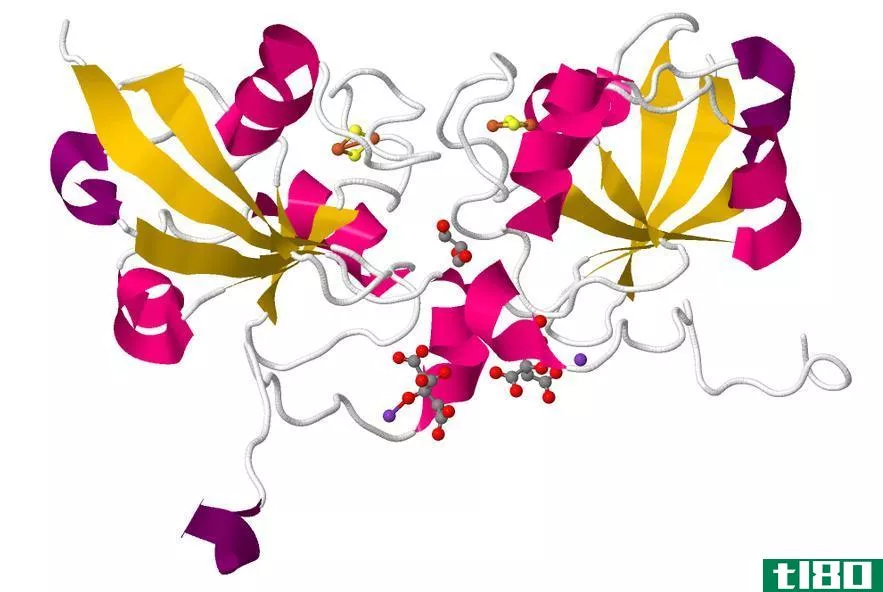
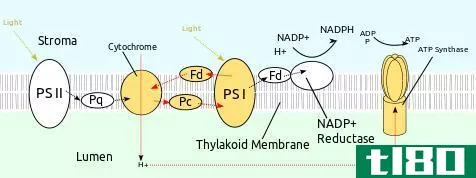
铁氧还蛋白的主要作用是在叶绿体中分配高能电子,这些蛋白质参与分配二氧化碳固定、腈还原、亚硫酸盐还原、谷氨酸合成、循环电子流等所需的电子。
什么是红霉素(rubredoxin)?
Rubredoxin是一种含铁的蛋白质,存在于细菌和古细菌中。它是一种低分子量蛋白质(通常蛋白质是高分子量化合物)。然而,与铁氧还蛋白不同,Rubredoxin蛋白质不含无机硫化物。Rubredoxin的主要作用是参与生物系统中发生的氧化还原反应中的电子转移机制。
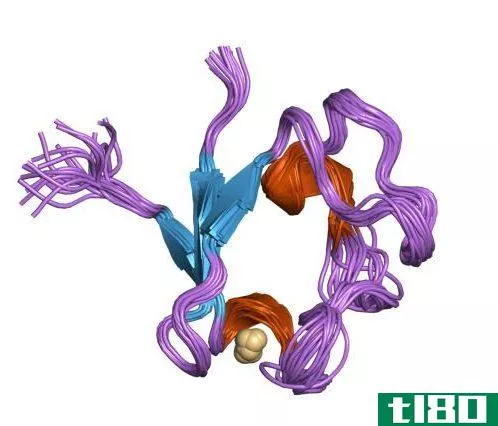
当考虑到Rubredoxin的结构时,它包含一个几乎四面体的中心铁原子。与这个铁原子结合的四个基团是半胱氨酸残基。红霉素蛋白大多为水溶性化学物质。然而,也有一些不溶性物质以膜结合蛋白的形式存在。E、 红曲霉毒素A。
在电子转移机制中,中心铁原子的氧化态从+2变为+3。我们很容易识别出氧化状态的这种变化,因为颜色从红色变为无色。在这种变化过程中,金属离子保持在高自旋状态,因为它有助于将蛋白质的结构变化降到最低。通常,红霉素的还原电位高于铁氧还蛋白,其范围在+50 mV至-50 mV之间。
铁氧还蛋白(ferredoxin)和红霉素(rubredoxin)的区别
铁氧还蛋白和红细胞还原蛋白是一种既含有铁又含有硫的蛋白质化合物。铁氧还蛋白和红霉素之间的关键区别在于,铁氧还蛋白的氧化还原电位比红细胞还原素低得多。铁氧还蛋白的氧化还原电位约为-420mv,而Rubredoxin的氧化还原电位为-50~+50mv。此外,铁氧还蛋白在每个蛋白质分子中可以含有2个、3个或4个铁原子,但在Rubredoxin中,只有一个中心铁原子。然而,这两种分子在铁原子周围有着非常相似的四面体几何形状。
此外,铁氧还蛋白分子中含有无机硫,而红血球蛋白中不含无机硫。考虑到铁氧还蛋白的存在,铁氧还蛋白可以以细菌的形式存在于植物中,而红霉素则存在于细菌和古细菌中。
下表总结了铁氧还蛋白和红霉素的区别。
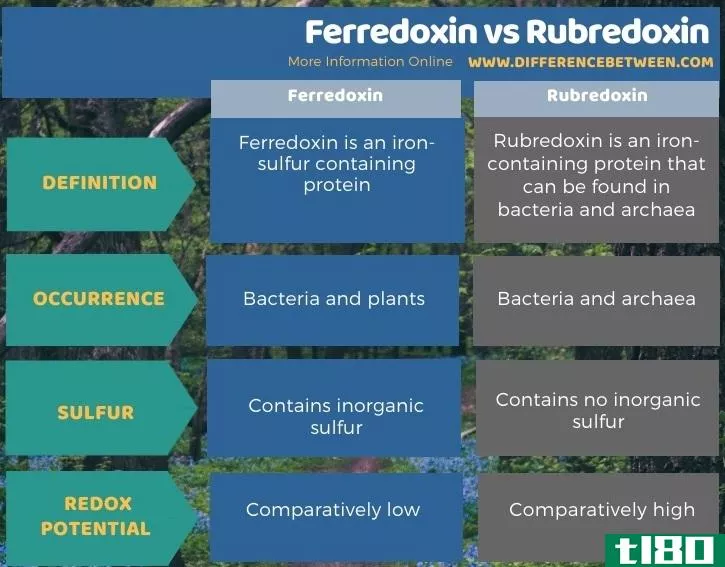
总结 - 铁氧还蛋白(ferredoxin) vs. 红霉素(rubredoxin)
铁氧还蛋白和红细胞还原蛋白是一种既含有铁又含有硫的蛋白质化合物。铁氧还蛋白和红霉素之间的关键区别在于,铁氧还蛋白的氧化还原电位比红细胞还原素低得多。
引用
1铁的性质与测定〉,《食品科学与营养百科全书》,2003年,第3367-3373页。,doi:10.1016/b0-12-227055-x/00650-7。