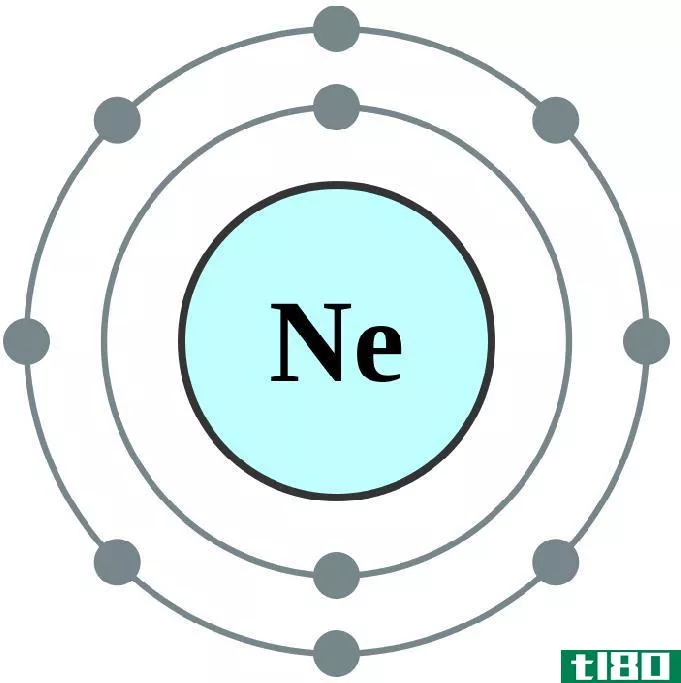
如何寻找价电子(find valence electrons)
第1部分第1部分,共2部分:用周期表寻找价电子
非过渡金属
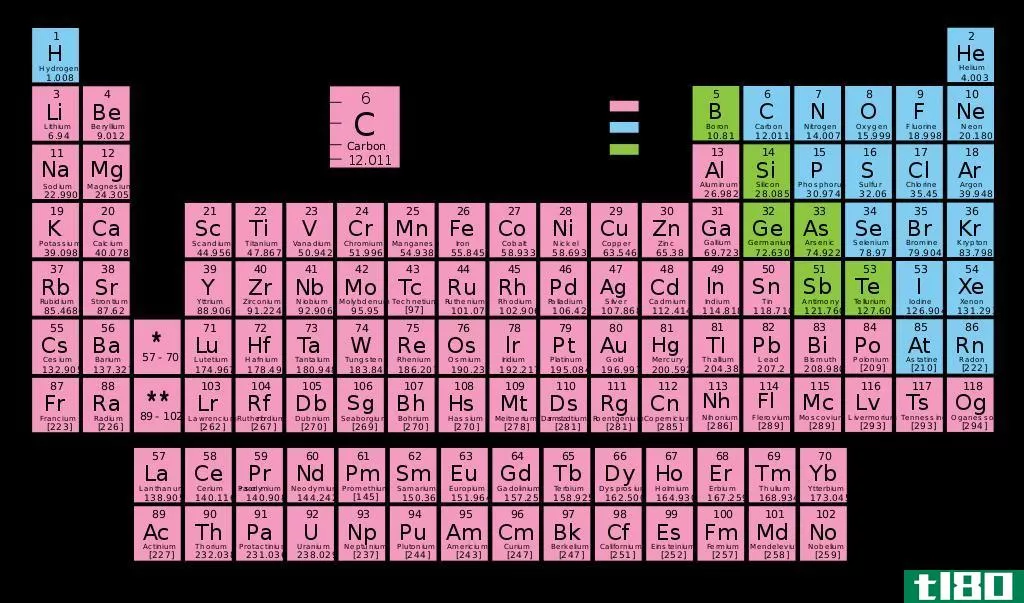
- 1找到元素周期表。这是一个由许多不同方块组成的彩色编码表格,列出了人类已知的所有化学元素。元素周期表揭示了许多关于元素的信息——我们将使用其中的一些信息来确定我们正在研究的原子中价电子的数量。你通常可以在化学教科书的封面上找到这些。这里还有一个很好的在线互动表格。
- 2将元素周期表上的每一列标记为1到18。一般来说,在周期表上,单个垂直列中的所有元素的价电子数都相同。如果你的元素周期表还没有对每一列进行编号,那么给每一列一个数字,最左端从1开始,最右端从18开始。用科学术语来说,这些列被称为元素“组”例如,如果我们使用的是一个元素周期表,其中的基团没有编号,我们会在氢(H)上写1,在铍(Be)上写2,依此类推,直到在氦(He)上写18。
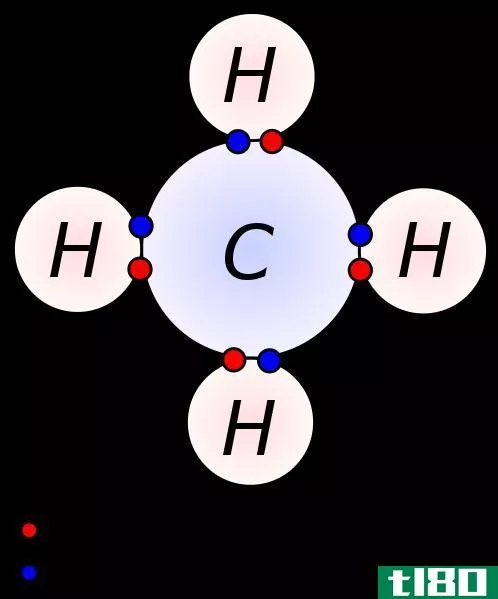
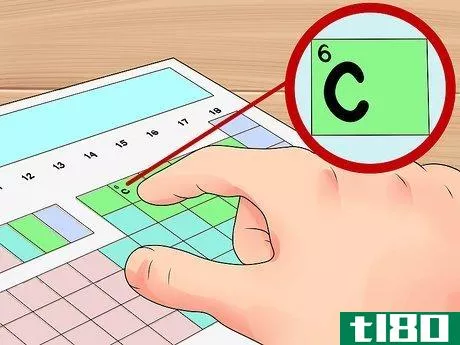
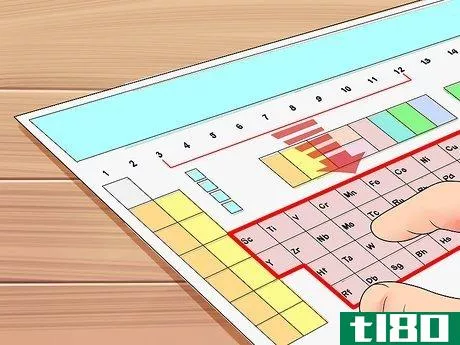
- 3.在桌子上找到你的元素。现在,找到你想在桌子上找到价电子的元素。你可以用它的化学符号(每个方框中的字母)、原子序数(每个方框左上角的数字)或桌子上的任何其他信息来实现这一点。例如,让我们找到一种非常常见的元素:碳(C)的价电子。这个元素的原子序数是6。它位于第14组的顶部。下一步,我们将找到它的价电子。在这一小节中,我们将忽略过渡金属,它们是由3到12组组成的矩形块中的元素。这些元素与其他元素略有不同,因此本小节中的步骤对它们不起作用。请参阅下面小节中如何处理这些问题。
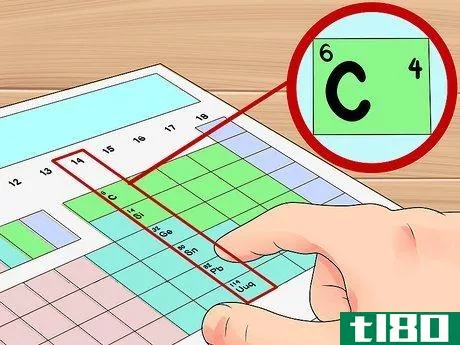
- 4使用组号确定价电子的数量。非过渡金属的基团数可以用来计算该元素原子的价电子数。族数的一个位置是这些元素的原子中价电子的数量。换句话说,第一组:1价电子第二组:2价电子第13组:3价电子第14组:4价电子第15组:5价电子第16组:6价电子第17组:7价电子第18组:8价电子(氦除外,它有2个)在我们的例子中,因为碳在第14组中,我们可以说一个碳原子有四个价电子。

过渡金属
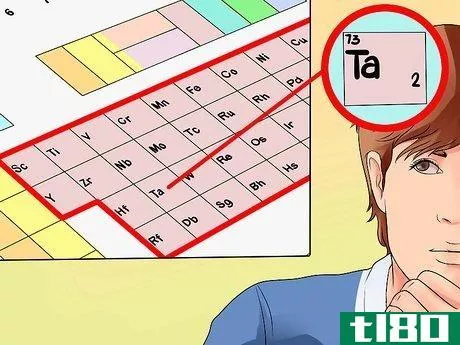
- 1从组3到组12中查找一个元素。如上所述,第3组到第12组中的元素被称为“过渡金属”,当涉及价电子时,它们的行为与其他元素不同。在本节中,我们将解释,在一定程度上,通常不可能将价电子分配给这些原子。例如,让我们选择钽(Ta),元素73。在接下来的几个步骤中,我们将找到它的价电子(或者,至少,试着找到。)请注意,过渡金属包括镧系元素和锕系元素(也称为“稀土金属”)——这两行元素通常位于表中以镧和锕开始的其余元素的下方。这些元素都属于元素周期表的第三组。
- 2了解过渡金属没有“传统”价电子。要理解为什么过渡金属不能像周期表的其他部分那样真正“工作”,就需要对电子在原子中的行为做一点解释。请参阅下面的快速浏览或跳过此步骤以获得正确答案。当电子被添加到原子中时,它们被分成不同的“轨道”——电子聚集在原子核周围的基本不同区域。一般来说,价电子是最外层的电子——换句话说,是最后添加的电子。由于这里难以解释的原因,当电子被添加到过渡金属的最外层d壳层时(下文将对此进行详细介绍),进入壳层的第一个电子倾向于像正常价电子一样工作,但在这之后,它们就不会了,来自其他轨道层的电子有时会充当价电子。这意味着一个原子可以有多个价电子,这取决于它的操控方式。
- 3根据基团数确定价电子数。再一次,你正在检查的元素的组号可以告诉你它的价电子。然而,对于过渡金属,没有一种模式可以遵循——基团数通常对应于一系列可能的价电子数。这些是:组3:3价电子组4:2-4价电子组5:2-5价电子组6:2-6价电子组7:2-7价电子组8:2或3价电子组9:2或3价电子组10:2或3价电子组11:1或2价电子组12:2价电子在我们的例子中,因为钽在组5中,我们可以说它有两到五个价电子,这取决于具体情况。
第2部分第2部分,共2部分:用电子构型寻找价电子
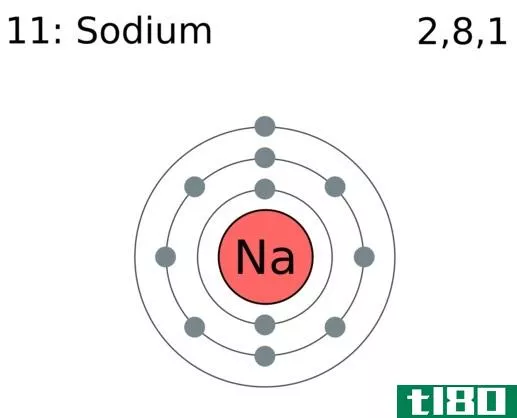
- 1了解如何读取电子配置。另一种找到元素价电子的方法是用一种叫做电子构型的东西。这些一开始看起来可能很复杂,但它们只是用字母和数字来表示原子中的电子轨道的一种方式,一旦你知道你在看什么,它们就很容易了。让我们来看元素钠(Na)的一个示例配置:1S222S22P63S1注意,这个电子配置只是一个重复的字符串,如下所示:(数字)(字母)(凸起的数字)(数字)(字母)(凸起的数字)。。。。。。等等(数字)(字母)区块是电子轨道的名称,(凸起的数字)是该轨道中的电子数-就是这样!例如,我们可以说钠在1s轨道上有2个电子,在2s轨道上有2个电子,在2p轨道上有6个电子,在3s轨道上有1个电子。总共是11个电子——钠是元素数11,所以这是有意义的。请记住,每个子壳层都有一定的电子容量。它们的电子容量如下:s:2电子容量P:6电子容量D:10电子容量Y:14电子容量
- 2查找所检查元素的电子配置。一旦你知道一种元素的电子构型,就很容易找到它的价电子数(当然,过渡金属除外)如果你一开始就得到了配置,你可以跳到下一步。如果你必须自己找到它,请看下面:检查元素118的完整电子构型,它是周期表上的最后一个元素。它拥有所有元素中最多的电子,所以它的电子构型展示了你在其他元素中可能遇到的所有可能性:1S222S22P63S23P64S23D104P65S24D105P66S24F145D106P67S25F146D107P6既然你有了这个,你只需要从一开始就填充这个模式,直到你用完电子。这比听起来容易。例如,如果我们想绘制氯(Cl)的轨道图,元素17有17个电子,我们会这样做:1S222S22P63S23P5注意,电子数加起来是17:2+2+6+2+5=17。你只需要改变最后一个轨道上的数字,其余的都一样,因为最后一个轨道之前的轨道已经完全满了。有关电子配置的更多信息,请参阅本文。
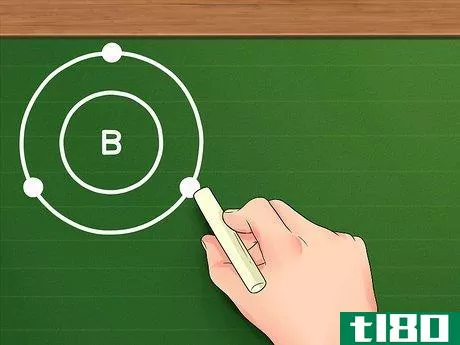
- 3用八重态规则将电子分配到轨道壳层。当电子被加到一个原子上时,它们会按照上面给出的顺序落入不同的轨道——前两个进入1s轨道,后两个进入2s轨道,后六个进入2p轨道,依此类推。当我们处理过渡金属之外的原子时,我们说这些轨道围绕着原子核形成“轨道壳”,每个连续的壳都比之前的壳更远。除了第一个壳层只能容纳两个电子外,每个壳层可以有八个电子(同样,当处理过渡金属时除外)这被称为八位组规则。例如,假设我们正在研究元素硼(B)。因为它的原子序数是五,我们知道它有五个电子,它的电子构型是这样的:1S22S2P1。由于第一个轨道壳层只有两个电子,我们知道硼有两个壳层:一个有两个1s电子,另一个有来自2s和2p轨道的三个电子。再举一个例子,像氯这样的元素(1S222S22P63S23P5)将有三个轨道壳:一个有两个1s电子,一个有两个2s电子和六个2p电子,一个有两个3s电子和五个3p电子。
- 4找出最外层的电子数。既然你知道了元素的电子壳层,那么找到价电子就很容易了:只需使用最外层壳层中的电子数即可。如果外壳是满的(换句话说,如果它有八个电子,或者第一个外壳有两个电子),元素是惰性的,不容易与其他元素发生反应。然而,对于过渡金属来说,情况并没有完全遵循这些规则。例如,如果我们研究硼,因为在第二个壳层中有三个电子,我们可以说硼有三个价电子。
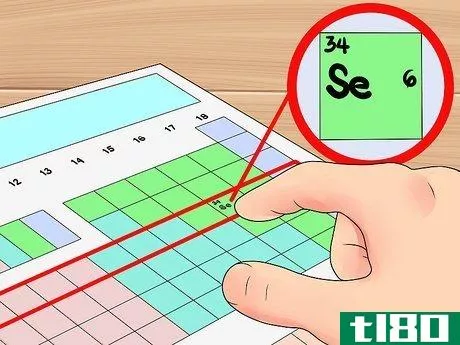
- 5.使用表中的行作为轨道壳快捷方式。元素周期表的水平行称为元素“周期”从表的顶部开始,每个周期对应于该周期中原子所拥有的电子壳层的数量。你可以用它作为一个快捷方式来确定一个元素有多少个价电子——在计算电子时,只需从周期的左侧开始。再一次,你需要用这种方法忽略过渡金属,包括3-12组。例如,我们知道元素硒有四个轨道壳,因为它处于第四周期。由于它是第四个周期中从左边算起的第六个元素(忽略过渡金属),我们知道外层第四层有六个电子,因此硒有六个价电子。
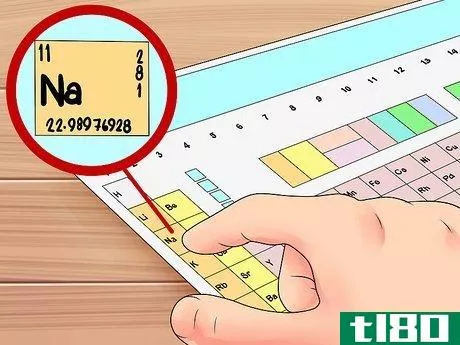


- 请注意,电子构型可以用一种简写法写成,即使用惰性气体(第18组中的元素)代表构型开始时的轨道。例如,钠的电子构型可以写成[Ne]3s1——本质上,它与氖相同,但在3s轨道上还有一个电子。
- 过渡金属可能具有未完全填充的价次壳层。确定过渡金属中价电子的确切数目涉及量子理论的原理,这超出了本文的范围。
- 请注意元素周期表因国家而异。因此,请检查您使用的是正确的更新版本,以避免混淆。
- 一定要知道什么时候从最后一个轨道上加或减才能找到价电子。
- 发表于 2022-03-28 00:19
- 阅读 ( 56 )
- 分类:教育
你可能感兴趣的文章
价壳(valence shell)和倒数第二壳(penultimate shell)的区别
... 价壳层是原子最外层的电子壳。这个壳层中的电子称为价电子。这些电子对原子核的吸引力最小。这是因为价电子与原子的其他电子相比,位于远离核的很长的距离。 图01:参与键形成的价电子 价壳层中的电子负责原子的化学...
- 发布于 2020-09-26 17:01
- 阅读 ( 879 )
价(valency)和氧化值(oxidation number)的区别
...一个原子形成键而可以失去或获得的电子数。 氧化数和价电子与原子的价电子有关。价电子是占据原子最外层轨道的电子。这些电子对原子核的吸引力很弱;因此,原子可以很容易地移除或与其他原子共享这些电子。这种电子...
- 发布于 2020-10-15 12:44
- 阅读 ( 312 )
价带(valence band)和导带(conduction band)的区别
...电子的物质原子的最外层电子轨道。此外,这一术语与“价电子”一词密切相关。 什么是导带(conduction band)? 导带是部分充满电子的晶体固体中能级的非定域带。这些电子具有很大的迁移率,并负责导电性。这里,导带是电子...
- 发布于 2020-10-17 00:55
- 阅读 ( 1583 )
激进的(radical)和价(valency)的区别
...自由基是一种具有不成对电子的化学物质。未成对电子是价电子。也就是说,它在原子的最外层。自由基可以是原子、分子或离子。由于不成对电子的存在是不稳定的,自由基是非常活泼的化学物质。因此,这些化学物质的寿命...
- 发布于 2020-10-17 02:38
- 阅读 ( 414 )
原子价(valence)和核心电子(core electrons)的区别
价电子和核心电子之间的关键区别在于,价电子参与化学键的形成,而核心电子不参与化学键的形成。 原子是所有现存物质的组成部分。它们太小了,我们甚至不能用肉眼观察它们。一般来说,原子在埃范围内。原子是由原...
- 发布于 2020-10-22 12:42
- 阅读 ( 1139 )
价(valency)和指控(charge)的区别
...控(charge)的区别 价表示原子的反应性,而电荷则表示原子如何反应。因此,价态和电荷的关键区别在于,价态表示一种化学元素与另一种化学元素结合的能力,而电荷则表示一种化学元素获得或移除的电子数。 此外,价的值没...
- 发布于 2020-10-23 02:08
- 阅读 ( 361 )
价(valency)和价电子(valence electrons)的区别
s价(s valency)和价电子(valence electr***)的区别 价电子和价电子是相互关联的术语,价电子和价电子之间的关键区别在它们的定义中得到了最好的解释;价电子是元素最外层壳层中的电子,而价电子是为了达到最接近的目的而应...
- 发布于 2020-10-24 18:09
- 阅读 ( 1005 )
分子轨道理论(molecular orbital theory)和价键理论(valence bond theory)的区别
...道都被填满时,电子会进入反键轨道。 什么是价键理论(valence bond theory)? 价键理论是基于局域键方法,它假定分子中的电子占据单个原子的原子轨道。例如,在H2分子的形成过程中,两个氢原子重叠了它们的1s轨道。通过重叠两...
- 发布于 2020-11-03 20:05
- 阅读 ( 472 )
配价(valency)和价电子(valence electrons)的区别
主差价(main difference valency) vs. 价电子(valence electr***) 尽管这两个术语,价电子和价电子之间有着非常密切的联系,但两者之间还是有细微的差别价态在化学中的文学意义是与容量有关的。用化学术语来说,元素的价态是...
- 发布于 2021-06-27 10:49
- 阅读 ( 628 )
离子共价(ionic covalent)和金属键(metallic bonds)的区别
...个原子在金属晶格**享可变数量的电子时,两个原子共享价电子和金属键时形成共价键。 本文探讨, 1.什么是离子键?–定义、形成、性质 2.什么是共价键?–定义、形成、性质 3.什么是金属键?–定义、形成、性质 4. What is the...
- 发布于 2021-06-28 11:41
- 阅读 ( 825 )