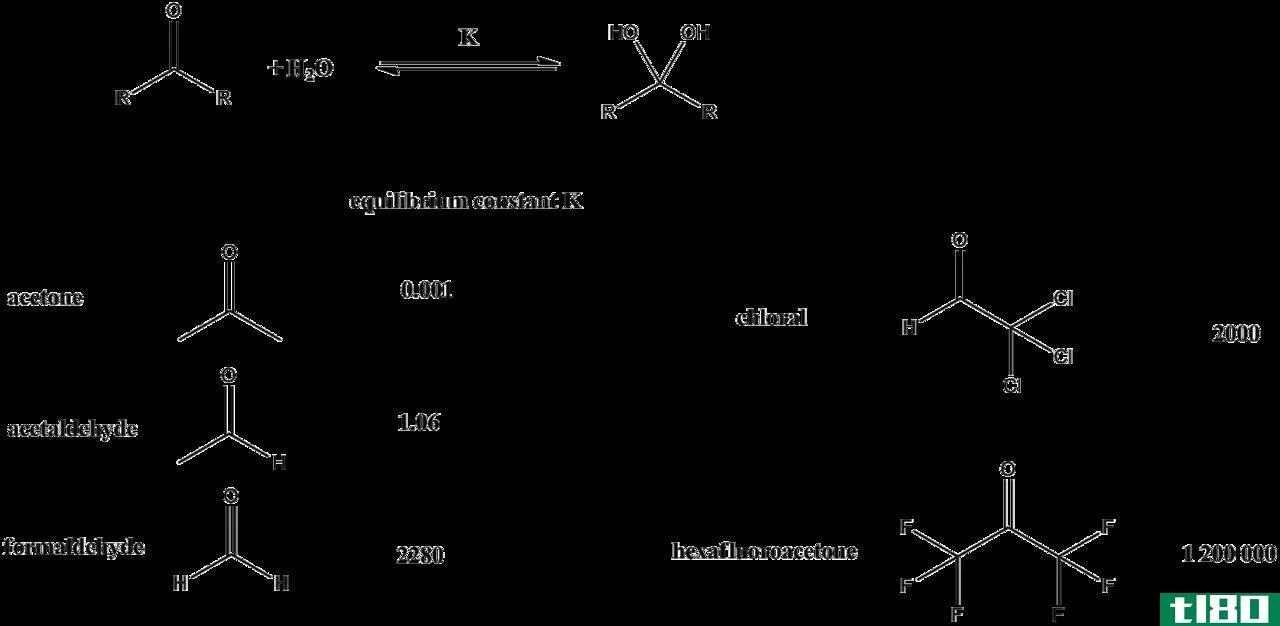
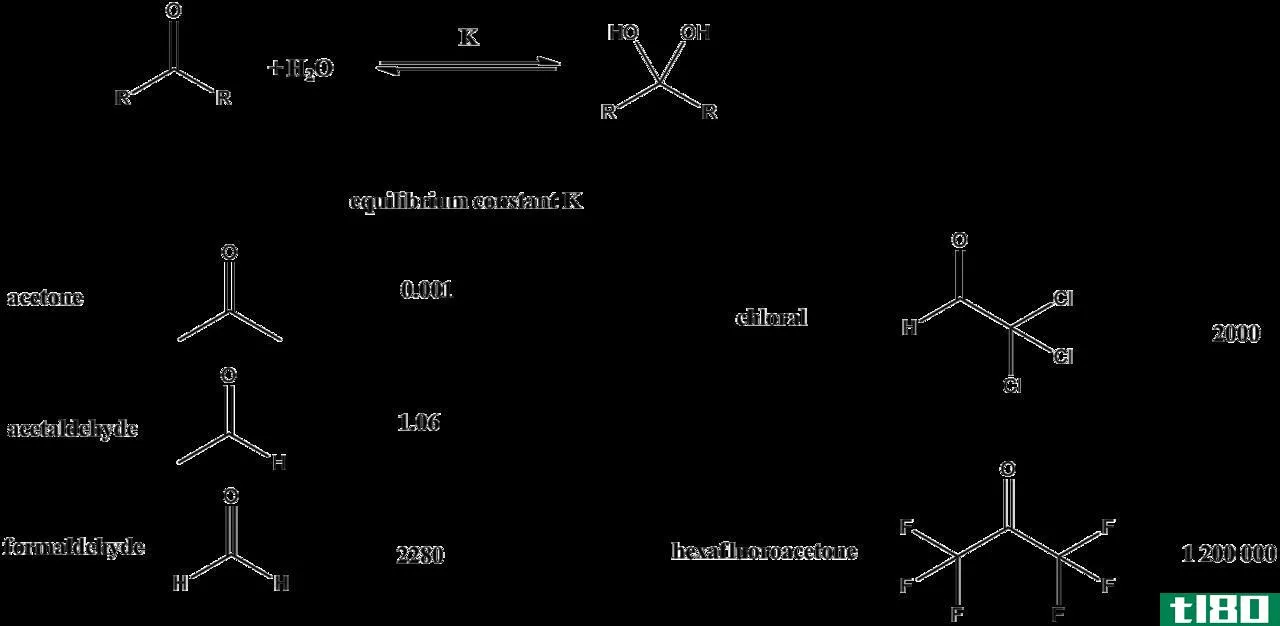
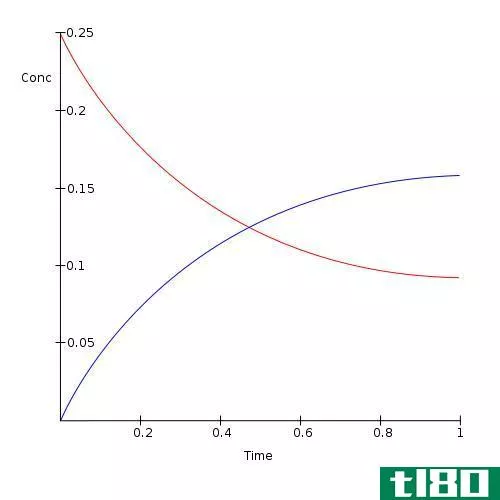
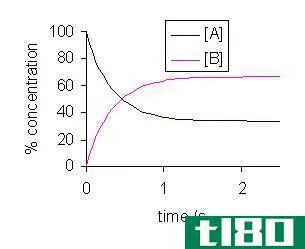
平衡常数与反应商
有些反应是可逆的,有些反应是不可逆的。反应物转化为反应物。在某些反应中,反应物可以从产物中再次生成。这种反应称为可逆反应。在不可逆反应中,一旦反应物转化为产物,它们就不能再从产物中再生。反应的产物称为正反应,反应物称为反向反应。当正向反应和反向反应的速率相等时,则称反应处于平衡状态。因此,在一段时间内,反应物和产物的量没有变化。可逆反应总是趋向于平衡并保持平衡。当体系处于平衡状态时,产物和反应物的量不一定相等。反应物的数量可能比产物多,反之亦然。平衡方程的唯一要求是随着时间的推移,两者的量都保持恒定。
什么是平衡常数?
对于一个反应,在平衡状态下,可以定义一个平衡常数,其中它等于产物的浓度/活性与反应的浓度/活性之间的比率。
K=[产物]n/[反应物]m;n和m是产物和反应物的化学计量系数。
平衡常数可以有单位,也可以没有单位。如果n等于m,所有的浓度单位都会抵消,K没有单位。如果n与m不同,根据总和,K将保留在一个单位上。平衡常数是恒定温度下的常数。无论介质中反应物或产物的数量如何,平衡常数在恒温下具有相同的值。催化剂或压力变化不影响它。平衡常数可以有几种类型。例如,当弱酸溶解在水中时,它建立平衡,平衡常数也称为酸离解常数。产物或反应物的物理状态也会影响平衡常数,因为方程中不包括固态物种。
什么是反应商?
反应商是在一个特定的时间点,反应产物和反应物之间的比率。它也表示为Q。它的计算方法与平衡常数相同,但在已达到平衡状态的反应中不必使用它。如果计算出的反应商大于平衡常数的值,则反应将以相反的方向进行。相反,当反应商小于平衡常数时,反应物将继续前进。因此,反应商是决定反应方向的重要因素。
| 平衡常数和反应商的区别是什么?•可以计算任何时刻的反应商,而不仅仅是平衡状态下的反应平衡常数。•如果平衡常数等于反应商,则反应处于平衡状态。通过比较K值和Q值,我们可以确定反应的方向。 |