主要区别
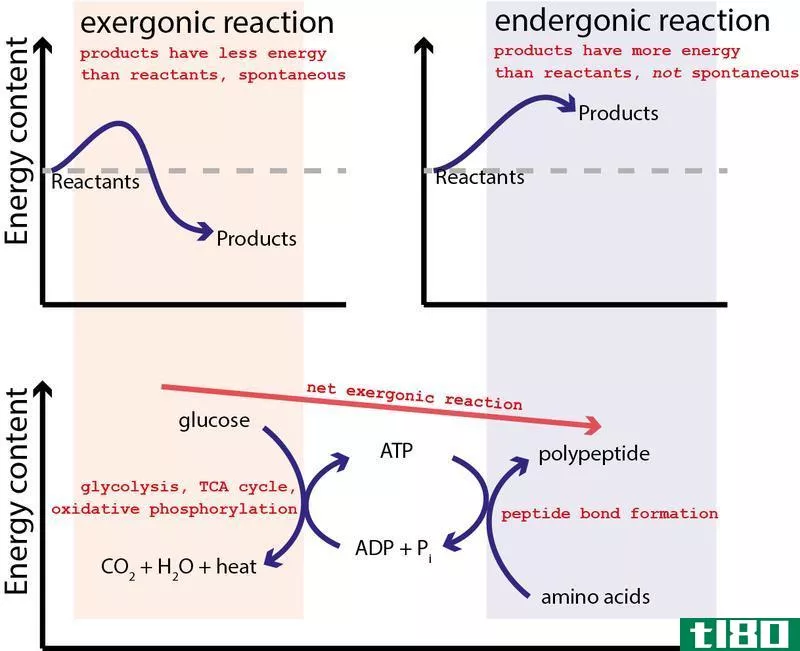
火用反应和能电子反应的主要区别在于,火用反应是自发反应,而能电子反应是非自发反应
火用反应(exergonic reaction) vs. 能电子反应(endergonic reaction)
(火用)是一种具有负吉布斯自由能的有利化学反应。这表明,一个(火用)反应是一个自发反应,因为在这个反应中吉布斯能量为负值。在这种类型的反应中,能量被释放到周围,因此产物的能量比反应物的要低。由于这个原因,焓的变化对火用反应有一个负值。由于系统无序,这个反应的熵增加了。放热反应也包括在火用反应中。相反,能电子反应是吉布斯自由能为正值的反应。非自发性反应也被称为不良反应。在这种类型的反应中,必须从反应的外部提供能量以进行反应。这就是产物比反应物获得更高能量值的原因。焓的变化有一个正值。由于新产品的形成,系统的熵减小。吸热反应也包括在能电子反应中。
当复杂分子被分解时,外显反应也可以被称为分解代谢(代谢的破坏部分),而当新的复杂分子由简单分子形成时,能电子反应也可以被称为合成代谢(代谢的创造性部分)。
比较图
什么是火用反应(exergonic reaction)?
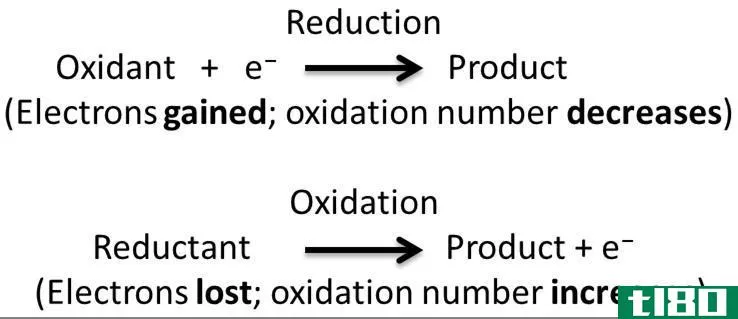
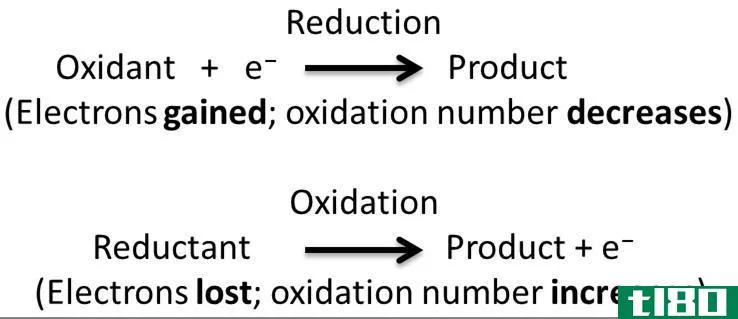
吉布斯自由能是一个热力学势,用来判断一个反应是自发的还是非自发的。Gibbs自由能为负值表示反应是自发的,正值表示反应是非自发的。火用反应是自然界自发发生的不可逆反应。它意味着它已经准备好或者渴望在很少的外部**下发生。这种反应的例子是钠暴露在空气中的氧气中燃烧。燃烧原木是火用反应的另一个例子。这些反应释放出更多的热量,在热力学领域被称为有利反应。在恒定的压力和温度下,吉布斯自由能为负,这意味着更多的能量被释放而不是被吸收。细胞呼吸就是一个典型的例子。当一个葡萄糖分子转化为二氧化碳时,释放了近3012kj的能量。其他的细胞活动所使用的能量。所有的分解代谢反应,例如,碳水化合物、脂肪和蛋白质的分解,都会释放出能量,供生物体工作。有些(火用)反应不是自发发生的,需要少量的能量来启动反应。一旦外部能源满足了这个能量需求,反应就开始打破键并形成新的键,能量在反应发生时被释放。这导致环境中能量的净增加和反应系统能量的净损失。
什么是能电子反应(endergonic reaction)?
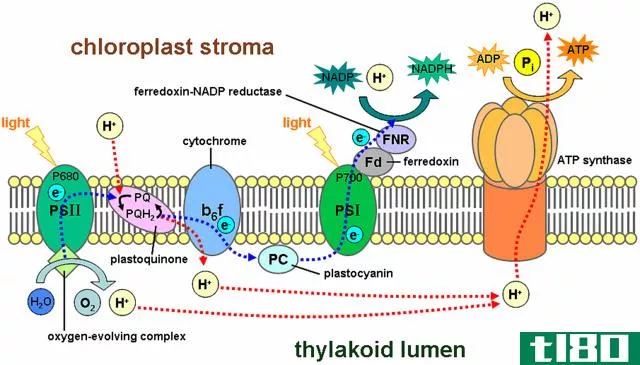
许多化学反应只有在周围有足够的能量供应时才会发生。这些反应本身是不可能发生的。外部能量有助于打破这些联系。使反应继续进行的键断裂释放的能量。这种能量不足以维持反应,需要外部能量。这些反应称为能电子反应。蛋白质合成是一种合成代谢反应,需要小氨基酸**在一起形成蛋白质分子。**肽键需要大量的能量。细胞膜中的钠钾泵参与了钠离子的泵出和钾离子逆浓度梯度的运动,从而实现了呼叫去极化和神经传导。这种反梯度运动需要大量的能量,这些能量来自ATP分子的分解。同样,只有当肌动蛋白和肌球蛋白纤维之间的键断裂形成新的键时,肌肉才会收缩。这也需要大量的能量。植物的光合作用是另一个能引起能量反应的例子。叶子有葡萄糖和水,但不能产生食物。阳光是启动它的外部能源。
主要区别
- 火用反应是自发反应,而能电子反应是非自发反应。
- 火用反应不需要能量,而能电子反应需要能量。
- 在(火用)反应中,能量被释放到环境中,而在电子反应中,能量从周围环境中被吸收。
- 在(火用)反应中,形成的键比被破坏的键强,而在能电子反应中,形成的键比被破坏的键弱。
- 在(火用)反应中,系统的自由能降低,而在能电子反应中,系统的自由能增加。
- 在(火用)反应中,熵变大,而在能电子反应中,熵变小。
- 在(火用)反应中,吉布斯自由能为负值,而在能电子反应中,吉布斯自由能为正值。
结论
从以上讨论可以得出结论,所有的化学反应都可以描述为火用或能电子反应,但两者都有相反的性质。