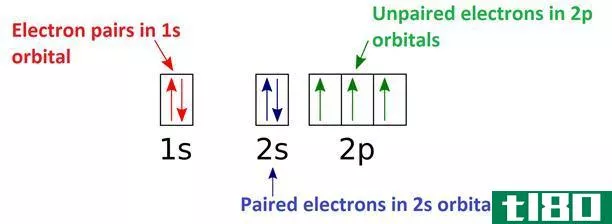
主要区别
键对和孤对的主要区别在于,键对被两个原子核吸引,而孤对只被一个原子核吸引。
键对(bond pair) vs. 单独一对(lone pair)
键对通常考虑存在于键中的一对电子,而孤对则认为通常没有键合的电子对。键对总是以键的形式存在,而孤对通常不存在于键中,但可以通过将孤对捐赠给原子而产生键并产生配位键。键对由两个电子组成,通常属于两个原子;另一方面,孤对由通常属于同一个原子的两个电子组成。
由于两个原子共享两个电子,形成了键对;另一方面,由于原子中不存在空轨道,形成了孤对。键对使用较少的空间,因为它的键对是在其电子云无法在大体积上扩散的地方形成的;另一方面,孤对中的电子通过将其电子云分布在占据更多体积的大表面积上而占据更多空间。
sigma键的一部分是键对,它位于远离中心原子的地方,这导致电子之间的排斥力较小;相反,带负电的孤对通常被中心带正电荷的原子拉近,这在孤对中产生更大的排斥力。键对参与键的形成,而孤对一般不参与键的形成,所以也可以说孤子对被称为无键对。
比较图
什么是键对(bond pair)?
键对是描述键对总是以键的形式存在的术语。单键对通常是由原子的两个电子配对而成,这两个成对的电子一起称为键对。键对使用较少的空间,因为它的键对是在电子云无法在大体积上扩散的地方形成的。
sigma键的一部分是键对,它位于远离中心原子的地方,这导致电子之间的排斥力较小。键对存在于配位化合物和共价化合物中。在共价化合物中,通常共价键是由键对形成的,而在配位化合物中,配位键通常是由键对形成的。
以NH3和BF3为例,其中N原子的电子对表示为BF3分子的B原子。后来,配位键也被称为共价键,电子对现在被认为是键对。
键对类型
- 配位化合物:在这种化合物中,配体通常会把它们的一对孤电子贡献给中心金属原子。产生配位键的孤对类似于两个原子之间的共价键,这是由于键对是由通常属于两个原子的两个电子组成的。
- 共价化合物:在这种化合物中,存在的两个不同的原子共享它们的未成对电子,从而与其他原子形成共享的对电子。这种共享电子形成键的过程称为键对。如果存在双键或三键,则每个键都存在键对。如果存在双键,则表示存在两个键对。然而,共价键是由两个原子的轨道杂化而产生的,这种键对存在于杂化轨道中。两个原子的杂化轨道可以产生π键和sigma键。这意味着可以观察到键对,并将其视为π键和sigma键。
什么是单独一对(lone pair)?
术语孤对可以描述为通常不结合的电子对。孤对由通常属于同一个原子的两个电子组成。孤对一般不参与成键,所以也可以说孤对被称为无键电子对。
然而,原子最内层的电子也被结合在一起,不参与键的形成,因为它们不被认为是孤对。但由于原子中没有空轨道,形成了孤子对。因此,原子中以组合形式存在的价电子被认为是孤对。
有时配位键是在孤对中产生的,由于将配位键捐赠给另一个由空轨道组成的原子而产生的配位键则不被认为是孤对。各种元素只有一个单独对,但许多元素由多个单独对组成。例如,氮原子最多能产生三个共价键。
孤对还可以改变分子中键的角度。E、 g.当一个线性分子有两个键和一个中心原子的形式存在时,如果目前没有孤立的对,这些分子将保持为线性分子。
然而,如果在中心原子中发现一个或多个孤对,那么它将不再是一个线性分子。孤子对中的键对可以被排斥,因为孤子对产生的排斥作用会使分子转化成角的,以代替线性的。
主要区别
- 由于两个电子在两个原子中的分布,形成了键对;另一方面,由于原子中没有空轨道,形成了孤子对。
- 键对是指通常存在于键中的一对电子,而孤对则是指通常不相连的电子对。
- 键对以键的方式连续存在,而孤对可以通过贡献孤对形成键,但通常不存在于键中。
- 键对通常适合于两个原子并包含两个电子;另一方面,孤对通常位于同一个原子的位置,并包含两个电子。
- 键对不需要太多的空间,因为它的连接集产生于电子云不能扩展到很大的地方;另一方面,存在于孤对中的电子通过将其电子云散射到更大体积的外部区域而构成了更大的空间。
- 键对是sigma键的一部分,它存在于远离中心原子的地方,导致电子之间产生较小的排斥力;相反,带负电荷的孤对通常被拉到主要的正电荷原子附近,在孤对中产生更大的排斥力。
- 键对在键形成过程中是复杂的,而孤对也被称为无键对,因为它通常不参与成键。
结论
以上讨论得出结论,键对参与成键,占据的空间较小,斥力较小,而孤对一般不参与成键,因此也可以说孤对是无键对,占据更多空间,具有更大的斥力。