邻位氢和对位氢之间的关键区别在于,邻位氢分子有两个原子核在同一方向上的自旋,而对位氢分子有两个相反方向的原子核自旋。
氢分子(H2)中的氢分子有两种形式:邻氢和对氢。我们根据这些原子的核自旋排列情况将它们分类。因此,我们通常把它们称为自旋异构体。
目录
1. 概述和主要区别
2. 什么是邻氢
3. 什么是对位氢
4. 并列比较-表格形式的正氢和对位氢
5. 摘要
什么是邻氢(ortho hydrogen)?
邻氢分子是含有氢原子的氢分子,其核自旋方向相同。换句话说,两个原子的自旋是平行排列的。它是对位氢的自旋异构体。
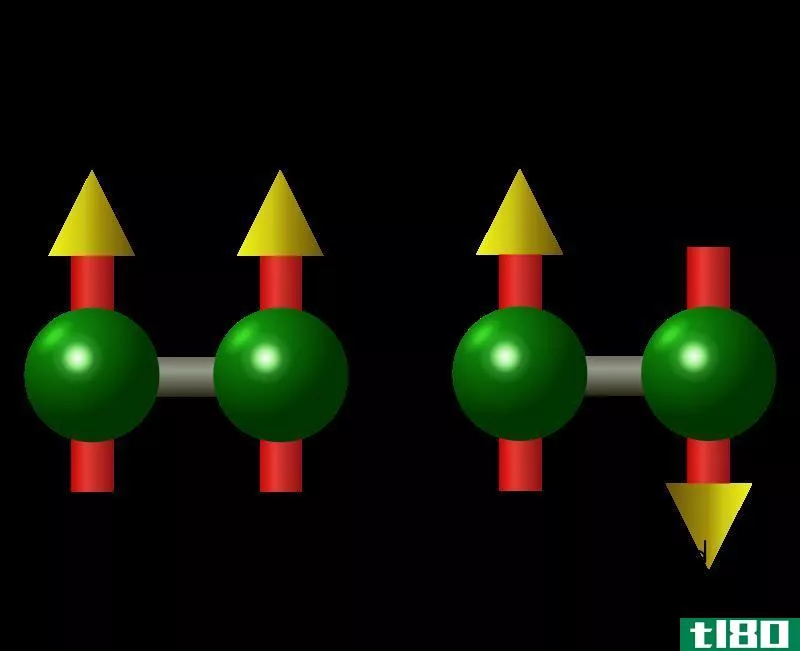
图01:正氢和对位氢比较
然而,这种异构体比对位氢异构体的能量更高。此外,在核磁共振波谱中,邻氢形成三重态。
什么是对位氢(para hydrogen)?
准氢分子是含有氢原子的二氢分子,其核自旋方向相反。这意味着氢分子中每个原子的核自旋是相反的。此外,它是邻氢的自旋异构体。两个氢原子的自旋原子也是反平行排列的。此外,这种同分异构体的能量比邻异构体低。此外,在核磁共振波谱中,这种氢呈现单重态。
正交(ortho)和对位氢(para hydrogen)的区别
邻位氢和对位氢之间的关键区别在于,邻位氢分子有两个原子核在同一方向上的自旋,而对位氢分子有两个相反方向的原子核自旋。当考虑这些分子的能量时,邻氢比对位氢具有更高的能量状态。此外,在核磁共振波谱中,邻氢为三重态,对位氢为单重态。

总结 - 正交(ortho) vs. 对位氢(para hydrogen)
基本上,邻位氢和对位氢是两种氢分子,我们可以根据氢原子的自旋进行分类。邻位氢和对位氢之间的关键区别在于,邻位氢分子有两个原子核在同一方向上的自旋,而对位氢分子有两个相反方向的原子核自旋。
引用
1.“邻位和对位氢。”化学歌词,歌词,2019年6月5日,可在此处查阅。