关键区别–kc与kp
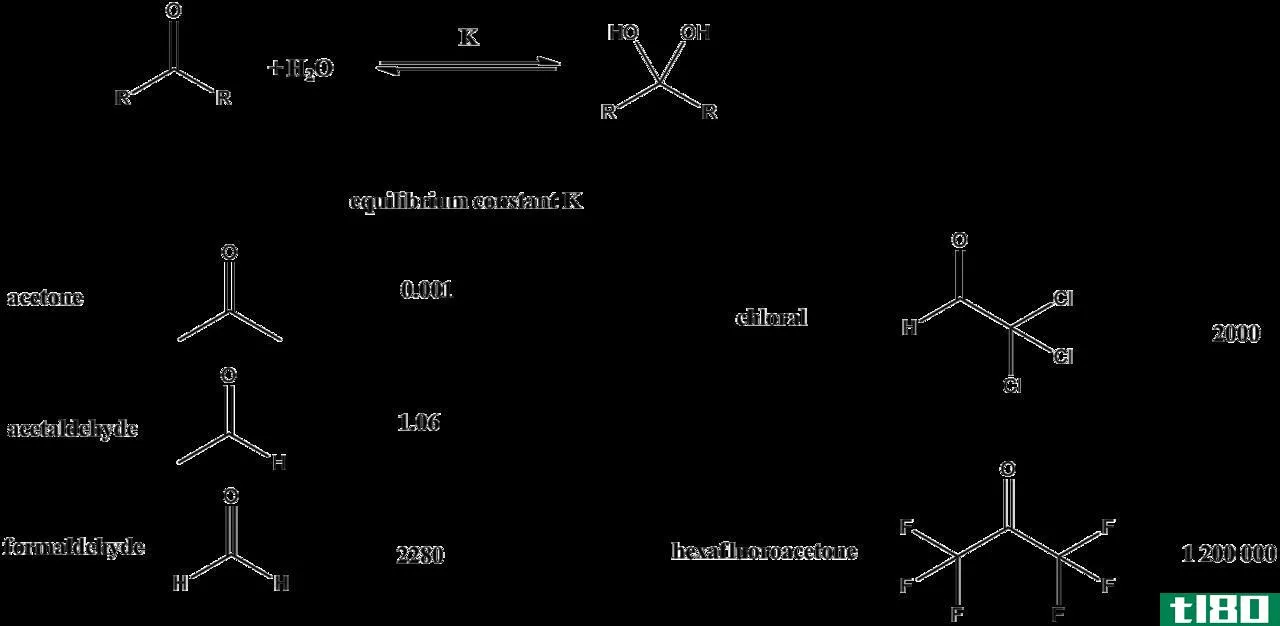
Kc和Kp是平衡常数。反应混合物的平衡常数是表示反应混合物中产物和反应物的浓度或压力之比的数字。Kc和Kp的关键区别在于Kc是由浓度项给出的平衡常数,而Kp是由压力项给出的平衡常数。
这个平衡常数是可逆反应的。Kc是产物和反应物浓度之比的平衡常数,而Kp是产物和反应物压力之比的平衡常数。
目录
1. 概述和主要区别
2. 什么是Kc
3. 什么是Kp
4. Kc与Kp的关系
5. 并列比较——Kc与Kp的表格形式
6. 摘要
什么是kc公司(kc)?
Kc是产物和反应物浓度之比的平衡常数。组分的摩尔浓度用于Kc的表达。
aA+bB型↔ 抄送+dD
上述反应的平衡常数可以写成:
[天]
[A] ,[B]、[C]和[D]是A、B反应物和C、D产物的浓度。指数“a”、“b”、“c”和“d”是化学方程式中每种反应物和产物的化学计量系数。在Kc的表达式中,反应物和产物的浓度被提高到与其化学计量系数相等的幂次。
什么是kp公司(kp)?
Kp是平衡常数,以产物和反应物的压力之比表示。该平衡常数适用于气体反应混合物。Kp取决于反应混合物中气体成分的分压。

图1:混合物中气体成分的分压。
pP+qQ↔ rR+sS
上述反应的平衡常数可以写成:
Kp=pRr.pSs/ 购买力平价
“p”表示分压。因此,pP、pQ、pR和pS是P、Q、R和S气体组分的分压。指数“p”、“q”、“r”和“s”是化学方程式中每种反应物和产物的化学计量系数。
什么是kc与kp的关系(the relati***hip between kc and kp)?
Kp=Kc(RT)Δn
式中,Kp为压力平衡常数,Kc为浓度平衡常数,R为通用气体常数(8.314jmol-1K-1),T为温度,Δn为气体产物总摩尔数与气体反应物总摩尔数之差。
kc公司(kc)和kp公司(kp)的区别
| Kc与Kp | |
| Kc是产物和反应物浓度之比的平衡常数。 | Kp是平衡常数,以产物和反应物的压力之比表示。 |
| 反应物 | |
| Kc可用于气态或液态反应混合物。 | Kp仅用于气态反应混合物。 |
| 单位 | |
| Kc由浓度单位表示。 | Kp由压力单位给出。 |
总结 - kc公司(kc) vs. kp公司(kp)
反应混合物的平衡常数用浓度(Kc)或分压(Kp)来解释反应混合物中产物和反应物之间的比率。Kc和Kp的关键区别在于Kc是由浓度项给出的平衡常数,而Kp是由压力项给出的平衡常数。
引用
1这里是“恒定韦氏平衡”。“气体平衡常数:Kc和Kp。”化学图书馆,图书馆,2016年7月21日,可在这里查阅。
2“气体平衡常数:Kc和Kp”,《化学图书馆》,图书馆,2016年7月21日,