主要区别
离子键和共价键的主要区别是电子对和原子的共享。在共价键中,原子在相互作用过程中被静电吸引,而在离子键中,原子之间共享电子对。
比较图
共价键
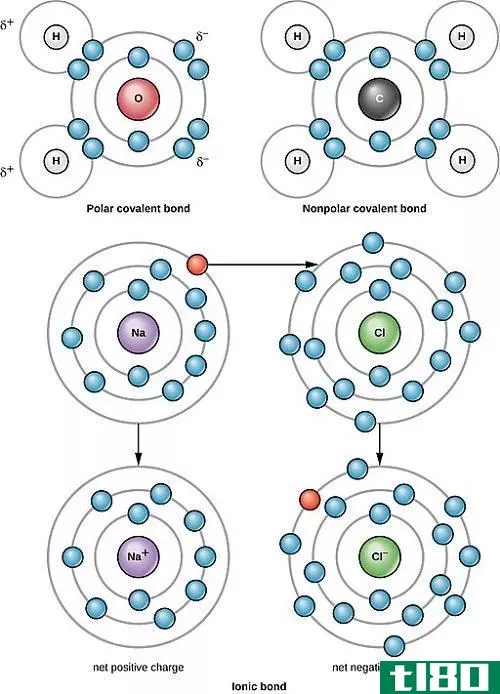
共价键是一种化学键,其特征是原子间共享对或键对(电子对)的共享。在大多数分子中,共享的电子使每个原子都能得到一个完整的外壳,类似于逐渐的数字配置。若原子对电子有相似的亲和力,共价键很容易发生,因为它们对电子的亲和力相同,而且不倾向于由原子捐赠。原子共享电子以获得八位元组态,并成长为更规则和更强的。由于sigma和pi轨道的相互作用,共价键可以分为四类,特别是单键、双键、三键和四重键。氧原子是最重要的场合,它需要另外两个电子来形成一个封闭的壳层,而氢原子需要一个电子来形成一个封闭的壳层。氧原子与氢原子共用两个电子,因此每个原子都有闭合的壳层。从长远来看,这会产生一个水分子。
离子键
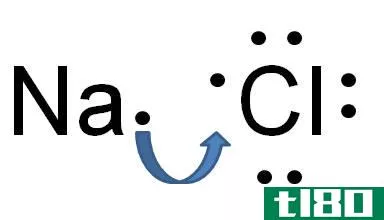
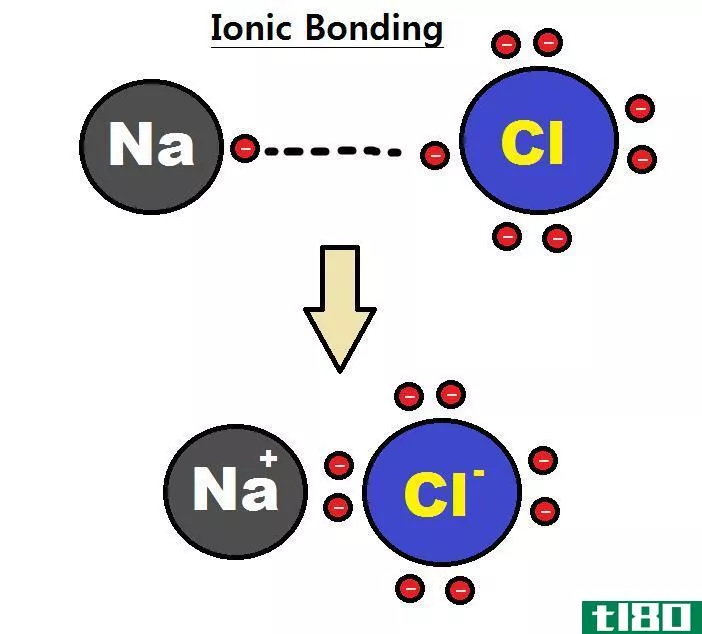
离子键是一种化学键的形式,其特征是一个原子将不同的电子共享或全部移交给一个不同的原子。离子键是容易失去电子的元素和获得电子的元素的产物。由于电荷之间的相互作用,如库仑定律所述,这些类型的键不适用于分子。离子键在室温下保持稳定是因为,在所有具有数十亿种离子的周期性晶格中,每个离子都被许多价格相反的离子包围。敌对离子和建设性离子之间的静电好奇因素共同保护了化合物。离子键合过程中的正常活力一般是建设性的,说明反应是吸热的,是不利的。另一方面,由于它们的静电吸引力,这种响应在同一时间是有利的。离子键的典型情况是钠或盐。钠原子很快就会产生电子,从而产生一个建设性的价格。氯接受这些电子并带负电。这两个带相反电荷的原子互相吸引形成氯化钠分子。
主要区别
- 在共价键中,电子轨道是重叠的,而离子键则是分开的。
- 与离子键相比,共价键相对容易,离子键可能很难和易碎。
- 金属原子和非金属原子都参与了离子键的形成,而共价键的形成则只涉及非金属原子。
- 共价键是由于共享电子而形成的,而离子键的形成是由于电子的转移。
- 分子是通过化合物形成的共价键中的粒子,而在离子键中则是带正电荷和负电荷的离子。
- 共价键是非导体,而离子键是导体。
- 共价键发生在电负性几乎完全不同的原子之间。离子键发生在电负性好的原子之间。
- 在离子键合的情况下,离子键需要极高的熔融度和沸点。共价键在共价键合的情况下,要求熔点和沸点较低。
- 甲烷和氢氯酸是普遍存在的共价氯化钠和硫酸是离子键的例子。
- 共价键有选择的类型,而离子键没有任何特定的类型
- 共价键具有低极性,而离子键具有极性。
- 100%的共价分子能溶于油,但不溶于水,而许多离子键却能溶于水而不溶于油。
- 共价键之所以重要,是因为碳分子主要通过共价键共同工作,而离子键之所以重要,是因为它们允许合成特定的纯化合物。
- 共价键可能是所有元素和化合物,而离子键可能是唯一的化合物。