溶解度与溶解性
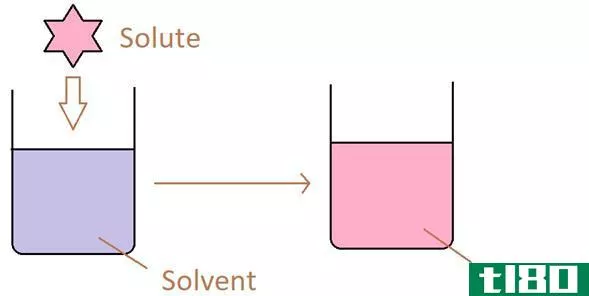
这两个术语是齐头并进的,指的是同一种化学情景,在定义上有两种不同的观点。作为概念的背景,首先要理解这里涉及的三个基本成分:溶质、溶剂和溶液。溶质是溶解在溶剂中的化合物。溶剂通常是用来溶解溶质的液体。溶液是指溶解在溶剂中的溶质形成的混合物。溶质可以是固体、液体或气体,即使溶剂通常是液体,也可以有固体和气体溶剂。E、 金属合金可以看作是固体溶质与固体溶剂混合的固溶体。“溶解度”是溶质的一种特性,“溶解”是溶质溶解在溶剂中形成溶液的过程。因此,根据定义,溶解度是一个热力学因素,溶解是一个动力学因素。
溶解度
溶解度是溶质的一种性质,它决定溶质在溶剂中溶解的程度,从而形成特定的溶液。溶质的化学和物理特性在决定其溶解度方面起着重要作用。当我们提到溶液的浓度时,我们指的是特定溶质在溶剂中的溶解度。在溶液相中,一种特定溶剂所能容纳的溶质量是有限度的。超过这个限度,如果溶质进一步溶解,它将在底部开始沉淀。这两种状态之间的动态平衡决定了溶解度的大小。因此,当溶解速率等于沉淀速率时,就会发生溶解度。溶解度可以量化,单位为摩尔/千克。
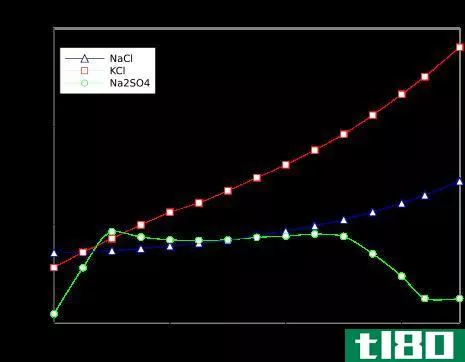
一般来说,我们在溶解度上遵循一条经验法则,即“类溶于类”。这一观点表明,极性化合物在极性溶剂中有更大的溶解倾向,反之亦然。当溶质完全可溶时,我们说它是可混溶的。对于两种液体(当一种液体与另一种液体混合)的情况下,这种情况更为常见。当溶解度较低时,我们称该化合物不易溶解或不溶。一种物质在另一种物质中的溶解度取决于溶质和溶剂分子之间分子间作用力的大小,各种物理和热力学因素都会影响溶解度的大小。E、 温度、压力、溶剂的极性、溶液中常见离子的过量或不足等。一般情况下,当温度较高时,某一特定溶质的溶解度高于较冷时的溶解度。有时,溶解可能是由于化学反应而不是溶质的纯溶解度引起的。这不应与溶解度混淆。当一种溶质是纯可溶的,那么在溶剂蒸发之后,人们应该能够再次获得溶质。
溶解
溶解是溶质溶解在溶剂中形成溶液的过程。因此,这有一个动力学效应。溶解可以以不同的速率发生,有时溶质完全溶解在溶剂中可能需要相当长的时间。在溶解过程中,溶质的结构完整性被分解成单独的组分、分子或原子,溶解的结果称为溶解度。溶解也受溶解度相似的物理原理控制,但溶解本身是一个动力学过程。离子化合物很容易溶于水,如上所述,这里也可以计算“同类溶解”原理。溶解速率取决于各种因素;机械混合、溶剂和溶质的性质、溶解物质的质量、温度等。溶解可以用单位摩尔/秒来量化。
溶解性和溶解性有什么区别?
•溶解是溶质溶解在溶剂中形成溶液的过程,而溶解度是溶解的结果。
•溶解度是一个热力学实体,而溶解是动力学的。