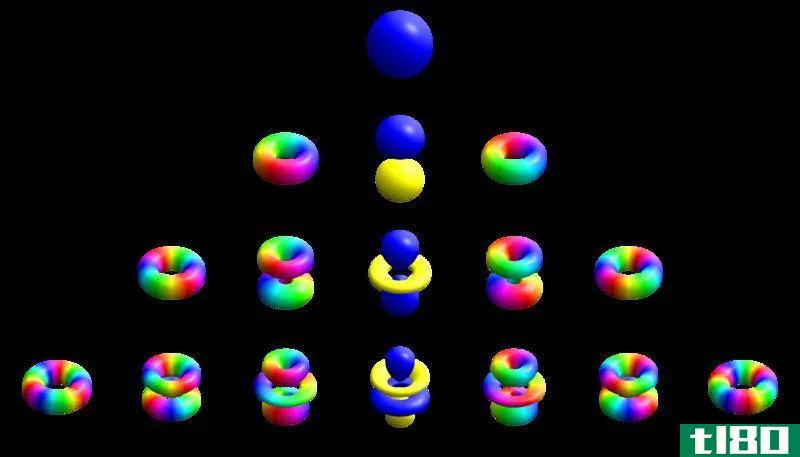方位量子数定义
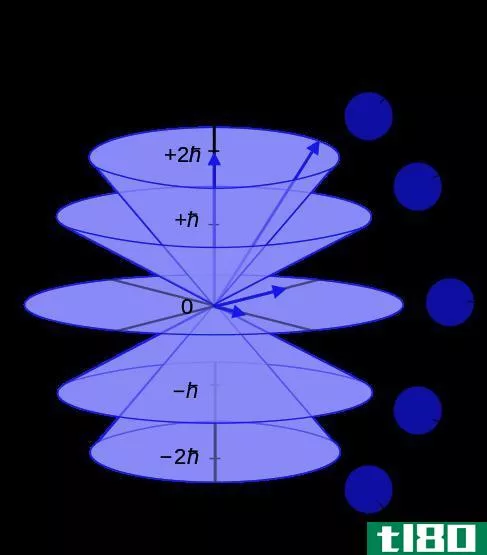
方位量子数,ℓ, 是与原子电子的角动量有关的量子数。它也被称为角动量量子数或第二量子数。角动量量子数决定了电子轨道的形状。Arnold Sommerfeld根据原子的玻尔模型提出了方位量子数。

量子数
方位量子数为:
- 本征角动量量子数(自旋量子数)
- 磁量子数
- 轨道角动量量子数
- 总角动量量子数
例子
p轨道与等于1的方位量子数有关。
来源
- 罗伯特·艾斯伯格(1974年)。原子、分子、固体、原子核和粒子的量子物理学。纽约:约翰·威利父子公司,第114-117页。ISBN 978-0-471-23464-7。
- 林赛,R.B.(1927年)。关于原子模型中“钟摆”轨道的注记。纳特尔。阿卡德。Sci。13: 413–419. 内政部:10.1073/pnas.13.6.413
- 发表于 2021-09-20 18:27
- 阅读 ( 224 )
- 分类:化学
你可能感兴趣的文章
方位角(azimuthal)和主量子数(principal quantum number)的区别
方位角量子数和主量子数的关键区别在于,方位角量子数描述的是原子中电子的角动量,而主量子数描述的是电子轨道的大小。 量子数是描述原子能级的重要数值。我们可以用四个量子数来描述电子在原子中的位置。它们是...
- 发布于 2020-10-07 18:13
- 阅读 ( 680 )
轨道图(orbital diagram)和电子组态(electron configuration)的区别
...壳层所能容纳的最大电子数。在这里,这个最大数取决于方位角量子数l。此外,l=0、1、2和3分别表示s、p、d和f轨道。一个壳层能容纳的最大电子数=2(2l+1)。因此,我们可以制定下表; 轨道 最大电子数2(2l+1) L=0...
- 发布于 2020-10-14 00:32
- 阅读 ( 738 )
px py公司(px py)和pz轨道(pz orbitals)的区别
...子数: 主量子数(n)描述了电子壳层。例:n=1,2,3… 方位角量子数或角动量量子数(l)解释了子壳层。例:l=0,1,2… 磁量子数(m)表示电子的唯一量子态。例:m=…-2,-1,0,+1,+2… 自旋量子数描述电子的自旋。示例:s...
- 发布于 2020-10-14 02:27
- 阅读 ( 945 )
磁量子数(magnetic quantum number)和自旋量子数(spin quantum number)的区别
磁性量子数和自旋量子数的关键区别在于,磁量子数在区分子壳层内可用的轨道时很有用,而自旋量子数则描述了轨道的能量、形状和方向。 量子数是描述原子中电子的唯一量子态的一组值。具体的量子数有四种:主量子数...
- 发布于 2020-10-15 03:08
- 阅读 ( 1281 )
玻尔(bohr)和量子模型(quantum model)的区别
玻尔(bohr)和量子模型(quantum model)的区别 玻尔模型和量子模型是解释原子结构的模型。玻尔模型又称卢瑟福玻尔模型,因为它是对卢瑟福模型的修正。玻尔模型是尼尔斯·玻尔在1915年提出的。量子模型是原子的现代模型。玻尔...
- 发布于 2020-10-25 03:52
- 阅读 ( 554 )
壳次壳(shell subshell)和轨道(orbital)的区别
...。壳层-子壳层和轨道的主要区别在于壳层由共享相同主量子数的电子组成,子壳层由共享相同角动量量子数的电子组成,而轨道由处于相同能级但自旋不同的电子组成。 覆盖的关键领域 1.什么是壳-定义、结构和属性2.什么是子...
- 发布于 2021-06-29 12:03
- 阅读 ( 1241 )
s轨道(s orbital)和p轨道(p orbital)的区别
...因此而得名。由于原子轨道是由一个确定的能级(能量是量子化的)组成的,所以它们被赋予一个量子数。S轨道指定原子的角动量量子数。 Figure 1: The size of the s orbital increases with the increasing of principle quantum number s轨道上的两个...
- 发布于 2021-06-29 12:41
- 阅读 ( 801 )
玻尔(bohr)和量子模型(quantum model)的区别
玻尔的主要区别(main difference bohr) vs. 量子模型(quantum model) 许多科学家提出了不同的模型来解释原子的结构。玻尔模型和量子模型就是这样两种模型。玻尔模型是一种先进的模型,但它不能解释大原子线谱中观察到的塞曼效应和...
- 发布于 2021-06-29 18:32
- 阅读 ( 471 )
径向的(radial)和角节点(angular nodes)的区别
...电子壳层。这些电子壳层是由子壳层组成的。根据角动量量子数,子壳层包含一个或多个轨道:s轨道、p轨道、d轨道和f轨道。这些轨道可以在不同的平面上。一个特定平面上的每个轨道称为波瓣。在这些波瓣中发现了电子。但...
- 发布于 2021-06-29 21:27
- 阅读 ( 1503 )